
| A. | 摩尔是国际单位制中7个基本物理量之一 | |
| B. | 物质的量就是物质的质量 | |
| C. | 物质的量像一座桥梁,把物质的质量或体积等宏观量与微观粒子的数量联系起来 | |
| D. | 是表示物质数量的单位 |
分析 A、物质的量是七个基本物理量之一;
B、物质的量是衡量微粒个数集合体的一个物理量;
C、根据物质的量n=$\frac{N}{{N}_{A}}$=$\frac{V}{Vm}$等公式来理解;
D、物质的量是表示微粒数目的集合体.
解答 解:A、物质的量是七个基本物理量之一,其单位为摩尔,故摩尔不是物理量,故A错误;
B、物质的量是衡量微粒个数集合体的一个物理量,与物质的质量是两个不同的概念,故B错误;
C、由于物质的量n=$\frac{N}{{N}_{A}}$=$\frac{m}{M}$=$\frac{V}{Vm}$,故物质的量将质量、体积和微粒个数等联系起来,故C正确;
D、物质的量是表示微粒数目的集合体,不是物质数量的单位,故D错误.
故选C.
点评 本题考查了物质的量和其单位--摩尔,应注意的是物质的量是衡量微粒个数集合体的一个物理量,其单位是摩尔,故摩尔是七个基本物理量的单位之一.


 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:选择题
 下列各组物质依次满足如图所示转化关系的是(图中箭头表示一步转化)( )
下列各组物质依次满足如图所示转化关系的是(图中箭头表示一步转化)( )| a | b | c | d | |
| ① | Si | SiO2 | H2SiO3 | Na2SiO3 |
| ② | N2 | NO | NO2 | HNO3 |
| ③ | Cu | CuO | Cu(OH)2 | CuSO4 |
| ④ | Na | NaCl | Na2CO3 | NaHCO3 |
| A. | ①② | B. | ②③ | C. | ③④ | D. | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{12b}{a}$或b•NA | B. | $\frac{12b}{a}$或a•NA | C. | $\frac{12a}{b}$或a•NA | D. | $\frac{12a}{b}$或b•NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题




 (注明反应条件),因此,在碱性条件下,由Ⅳ与
(注明反应条件),因此,在碱性条件下,由Ⅳ与 反应生成Ⅱ,其反应类型为取代反应.
反应生成Ⅱ,其反应类型为取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铝和氢氧化钾都是重要的工业产品,请回答问题:
铝和氢氧化钾都是重要的工业产品,请回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
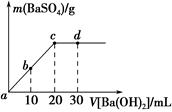 常温下,向0.25mol•L-1的硫酸氢钠溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中正确的是( )
常温下,向0.25mol•L-1的硫酸氢钠溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中正确的是( )| A. | 硫酸氢钠溶液的体积为10 mL | |
| B. | 溶液的导电能力:c<b<a | |
| C. | d时刻溶液的pH为13 | |
| D. | b时刻溶液中SO42-的浓度约为0.125 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com