
【题目】某硫酸工厂运用电化学原理设计了如图所示的装置,实现了用SO2发电的同时制备硫酸。图中电极是含催化剂、多孔吸附性的惰性材料。下列说法正确的是
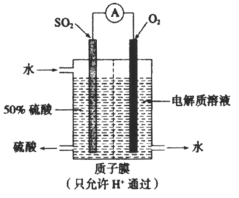
A.通入SO2气体的一极是负极,发生还原反应
B.正极的电极反应:O2+4e=2O2
C.该装置工作时的总反应:2SO2+O2+2H2O=2H2SO4
D.氢离子向负极区移动,与负极生成的SO42结合形成硫酸
【答案】C
【解析】
据图可知二氧化硫被氧化成硫酸根,所以通入二氧化硫的一极为负极,根据电解质溶液的成分可知电极反应式为:SO2-2e-+2H2O=SO![]() +4H+;通入氧气的一极为正极,电极反应式为O2+4e-+4H+=2H2O。
+4H+;通入氧气的一极为正极,电极反应式为O2+4e-+4H+=2H2O。
A.根据分析可知通入二氧化硫的一极为负极,失电子发生氧化反应,故A错误;
B.正极上是氧气得电子的还原反应,在酸性环境下生成水,正确的反应为:O2+4e-+4H+=2H2O,故B错误;
C.负极上是燃料二氧化硫失电子的氧化反应,正极上是氧气得电子的还原反应,总反应为:2SO2+O2+2H2O=2H2SO4,故C正确;
D.原电池中阳离子流向正极,故D错误;
综上所述答案为C。


科目:高中化学 来源: 题型:
【题目】天门冬氨酸锌是一种补锌剂,可以![]() 、天门冬氨酸(
、天门冬氨酸(![]() )为原料制备。回答下列问题:
)为原料制备。回答下列问题:
(1)Zn成为阳离子时首先失去______轨道电子。碲(Te)与O同主族,则Te元素中电子占据的能量最高的能级是______。
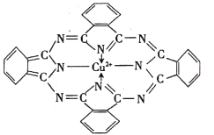
(2)P是N的同族元素,PH3与NH3中稳定性更高的是______(填化学式),其判断理由是______;酞菁铜可用于生产蓝色颜料(结构如图),其中C原子的轨道杂化类型为______。
(3)CO为______(填“极性”或“非极性”)分子。
(4)ZnO晶体的一种晶胞结构如图:
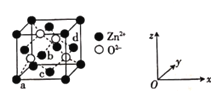
①![]() 的配位数为____________。
的配位数为____________。
②以晶胞边长为单位长度建立的坐标系可表示晶胞中锌原子的位置,称作原子分数坐标。图中原子a的分数坐标为![]() ,原子d的分数坐标为
,原子d的分数坐标为![]() ,则原子b和c的分数坐标分别为______、______。
,则原子b和c的分数坐标分别为______、______。
③设![]() 为阿伏加德罗常数的值。已知晶胞边长为
为阿伏加德罗常数的值。已知晶胞边长为![]() nm,则ZnO晶体的密度为______(列出计算式)
nm,则ZnO晶体的密度为______(列出计算式)![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质结构和性质的叙述不正确的是( )
A.甲苯可以被酸性![]() 溶液氧化成苯甲酸,而乙烷不能被其氧化,说明苯环对侧链产生了影响
溶液氧化成苯甲酸,而乙烷不能被其氧化,说明苯环对侧链产生了影响
B.苯酚能与氢氧化钠溶液反应而乙醇不能,说明苯环对羟基产生了影响
C.二氯甲烷只有一种结构,说明甲烷的分子构型不是平面型
D.间二甲苯只有一种结构,说明苯环中不存在单双键交替出现的结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作会引起实验结果偏高的是( )
A.测定硫酸铜晶体中结晶水含量的实验中,晶体加热完全失去结晶水后,将盛试样的坩埚放在实验桌上自行冷却
B.镀锌铁皮锌镀层厚度测量实验中,将铁皮用酒精灯持续加强热以彻底烘干
C.用标准碱滴定待测酸溶液时,装有标准碱的滴定管滴定前无气泡,滴定后有气泡
D.一定物质的量浓度的盐酸配制过程中用量筒量取计算所需的浓盐酸时,仰视观察刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用乙酸和正丁醇(![]() )制备乙酸正丁酯,制备过程如下:
)制备乙酸正丁酯,制备过程如下:
①在干燥的![]() 圆底烧瓶中,加入一定量的正丁醇和冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石。按下图所示安装带分水器的回流反应装置,并在分水器中预先加入水,使水面略低于分水器一分水器的支管口。
圆底烧瓶中,加入一定量的正丁醇和冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石。按下图所示安装带分水器的回流反应装置,并在分水器中预先加入水,使水面略低于分水器一分水器的支管口。
②打开冷凝水,圆底烧瓶在石棉网上用小火加热。在反应过程中,通过分水器下部的旋塞不断分出生成的水,注意保持分水器中水层液面原来的高度,使油层尽量回到圆底烧瓶中。反应达到终点后,停止加热,记录分出的水的体积。
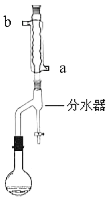
请回答有关问题:
(1)冷凝水的流向为________进________出(填a或b)。
(2)步骤②中不断从分水器下部分出生成的水的目的是________________。步骤②中判断反应终点的依据是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是
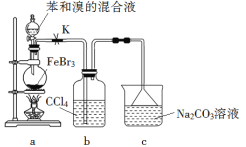
A. 向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B. 实验中装置b中的液体逐渐变为浅红色
C. 装置c中的碳酸钠溶液的作用是吸收溴化氢
D. 反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.1mol·L-1的盐酸中逐滴加入0.1 mol·L-1的氨水,溶液pH的变化与加入氨水的体积关系如图所示。下列叙述不正确的是
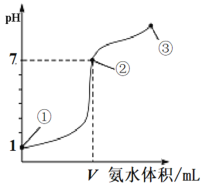
A.V>20 mL
B.①、②、③点水的电离程度大小为:②>③>①
C.在点②所示溶液中:c(Cl-)=c(NH3·H2O)+c(NH![]() )
)
D.在点②、③之间可能存在:c(NH![]() )>c(Cl-)=c(OH-)>c(H+)
)>c(Cl-)=c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、![]() 太阳能电池及铜铟镓硒薄膜太阳能电池等。
太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)基态![]() 原子的价层电子排布式为_______________。
原子的价层电子排布式为_______________。
(2)高温下![]() 容易转化为
容易转化为![]() ,试从原子结构角度解释原因:_______________。
,试从原子结构角度解释原因:_______________。
(3)乙醇的沸点高于乙烷的沸点,其原因是______________。
(4)![]() 的立体构型为________。
的立体构型为________。
(5)硼酸![]() 本身不能电离出
本身不能电离出![]() ,在水中易结合一个
,在水中易结合一个![]() 生成
生成![]() ,而体现弱酸性。
,而体现弱酸性。
①![]() 中含有配位键,其中提供空轨道的是________(填元素符号)。
中含有配位键,其中提供空轨道的是________(填元素符号)。
②![]() 的结构式为________。
的结构式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项比较中前者高于(或大于或强于)后者的是
A. 金属Mg(六方最密堆积)和金属Cu(面心立方最密堆积)的空间利用率
B. BF3和CH4中心原子的价层电子对数
C. Si-O和C-O的键能
D. 对羟基苯甲醛(![]() )和邻羟基苯甲醛(
)和邻羟基苯甲醛(![]() )的沸点
)的沸点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com