
有七种物质:① 铝,② A12O3,③ 稀硝酸,④ NaHCO3,⑤ Ba(OH)2
固体,⑥ 氨水,⑦ A12(SO4)3,根据下列要求回答问题:
(1)属于电解质的是 (填序号)。
(2)既能与强酸反应,又能与强碱反应的是 (填序号)。
(3)34.2 g ⑦ 溶于水配成500 mL溶液,溶液中SO42-的物质的量浓度为 。
(4)①与③发生反应的化学方程式为A1+4HNO3=A1(NO3)3+NO↑+2H2O,该反应中还原剂
与氧化剂的物质的量之比是 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
能正确表示下列化学反应的离子方程式
的是 ( )
A.向碳酸氢铵溶液中加入过量的NaOH固体 NH4++OH-= NH3↑+H2O
B.澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C.铜片插入硝酸银溶液中 Cu + Ag+ = Cu2+ + Ag
D.碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
在溶液中能大量共存,加入OH-有沉淀析出,加入H+有气体 放
放
出的是( )
A.Na+、Cu2+、Cl-、SO42- B.Na+、Ca2+、Cl-、HCO3-
C.H+、Al3+、OH-、NO3- D.Fe3+、K+、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能大量共存的是( )
A.Na+、Al3+、NO3-、H+ B.Ba2+、Na+、Cl-、SO42-
C.Mg2+、H+、SO42-、OH- D.H+、Na+、CO32-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.固体氯化钠不导电,所以氯化钠不是电解质
B.虽然NaHSO4溶于水能电离出H+,但它不是酸
C.“纳米材料”是粒子直径1~100 nm的材料,它属于胶体
D.在一个氧化还原 反应中,有一种元素被氧化肯定有另一种元素被还原
反应中,有一种元素被氧化肯定有另一种元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
下列微粒的核外电子的表示方法中正确的是( )
|
| A. | 碳原子 |
|
| B. | P原子价电子轨道表示式 |
|
| C. | Cr原子的价电子排布式3d44s1 |
|
| D. | Fe2+价电子排布式3d44s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是(NA为阿伏加德罗常数)( )
|
| A. | 124g P4含有P﹣P键的个数为4NA |
|
| B. | 12g石墨中含有C﹣C键的个数为3NA |
|
| C. | 12g金刚石中含有C﹣C键的个数为2NA |
|
| D. | 60g SiO2中含Si﹣O键的个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第八列 |
(1)已知BA5为离子化合物,是由 、 两种微粒构成的(填化学符号).
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈 形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,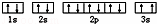 该同学所画的电子排布图违背了 .
该同学所画的电子排布图违背了 .
(4)G位于 族,G3+价电子排布式为 .GE3常温下为固体,熔点282℃,沸点315℃,在300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断GE3的晶体类型为 .
(5)DE3中心原子的杂化方式为 ,其空间构型为 .
(6)前四周期中与F同一族的所有元素分别与E元素形成化合物,其晶体的熔点由高到低的排列顺序为(写化学式) ,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.2mol两种气态组成的混合气完全燃烧后得到6.72升二氧化碳(标准状况下)和7.2克水,下列说法正确的是 ( )
A. 一定有乙烷 B. 一定有甲烷 C. 一定没有甲烷 D. 一定没有乙烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com