
分析 (l)三价铁水解生成的氢氧化铁胶体具有净水作用;
(2)根据反应Fe(OH)3+3H+?Fe3++3H2O的平衡常数K=$\frac{c(F{e}^{3+})}{{c}^{3}({H}^{+})}$=$\frac{c(F{e}^{3+})}{{c}^{3}({H}^{+})}$×$\frac{{c}^{3}(O{H}^{-})}{{c}^{3}(O{H}^{-})}$=$\frac{{K}_{sp}(Fe(OH)_{3})}{{K}_{w}}$计算;
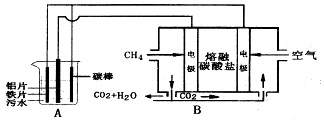
(3)B能自发的进行氧化还原反应,为原电池,通入甲烷的电极为负极,发生氧化反应,负极电极反应是CH4+4CO32--8e-=5CO2+2H2O,通入空气的一极为正极,发生还原反应,正极反应为O2+2CO2+4e-=2CO32-;A有外接电源,属于电解池,电解池中Fe和碳棒为阳极,发生Fe-2e-=Fe2+,Al为阴极,阴极的电极反应为:2H++2e-=H2↑,二价铁离子具有还原性,能被氧气氧化到正三价,4Fe2++10H2O+O2=4Fe(OH)3↓+8H+,据此分析解答.
①通入空气的一极为正极,发生还原反应;
②A有外接电源,属于电解池,根据阳极电极材料和离子的放电顺序考虑放电的离子,并书写电极反应式;
③能使导电能力增强的电解质必须是易溶于水的,且只能是中性的;
(4)①草酸被H2O2氧化生成水和二氧化碳;
②K3[Fe(C2O4)3]•3H2O中的铁为亚铁离子,而铁离子遇KSCN溶液变为血红色.
解答 解:(1)氯化铁为强酸弱碱盐,在水中发生水解,三价铁水解生成的氢氧化铁胶体具有净水作用,原理方程式为:Fe3++3H2O?Fe(OH)3(胶体)+3H+,
故答案为:Fe3++3H2O?Fe(OH)3(胶体)+3H+;
(2)已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,Fe(OH)3+3H+?Fe3++3H2O的平衡常数K=$\frac{c(F{e}^{3+})}{{c}^{3}({H}^{+})}$=$\frac{c(F{e}^{3+})}{{c}^{3}({H}^{+})}$×$\frac{{c}^{3}(O{H}^{-})}{{c}^{3}(O{H}^{-})}$=$\frac{{K}_{sp}(Fe(OH)_{3})}{{K}_{w}}$=$\frac{2.79×1{0}^{-39}}{(1×1{0}^{-14})^{3}}$=2.79×103,
故答案为:2.79×103;
(3)①通入空气的一极为正极,发生还原反应,B中电解质为熔融碳酸盐,所以正极反应式为O2+2CO2+4e-=2CO32-,
故答案为:O2+2CO2+4e-=2CO32-;
②电解时铁作阳极,因此主要发生Fe-2e-=Fe2+,同时也发生副反应,即溶液中的OH-失电子被氧化生成O2,4OH--4e-=2H2O+O2↑,
故答案为:4OH--4e-=2H2O+O2↑;
③保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀时,加入的使导电能力增强的电解质必须是可溶于水的、显中性的盐,所以c符合,
故答案为:c;
(4)①草酸被H2O2氧化生成水和二氧化碳,该反应为H2C2O4+H2O2=2CO2↑+2H2O,
故答案为:H2C2O4+H2O2=2CO2↑+2H2O;
②K3[Fe(C2O4)3]•3H2O中的铁为亚铁离子,则不能用KSCN溶液检验K3[Fe(C2O4)3]•3H2O中的铁元素,检验铁元素的方案为取适量晶体加热,取固体残留物溶解在H2SO4中,取上层清液于试管中,滴加KSCN溶液.若溶液呈血红色则有铁元素,反之则无,
故答案为:取适量晶体加热,取固体残留物溶解在H2SO4中,取上层清液于试管中,滴加KSCN溶液,若溶液呈血红色则有铁元素,反之则无.
点评 本题考查知识点较多,涉及盐类水解、沉淀溶解平衡、原电池和电解池原理、离子检验等知识,为高频考点,侧重考查学生分析计算能力,明确原电池和电解池区别、各个电极上发生的反应、转移电子守恒是解本题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Cu溶于稀HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O | |
| B. | 用石墨电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ | |
| D. | 向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4项 | B. | 5项 | C. | 6项 | D. | 7 项 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用饱和食盐水和稀硫酸为原料制取HCl | |
| B. | 用大理石和稀硫酸制取CO2 | |
| C. | 用铁和盐酸为原料制取H2 | |
| D. | 用双氧水和二氧化锰为原料制取O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在粗盐提纯中,当加热到蒸发皿中有较多固体析出,残留少量液体时,停止加热,用余热将液体蒸干 | |
| B. | 当振荡分液漏斗中的混合溶液时,须用一只手压住分液漏斗的玻璃塞,另一只手握住旋塞,将分液漏斗倒转过来,用力振荡 | |
| C. | 粗盐提纯得到精盐的过程一定需要两次过滤操作 | |
| D. | 实验过程中若皮肤不慎沾上少量碱液,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉、漂粉精可用于饮用水及餐具等的消毒 | |
| B. | 福尔马林可用于食品的消毒,如浸泡海鲜,使其不易变质 | |
| C. | 药用酒精可用于食物及饮用水消毒 | |
| D. | 过氧乙酸无须稀释可直接使用消毒,不会对人体造成伤害 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

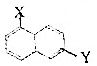 和
和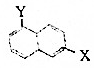
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量的烧碱溶液与二氧化碳的反应:OH-+CO2═HCO3- | |
| B. | 盐酸溶液与硝酸银溶液反应:HCl+Ag+═AgCl↓+H+ | |
| C. | 向Na2SiO3溶液中通入少量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| D. | 将稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用该溶液滴定未知浓度的NaOH溶液,用甲堪橙作指示剂 | |
| B. | 加水稀释时,$\frac{c(O{H}^{-})}{c({H}_{3}B{O}_{3})}$减小 | |
| C. | 常温下,加入等体积pH=9的NaOH溶液后,溶液呈中性 | |
| D. | 常温下,向该溶液滴加NaOH溶液至pH=7时,c(Na+)=c([B(OH)4]-)>c(H+)=c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com