
| A、②④⑤①③⑥ |
| B、⑤④②①③⑥ |
| C、⑤④②③①⑥ |
| D、②④⑤①③⑥ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
Ⅰ.取第一份溶液和适量稀盐酸加入下列装置的试管中,把澄清的石灰水加入烧杯中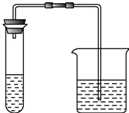 | 清的石灰水变浑浊 | 证明含有碳酸根离子 |
| Ⅱ.取第二份溶液,先别滴加 后加 | 证明含有硫酸根离子 | |
| Ⅲ.取第三份溶液加入过量BaCl2溶液,过滤,除去SO4-和CO32-,再滴加AgNO3溶液和稀硝酸 | 有 | 证明含有氯离子 |
| Ⅳ.取第四份溶液进行焰色反应 | 透过蓝色钴玻璃 火焰呈 | 证明含有K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若向原溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 |
| B、原溶液中一定不含有HCO3-或CO32- |
| C、原溶液中一定含有Ba2+、Al3+ |
| D、若向原溶液中加入足量的氢氧化钠溶液,充分反应后将沉淀过滤、洗涤、干燥并灼烧至恒重,得到固体的质量为12g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述实验无法确定是否含有Cl-和NO3- |
| B、溶液中肯定含有CO32-和SO42-,且浓度分别为4.00mol/L、2.00mol/L |
| C、上述实验确定溶液中肯定不含有Mg2+、Fe3+、Al3+ |
| D、要确定是否含有K+,应进一步做焰色反应实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
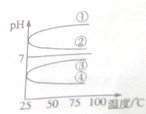 A、B、C、D、E五种溶液分别是NaOH、NH3?H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验:
A、B、C、D、E五种溶液分别是NaOH、NH3?H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验:| c(B) |
| c(OH-) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
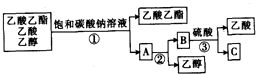
| A、①蒸馏 ②过滤 ③分液 |
| B、①分液 ②蒸馏 ③蒸馏 |
| C、①蒸馏 ②分液 ③分液 |
| D、①分液 ②蒸馏 ③结晶、过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com