
 .
.
 、
、 (写2种).
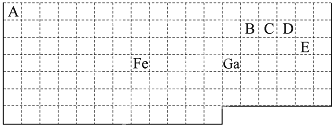
(写2种). 分析 上边界为短周期元素,一周期有2种元素,二、三周期有8种元素,表示元素周期表的部分边界如图: ;(1)、主族元素的族序数=其最外层电子数=其价电子数,最外层电子在排列时,遵循能量最低原理(先排能量低的后排能量高的),4s的能量小于4p的能量,4s能级最多排两个电子,4p能级最多排6个电子;
;(1)、主族元素的族序数=其最外层电子数=其价电子数,最外层电子在排列时,遵循能量最低原理(先排能量低的后排能量高的),4s的能量小于4p的能量,4s能级最多排两个电子,4p能级最多排6个电子;
(2)、元素周期表五区的划分是根据最后排入的电子名称命名的.Fe原子是26号元素,Fe原子的基态核外电子排布式为:1s22s22p63s23p63d64s2,这些电子排列时遵循能量最低原理(先排能量低的后排能量高的),这些能级的能量大小顺序为:1s<2s<2p<3s<3p<4s<3d,所以根据能量最低原理先排4s电子后排3d电子,根据等电子体的定义,只要原子数目和电子总数(或价电子总数)相同就是等电子体.CO分子含两个原子,且组成该物质的元素一个是6号一个是8号,找它的等电子体时,如果是分子,就把两种元素的原子序数一个增大1一个减小1,如果是离子,其中一种元素不变,另一种原子序数增大(或减小),带正电荷(或负电荷);
(3)、判断原子采取杂化方式时,先根据价层电子对互斥理论判断价层电子对,然后再确定采取的杂化方式,如:如果是直线型,采取的就是SP杂化;
(4)、分子空间构型的判断
价层电子对数=σ键电子对数+中心原子上的孤电子对数
σ键电子对数=σ键个数=中心原子结合的原子个数
中心原子上的孤电子对数=1/2(a-xb)
说明:对于分子,a为中心原子的价电子数
对于阳离子,a为中心原子的价电子数-离子所带的电荷数如:NH4+
对于阴离子,a为中心原子的价电子数+离子所带的电荷数如:CO3-
x为配位原子个数;b为配位原子最多能接受的电子数
如果价层电子对=2,VSEPR模型为直线型
如果价层电子对=3,VSEPR模型为平面三角形
如果价层电子对=4,VSEPR模型为四面体,由此分析.
解答 解:上边界为短周期元素,一周期有2种元素,二、三周期有8种元素,表示元素周期表的部分边界如图: ,故答案为:
,故答案为: ;
;
(1)、元素周期表每一横行是一个周期,一共有18个纵行,从左向右,1、2和13至17七个纵行是主族,且第一纵行开始分别为第IA族、第IIA族,第IIIA族、第IVA族,V第A族,V第IA族,第VIIA族,Ga是第四横行第十一纵行的元素,所以是第四周期第IIIA族的元素,主族元素的族序数=其最外层电子数=其价电子数,所以Ga最外层有3个电子,最外层电子在排列时,遵循能量最低原理(先排能量低的后排能量高的),4s的能量小于4p的能量,4s能级最多排两个电子,故答案为:4s24p1.
(2)、元素周期表五区的划分是根据最后排入的电子名称命名的.Fe原子是26号元素,Fe原子的基态核外电子排布式为:1s22s22p63s23p63d64s2,
这些电子排列时遵循能量最低原理(先排能量低的后排能量高的),这些能级的能量大小顺序为:1s<2s<2p<3s<3p<4s<3d,
根据能量最低原理先排4s电子后排3d电子,所以 最后排入的是3d电子,根据命名规则属d区,最外层有2个电子,根据等电子体的定义,CO的等电子体必须是双原子分子或离子,且电子总数相等.对于原子,原子序数=原子核外电子总数,所以,如果是分子,只要原子序数之和相等即可.
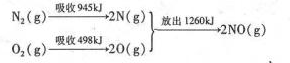
CO中C是6号元素,O是8号元素,原子序数之和为14,N是7号元素,且可形成双原子分子,所以分子是N2.
如果是阳离子离子,原子序数之和减去所带电荷数值,如果是阴离子,原子序数之和加上所带电荷数值,等于CO的原子序数之和即可所以是CN-..
故答案为:d区;2;N2、CN-.
(3)、判断原子采取杂化方式时,先根据价层电子对互斥理论判断价层电子对,然后再确定采取的杂化方式.价层电子对数=σ键电子对数+中心原子上的孤电子对数,σ键电子对数=σ键个数=中心原子结合的原子个数,中心原子上的孤电子对数=1/2(a-xb),说明:对于分子,a为中心原子的价电子数,x为配位原子个数,b为配位原子最多能接受的电子数
.在CH4中价层电子对数=σ键电子对数(4)+中心原子上的孤电子对数(0),所以碳原子采取sp3杂化.在CO分子中价层电子对数=σ键电子对数(1)+中心原子上的孤电子对数(1),所以碳原子采取sp杂化;CH2=CH2中,价层电子对数=σ键电子对数(3)+中心原子上的孤电子对数(0),所以碳原子采取sp2杂化.
故答案为:CH2=CH2、CH4;
(4)、根据元素周期表知,E是Cl元素,D是O元素,ED4-是ClO4-离子,价层电子对数=σ键电子对数+中心原子上的孤电子对数,σ键电子对数=σ键个数=中心原子结合的原子个数,中心原子是Cl原子,中心原子结合的原子个数是4,所以σ键电子对数=4,中心原子上的孤电子对数=1/2(a-xb),说明:x为配位原子个数,b为配位原子最多能接受的电子数,对于阴离子,a为中心原子的价电子数+离子所带的电荷数,中心原子上的孤电子对数=1/2(a-xb)=1/2(8-4*2)=0,所以价层电子对数=4,根据VSEPR理论预测ED4-离子的空间构型为正四面体型.
根据元素周期表知,B、C、D、E分别是C、N、O、Cl是四种元素,分子中每个原子最外层都达到8电子稳定结构的判断公式是:化合价的绝对值+原子最外层电子数=8,分子中每个原子最外层都达到8电子稳定结构.否则就没有达到8电子稳定结构.对于C元素,8-原子最外层电子数(4)=化合价的绝对值(4)
对于O元素,8-原子最外层电子数(6)=化合价的绝对值(2)
对于N元素,8-原子最外层电子数(5)=化合价的绝对值(3)
对于Cl元素,8-原子最外层电子数(7)=化合价的绝对值(1)
所以两两形成的化合物且每个原子最外层都达到8电子稳定结构的化合物有:CO2 CCl4,CO2 的电子式为: ; CCl4电子式为
; CCl4电子式为
故答案为:正四面体、 、
、
点评 本题考查基态原子或离子的核外电子排布或最外层电子排布、分子中原子采取的杂化方式、对于元素周期表,学习时要记住它的周期、族的划分,要熟记前36号元素,五区的划分、边界、划分依据等都要掌握,考查方式较多,在学习中要灵活掌握根据VSEPR理论预测分子或离子的空间构型是学习的重点,也是近几年高考的热点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 1<n<2 | B. | 1<n<5 | C. | 2<n<4 | D. | 2<n<5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以上反应均可发生 | B. | 只有①不能发生 | ||
| C. | 只有⑥不能发生 | D. | 只有②不能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Ca2+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol.L-1 | 2×10-6 | 6×10-6 | 2×10-5 | 4×10-6 | 3×10-5 | 2×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 沉淀完全的pH | 3.0 | 8.8 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式可能为C3H6O2 | |
| B. | 该物质不存在属于酯类的同分异构体 | |
| C. | 相对分子质量比乙酸大14n(n为整数) | |
| D. | 完全燃烧时生成CO2和H2O的质量比一定为11:9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com