
| A. | 在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 | |
| B. | 温度、压强一定时,放热的熵增加的反应一定能自发进行 | |
| C. | 反应焓变是决定反应是否自发进行的唯一因素 | |
| D. | 固体的溶解过程与熵变有关 |
分析 在一定的条件下,一个化学反应能否自发进行,既可能与反应的焓变有关,又可能与反应的熵变有关.在温度、压力一定的条件下,化学反应的方向是熵变和焓变共同影响的结果.温度、压强一定时,反应方向的判据是△G=△H-T△S,△G>0反应不能自发进行,△G<0反应能自发进行,△G=0达到平衡.
解答 解:A.在温度、压强一定的条件下,化学反应的方向是熵变和焓变共同影响的结果,故A正确;
B.放热反应△H<0,熵增加的反应,△S>0,△H-T△S一定小于0,反应一定能自发进行,故B正确;
C.化学反应的方向是熵变和焓变共同影响的结果,故C错误;
D.固体的溶解过程是熵值增加的过程,故D正确;
故选C.
点评 本题考查了化学反应能否自发进行的判断,题目比较简单,注意化学反应的方向是熵变和焓变共同影响的结果,根据公式判断.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 规律 | 推论 |
| A | 含Ag+离子的溶液中滴加稀盐酸会产生白色沉淀 | 滴加稀盐酸产生白色沉淀的溶液中一定含有Ag+离子 |
| B | 硫酸铝溶液中滴加过量氨水制取氢氧化铝沉淀 | 硫酸铝溶液中滴加过量NaOH溶液最终得不到氢氧化铝沉淀 |
| C | Fe(OH)3固体中滴加稀盐酸生成氯化铁和水 | Fe(OH)3固体中滴加HI生成碘化铁和水 |
| D | 铜片不溶于稀硫酸 | 铜片也不溶于稀硝酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液显电中性,胶体带有电荷,所以胶体较稳定 | |
| B. | 胶体粒子能透过滤纸,但不能透过半透膜,所以可用渗析的方法精制胶体 | |
| C. | 可用丁达尔效应区分溶液和胶体 | |
| D. | 电泳实验说明了胶体粒子能吸附溶液中的阳离子或阴离子而带有电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
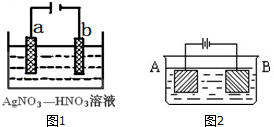 金属冶炼和处理常涉及电化学反应.
金属冶炼和处理常涉及电化学反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Na2SO4、Na2O以及Na2O2中,阳离子与阴离子的个数比均为2:1 | |
| B. | 实验桌上金属钠着火不能用常规灭火器灭火,可以选择用湿布盖灭 | |
| C. | 长距离运输鱼苗,最好在水中加入一定量的Na2O2,以起到供氧和杀菌的作用 | |
| D. | 金属钠和钾都保存在煤油中,所以金属锂(密度为0.534 g/cm3)也应该保存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | C-O | C═O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
| A. | 403 kJ•mol-1,-66 kJ•mol-1 | B. | 423 kJ•mol-1,+28 kJ•mol-1 | ||
| C. | 314 kJ•mol-1,-18 kJ•mol-1 | D. | 413 kJ•mol-1,-58 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com