
����Ŀ��SO2�Ǵ�����Ⱦ��֮һ��Ҳ����Ҫ�Ļ���ԭ�ϡ�
(1)ij�¶��£���Ӧ![]()
![]() �������仯��ͼ�����ݷ�Ӧ�Է����жϣ���Ӧ��______(�����������������������κ��¶���)�����¿������Է��ԣ��淴Ӧ�Ļ��Ϊ______��
�������仯��ͼ�����ݷ�Ӧ�Է����жϣ���Ӧ��______(�����������������������κ��¶���)�����¿������Է��ԣ��淴Ӧ�Ļ��Ϊ______��
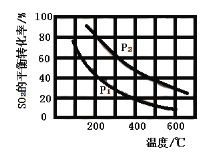
(2)��0.1 mol O2��0.2 mol SO2ͨ��һ�ݻ��ɱ�������н��з�Ӧ��![]() �����SO2��ƽ��ת�������¶ȡ�ѹǿ�ı仯��ͼ��
�����SO2��ƽ��ת�������¶ȡ�ѹǿ�ı仯��ͼ��
��![]() ______(������������������=��)
______(������������������=��)![]() ��
��
������300����ѹǿΪ![]() ʱ����Ӧ�ﵽƽ�⣬�����ݻ�ǡ��Ϊ10 L�����״̬�·�Ӧ��ƽ�ⳣ��K=____________��
ʱ����Ӧ�ﵽƽ�⣬�����ݻ�ǡ��Ϊ10 L�����״̬�·�Ӧ��ƽ�ⳣ��K=____________��
�۷�Ӧ![]() ��
��![]() ʱ�̴ﵽƽ�����
ʱ�̴ﵽƽ�����![]() ʱ�����ʷ�����ͼ��ʾ�仯���˿̿��ܸı�ķ�Ӧ����������______(����)��
ʱ�����ʷ�����ͼ��ʾ�仯���˿̿��ܸı�ķ�Ӧ����������______(����)��
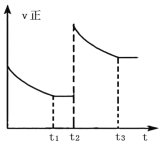
A.��ѹB.����ϵ����ͨ��һ����SO2
C.�����¶�D.�Ӵ���
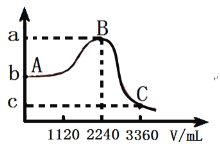
(3)�����£���1L![]() ��ˮ��Һ�л���ͨ��SO2����(������Һ����ı仯)������Һ��pH��ͨ��SO2��������(��״��)�Ĺ�ϵ��ͼ����
��ˮ��Һ�л���ͨ��SO2����(������Һ����ı仯)������Һ��pH��ͨ��SO2��������(��״��)�Ĺ�ϵ��ͼ����![]() _____��
_____��![]() _____��
_____��![]() _____����֪�������£��������
_____����֪�������£��������![]() ��
��![]() ���������
���������![]() ��
��![]() ��
��![]() ��
��
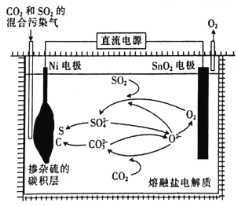
(4)�õ�ⷨ����CO2��SO2�Ļ����Ⱦ����ԭ����ͼ��ʾ�������Ϊ����̼���κ������Σ�ͨ��һ��ʱ���Ni�缫�����γɲ������̼���㣬����Ni�缫�������ǵ�Դ��______(��������������������)�������ĵ缫��ӦʽΪ________________________��
���𰸡����� ![]() ��
�� ![]() AB 7 3.8 1.6 ����
AB 7 3.8 1.6 ���� ![]()
��������
(1)���ݷ�Ӧ���ص��Լ���Ӧ���Է����е�����![]() ���з�������Ӧ��
���з�������Ӧ��![]() ��
��
(2)�ٸ���ѹǿ��ƽ���ƶ���Ӱ�������
���г�����ʽ����ƽ�ⳣ����
�۸���������ضԷ�Ӧ���ʺͻ�ѧƽ���Ӱ�������
(3)��ϻ�ѧ��Ӧ�Լ�����ĵ���ƽ�ⳣ�����м��㣻
(4)���ݵ��ԭ�����з�����
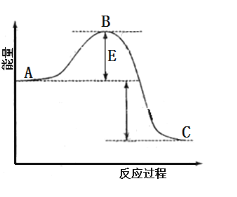
(1)��Ӧ![]() Ϊ�������ʵ�����С�ķ�Ӧ���ɸ÷�Ӧ�������仯ͼ��֪��
Ϊ�������ʵ�����С�ķ�Ӧ���ɸ÷�Ӧ�������仯ͼ��֪��![]() ��
��![]() ������Ӧ���Է����У���
������Ӧ���Է����У���![]() ���ʸ÷�Ӧ�ڵ��������¿������Է��ԣ���ͼ��֪�÷�Ӧ������Ӧ�Ļ��ΪE����
���ʸ÷�Ӧ�ڵ��������¿������Է��ԣ���ͼ��֪�÷�Ӧ������Ӧ�Ļ��ΪE����![]() �����淴Ӧ�Ļ��
�����淴Ӧ�Ļ��![]() ��
��
(2)�ٸ÷�Ӧ������ӦΪ�������ʵ�����С�ķ�Ӧ�����¶�һ��ʱ����ѹƽ�������ƶ���SO2��ƽ��ת��������![]() ��
��![]() ��
��
���¶�Ϊ300����ѹǿΪ![]() ʱ����Ӧ�ﵽƽ�⣬SO2��ƽ��ת����Ϊ60%�������ݻ�ǡ��Ϊ10 L�����г�����ʽ(��λΪmol)��
ʱ����Ӧ�ﵽƽ�⣬SO2��ƽ��ת����Ϊ60%�������ݻ�ǡ��Ϊ10 L�����г�����ʽ(��λΪmol)��
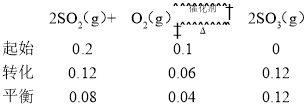 ��
��
��ʱc(SO2)=0.008mol/L��c(O2)=0.004mol/L��c(SO3)=0.012mol/L�����״̬�·�Ӧ��ƽ�ⳣ��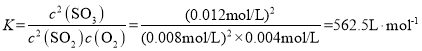 ��
��
��A. ��ѹ˲�䣬�����淴Ӧ���ʾ�������ƽ�������ƶ���������Ӧ���ʴ����淴Ӧ���ʣ��淴Ӧ���У�����Ӧ������С���淴Ӧ����������A���ϣ�
B. ����ϵ����ͨ��һ����SO2������Ӧ����˲�������淴Ӧ���ʲ��䣬�淴Ӧ���У�����Ӧ������С���淴Ӧ����������B���ϣ�
C. �����¶�˲�䣬�����淴Ӧ���ʾ�������ƽ�������ƶ������淴Ӧ���ʴ�������Ӧ���ʣ��淴Ӧ���У�����Ӧ�����������淴Ӧ������С����C�����ϣ�
D. �Ӵ��������淴Ӧ����ͬ�ȳ̶�����ƽ�ⲻ�ƶ����淴Ӧ���У����ʲ��ٱ仯����D�����ϣ�
��ѡAB��
(3)�����£���1L ![]() ��ˮ��Һ�л���ͨ��SO2����(������Һ����ı仯)���ᷢ����Ӧ
��ˮ��Һ�л���ͨ��SO2����(������Һ����ı仯)���ᷢ����Ӧ![]() ������Һ��������������pH����������ǡ�÷�Ӧ����Һ��Ϊ��������Һ����������ǿ��pH����С����SO2ͨ��2240mLʱ������ǡ�÷�Ӧ�������ʳ�������ʱ��ҺpH=7����a=7�����ĵ�n(SO2)=0.1mol����n(H2S)=0.2mol��δͨ��SO2ʱ����Һ����ҪΪ������ĵ�һ������
������Һ��������������pH����������ǡ�÷�Ӧ����Һ��Ϊ��������Һ����������ǿ��pH����С����SO2ͨ��2240mLʱ������ǡ�÷�Ӧ�������ʳ�������ʱ��ҺpH=7����a=7�����ĵ�n(SO2)=0.1mol����n(H2S)=0.2mol��δͨ��SO2ʱ����Һ����ҪΪ������ĵ�һ������![]() ��
��![]() ��
��![]() ����
����![]() ����
����![]() ����b=3.8���ټ���ͨ��SO21120mL��3360mL-2240mL=1120mL������0.05molʱ��SO2��ˮ��Ӧ���������ᣬ��Һ���������Ũ��Ϊ0.05mol/L��������ĵ�����������ĵ������ƣ���ͬ����֪��
����b=3.8���ټ���ͨ��SO21120mL��3360mL-2240mL=1120mL������0.05molʱ��SO2��ˮ��Ӧ���������ᣬ��Һ���������Ũ��Ϊ0.05mol/L��������ĵ�����������ĵ������ƣ���ͬ����֪��![]() ��
��![]() ����
����![]() ����c=1.6��
����c=1.6��
(4)��ͼʾ��֪����SnO2�缫�ϣ�O2-ʧ����������������õ缫Ϊ�������������ĵ缫��ӦʽΪ![]() ����һ��Ni�缫Ϊ����������������Ӧ����ӵ�Դ�ĸ���������
����һ��Ni�缫Ϊ����������������Ӧ����ӵ�Դ�ĸ���������


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ء����������д������
A.������ɱ������״�������á�84������Һ
B.ʳƷ�еĿ�����������ά����C
C.�����������CaCO3��Ca(OH)2
D.��ȥ��ҵ��ˮ�е�Cu2+����FeS
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����������������Һ�еķ�Ӧ������ͬһ���ӷ���ʽ��ʾ��( )
A.�������������������ͭ������
B.BaCl2��Һ��Na2SO4��Һ��Ba(OH)2��Һ��H2SO4��Һ
C.Na2CO3��Һ��������Һ��CaCO3��Һ��������Һ
D.ʯ��ʯ�����ᷴӦ��ʯ��ʯ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ�������·�Ӧ���Ȼ�ѧ����ʽ���£�
��Br2(g)+H2(g)2HBr(g) ��H=-Q1kJ��mol-1
��Br2(l)+H2(g)2HBr(g) ��H =-Q2kJ��mol-1
����˵����ȷ����
A.Q1<Q2
B.1molHBr(g)�����������1molHBr(l)�������
C.��ͬ�����£�Cl2(g)+H2(g)2HCl(g) ��H >-Q1kJ��mol-1
D.��1molBr2(g)�м���1molH2(g)�ڸ������³�ַ�Ӧ���ų�Q1kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pc����pH����ָϡ��Һ�����ӵ����ʵ���Ũ�ȵĸ�����������Һ��ij���ӵ����ʵ���Ũ��Ϊ![]() �������Һ�����ӵ�pc=2������������ȷ����( )
�������Һ�����ӵ�pc=2������������ȷ����( )
A.��0.01mol��L-1������ζ�ijŨ�ȵ�NaOH��Һ����Һ��pH������
B.��0.01mol��L-1��CaCl2��Һ����μ��봿����Һ���μӹ�����pc(Ca2+)��С
C.0.01mol��L-1��Na2CO3��Һ�У�pc(Na+)=2pc(CO![]() )
)
D.�����£���ˮ��pc(H+)+pc(OH��)=14
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ���л����������ҽ���һ�ֽṹ����
A.�����ϩ![]()
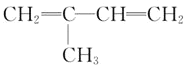
![]() ������ʵ�����
������ʵ�����![]() �����ӳɷ�Ӧ
�����ӳɷ�Ӧ
B.2���ȶ���(CH3CHClCH2CH3)��NaOH�Ҵ���Һ���ȷ�����ȥHCl�ķ�Ӧ
C.�ױ���һ�������·�����������һ�����ױ��ķ�Ӧ
D.���ǻ���������NaHCO3��Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���G�Ľṹ��ʽΪ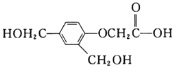 �����й����л���G��˵���������
�����й����л���G��˵���������
A.����ʽΪC10H12O5
B.1 mol G�������Ľ����Ʒ�Ӧ������H2�����Ϊ33.6 L
C.��һ�������£�1 mol G��������H2��Ӧ���������3 mol H2
D.�ɷ���ȡ����Ӧ���ӳɷ�Ӧ��������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ŷ�������Դ����ҽ���䷽����ϣ����¹ڷ��ײ�����Ⱦ�����͡���ͨ�͵����ƾ������õ�Ч�������е�һζ��ҩ���ˣ�����Ч�ɷֻ����յĽṹ��ʽ����ͼ��ʾ�������йػ����յ�˵������ȷ����( )
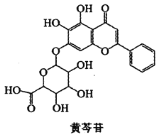
A.���ڷ����廯�������ʽΪ![]()
B.�����б����ϵ�һ�ȴ�����4��
C.�ɷ���ȡ����Ӧ���ӳɷ�Ӧ�����ܷ���������Ӧ
D.������![]() �����ӳɷ�Ӧ�������������1��
�����ӳɷ�Ӧ�������������1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ĸ���Ӧ�У���Ӧ����������������ͬ����
A.CH3CH2OH��CH3COOH![]() CH3COOCH2CH3��H2O
CH3COOCH2CH3��H2O
B.CH3CH2Br��NaOH![]() CH3CH2OH��NaBr
CH3CH2OH��NaBr
C.C6H5OH��3Br2 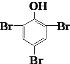 ��3HBr
��3HBr
D.2CH3CH2OH��O2![]() 2CH3CHO��2H2O
2CH3CHO��2H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com