
亚氯酸钠(![]() )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
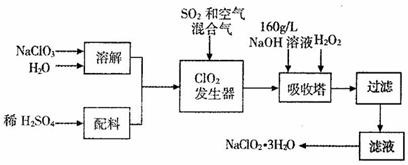
已知:
①![]() 的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O;
的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O;
②纯![]() 易分解爆炸,一般用稀有气体或空气稀释到10%以下。
易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(1)发生器中鼓入空气的作用可能是________________________________;
(2)吸收塔内发生反应的化学方程式为______________________________;吸收塔内的温度不能超过![]() ,其目的是防止
,其目的是防止![]() 分解,写出
分解,写出![]() 分解的化学方程式____________________________________;
分解的化学方程式____________________________________;
(3)在碱性溶液中![]() 比较稳定,所以吸收塔中应维持
比较稳定,所以吸收塔中应维持![]() 稍过量,判断
稍过量,判断![]() 是否过量的简单实验方法是_________________________________;
是否过量的简单实验方法是_________________________________;
(4)从滤液中得到NaClO2?3H2O粗晶体的实验操作依次是____________
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:填空题
工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下:
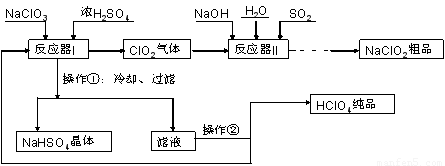
(1)实验室进行过滤操作的常用玻璃仪器有???????????? 。
(2)反应器I中的温度最佳为???????? (填序号);操作②的名称为????????? 。
A. 0°C ;????????? B. 20°C ;??????? C. 80°C ;????????? D. 120°C??
(3)反应器II中发生反应的离子方程式为?????????????? 。
(4)加快反应器II中反应速率的措施有?????????????? (写出一种措施即可)等。从反应器II中获得NaClO2?? 粗品的实验操作依次是???????? (填序号,下同),进一步提纯的操作名称为???????? 。
A.过滤? B.重结晶? C.蒸馏? D.蒸发浓缩? E.蒸干灼烧? F.冷却结晶? G.萃取分液
(5)上述流程中可循环使用的物质为???????? ,副产品除NaClO2、NaHSO4外还有???????? (填化学式)。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年辽宁省高三上学期期中考试理综化学试卷(解析版) 题型:填空题
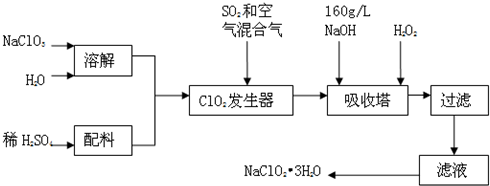
亚氯酸钠(NaC1O2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖,油脂的漂白与杀菌.以下是过氧化氢法生产亚氯酸钠的工艺流程图:
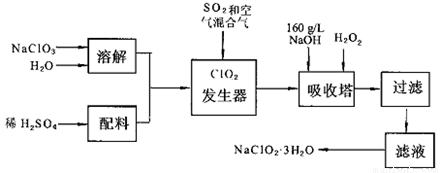
已知:①NaC1O2的溶解度随温度升高而增大,适当条件下可结晶析出NaC1O2·3H2O.
②纯C1O2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全.
I.请根据上述流程回答下列问题
(1)发生器中鼓入空气的作用可能是
(2)吸收塔内的反应的化学方程式为 . 吸收塔的温度不能超过20℃,其目的是 .
(3)在碱性溶液中NaC1O2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 .
(4)从滤液中得到NaC1O2·3H2O粗晶体的实验操作依次是 .
II.上述流程中的原料NaC1O3可由氯气通入热的烧碱溶液后重结晶就得到比较纯净的产品,所以通常工厂联合氯碱车间制备.
(1)氯碱工业中的原料为 ,原料需要净化的原因是 ,阳极产品为
(2)工业生产NaC1O3的化学方程式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com