
| A、X2和Y2 |
| B、YX2和Y2 |
| C、X2和XY |
| D、XY和Y2 |


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
| A、CO、NO、NaH、N2 |
| B、SO2、NO2+、N3-、OCN- |
| C、CO32-、NO3-、BCl3 |
| D、SiF4、SiO44-、SO32-、PO43- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol |
| B、0.3 mol |
| C、0.5 mol |
| D、0.15 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L酒精所含分子数为0.5NA |
| B、1L 0.3mol?L-1Na2SO4溶液中,含有Na+和SO42-总数为0.9NA |
| C、1 L NaCl溶液中,所含离子总数为2 NA |
| D、标准状况下,22.4L氢气含有NA个氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化亚铁溶中通入氯气:Fe2++Cl2=Fe3++2Cl- |
| B、硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| C、氧化铜溶于硫酸:O2-+2H+=H2O |
| D、碳酸钙溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | ① | ② | ③ | ④ |
| 备选装置 |  品红溶液 品红溶液 | 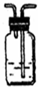 溴水 溴水 |  澄清石灰水 澄清石灰水 | 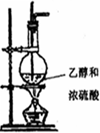 |
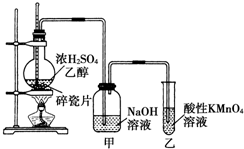
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com