
| A、KHCO3═K++H++CO32- |
| B、H2S═2H++S2- |
| C、KHSO4═K++H++SO42- |
| D、Ba(OH)2=Ba2++(OH)2- |


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
| A、大于6 | B、小于6 |
| C、等于6 | D、大于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
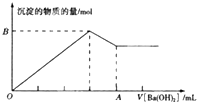 已知Ba[Al(OH)4]2可溶于水,图中表示的向100mL0.02mol.L-1KAl(SO4)2溶液中逐加入0.05mol.L-1Ba(OH)2溶液时(25℃),生成沉淀的物质的量与加入Ba(OH)2溶液的体积的关系.下列说法不正确的是( )
已知Ba[Al(OH)4]2可溶于水,图中表示的向100mL0.02mol.L-1KAl(SO4)2溶液中逐加入0.05mol.L-1Ba(OH)2溶液时(25℃),生成沉淀的物质的量与加入Ba(OH)2溶液的体积的关系.下列说法不正确的是( )| A、所价的Ba(OH)2溶液的c(OH-)=0.1mol.L- |
| B、A点的值是80mL |
| C、B点的值是0.005mol |
| D、当V[Ba(OH)2]时,生成沉淀的质量是0.699g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molFe2+与足量的H2O2溶液反应,转移2NA个电子 |
| B、46gNO2和N2O4混合气体中含有原子总数为3NA |
| C、1 mol Na 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
| D、1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、③④ | C、①③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
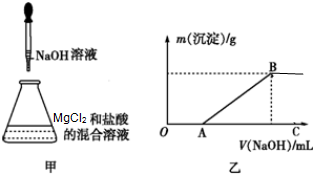 某同学称取一定量的MgCl2固体配成溶液,在该溶液中先加入一定量的稀盐酸,然后逐滴加入NaOH溶液(如图甲所示)
某同学称取一定量的MgCl2固体配成溶液,在该溶液中先加入一定量的稀盐酸,然后逐滴加入NaOH溶液(如图甲所示)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com