
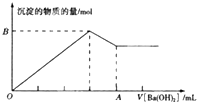
 已知Ba[Al(OH)4]2可溶于水,图中表示的向100mL0.02mol.L-1KAl(SO4)2溶液中逐加入0.05mol.L-1Ba(OH)2溶液时(25℃),生成沉淀的物质的量与加入Ba(OH)2溶液的体积的关系.下列说法不正确的是( )
已知Ba[Al(OH)4]2可溶于水,图中表示的向100mL0.02mol.L-1KAl(SO4)2溶液中逐加入0.05mol.L-1Ba(OH)2溶液时(25℃),生成沉淀的物质的量与加入Ba(OH)2溶液的体积的关系.下列说法不正确的是( )| A、所价的Ba(OH)2溶液的c(OH-)=0.1mol.L- |
| B、A点的值是80mL |
| C、B点的值是0.005mol |
| D、当V[Ba(OH)2]时,生成沉淀的质量是0.699g |


科目:高中化学 来源: 题型:
| A、HCl+Na2CO3;H2SO4+KHCO3 |
| B、BaCl2+Na2SO4;Ba(OH)2+(NH4)2SO4 |
| C、Fe+H2SO4(稀);Fe+CH3COOH(稀) |
| D、NaHCO3(过量)+Ca(OH)2;Ca(HCO3)2+NaOH(过量) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性:HF>HCl>HBr>HI |
| B、微粒半径:K+>Na+>Mg2+>Al3+ |
| C、酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
| D、沸点:HF>HCl>HBr>HI |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④ | B、①②③ |
| C、①②③④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H2SO4(浓),△ |
| 或Al2O3,△ |
| Br2 |
| 溶剂CCl4 |
| A、CH3CH2CHBrCH2Br |
| B、CH3CH(CH2Br)2 |
| C、CH3CHBrCHBrCH3 |
| D、(CH3)2CBrCH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KHCO3═K++H++CO32- |
| B、H2S═2H++S2- |
| C、KHSO4═K++H++SO42- |
| D、Ba(OH)2=Ba2++(OH)2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1:4.3×10-7 K2:5.6×10-11 |
| A、pH相同的三种溶液物质的量浓度关系:c(Na2CO3)>c(NaCN)>c(CH3COONa) |
| B、a L 0.1mol?L-1CH3COOH与b L 0.1mol?L-1NaOH溶液混合后所得溶液中pH>7,则a一定小于或等于b |
| C、物质的量浓度和体积均相同的CH3COONa和NaOH两种溶液,已知前者溶液中离子数目为n1,后者溶液中离子数目为n2,则n1>n2 |
| D、物质的量浓度相同NaHCO3和Na2CO3的混合溶液中:2c(H+)-2c(OH-)=c(CO32-)-c(HCO3-)-c(H2CO3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com