
| A. | 熔点:HI<HBr | B. | 硬度:MgO>CaO | ||
| C. | 晶格能:NaCl<NaBr | D. | 熔沸点:CO2>NaCl |
分析 A.均为分子晶体,且不存在氢键,相对分子质量越大熔点越高;
B.离子键越强硬度越大,离子所带电荷越多、离子半径越小,离子键越强;
C.离子所带电荷越多、离子半径越小,晶格能越大;
D.CO2形成分子晶体,NaCl属于离子晶体.
解答 解:A.HI、HBr均为分子晶体,且不存在氢键,HF相对分子质量更大,分子间作用力更强,故HI的熔点更高,故A错误;
B.离子所带电荷相同,Mg2+离子半径小于Ca2+离子半径,MgO晶体中离子键更稳定,则硬度:MgO>CaO,故B正确;
C.离子所带电荷相同,Cl-离子半径小于Br-离子半径,则晶格能:NaCl>NaBr,故C错误;
D.CO2形成分子晶体,NaCl属于离子晶体,离子晶体熔沸点大于分子晶体,故熔沸点:CO2<NaCl,故D错误,
故选:B.
点评 本题考查熔沸点高低比较、晶格能、晶体类型与性质,关键是理解掌握晶体类型与熔沸点、硬度关系及判断方法,分子晶体熔沸点与分子间作用力和氢键有关.


科目:高中化学 来源: 题型:选择题
| A. | 在地壳中的含量:Al>Fe>Na | |
| B. | 均能与盐酸反应,但金属钠与盐酸的反应最剧烈 | |
| C. | 钠、铝均能从FeCl3溶液中置换出铁单质 | |
| D. | 钠、铝均能与NaOH溶液反应,但参加反应的物质种类前者少于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25.5g | B. | 39g | C. | 51g | D. | 106.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6与C3H8没有同分异构体,CH2O2与C2H4O2属于同系物 | |
| B. | 一定条件下,乙酸乙酯、淀粉、蛋白质、乙烯都能与水发生水解反应 | |
| C. | 一定条件下,完全燃烧14g含氧质量分数为a的乙烯、乙醛混合气体,则生成水的质量为18(1-a)g | |
| D. | 全降解塑料(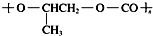 )可由单体环氧丙烷( )可由单体环氧丙烷(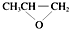 )和CO2缩聚制得 )和CO2缩聚制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学名称为乙醇 | B. | 易挥发 | ||
| C. | 常用作有机溶剂 | D. | 不能被酸性高锰酸钾氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5%蔗糖溶液 | B. | 75%乙醇溶液 | ||
| C. | 0.5mol/LNaCl溶液 | D. | 1mol/LNaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
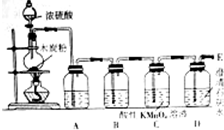 在100mL 18.4mol•L-1浓硫酸中加入1.2g木炭粉,加热使之充分反应.并按如图的装置图进行实验,依次检验反应得到的产物,请回答下列问题:
在100mL 18.4mol•L-1浓硫酸中加入1.2g木炭粉,加热使之充分反应.并按如图的装置图进行实验,依次检验反应得到的产物,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com