
化学实验有助于理解化学知识,提升科学素养。某学习小组在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关探究。
(1)已知发生装置如图所示。制备实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)
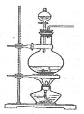
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸。
(2)该小组关于实验中可制得氯气体积(标准状况)的讨论正确的是
A.若提供0.4 mol HCl,MnO2不足量,则可制得氯气2.24 L
B.若提供0.4 mol HCl,MnO2过量,则可制得氯气2.24 L
C.若有0.4 mol HCl参与反应,则可制得氯气2.24 L
D.若有0.4 mol HCl被氧化,则可制得氯气2.24 L
(3)将Cl2通入水中,所得溶液中具有氧化性的含氯粒子有________ (填微粒符号)
(4)下列收集Cl2的正确装置是________。
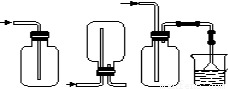
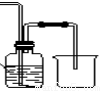
A B C D
(5)该小组利用刚吸收过少量SO2的NaOH溶液对Cl2进行尾气处理。
①请完成吸收初期的化学方程式:Cl2+Na2SO3+2 NaOH= ________________
②吸收一段时间后,某同学取出2mL吸收后的溶液(强碱性)于试管中,充分振荡后向其中滴加3~4滴淀粉-KI溶液,发现溶液先变蓝,随即又褪去。溶液先变蓝,说明吸收后的溶液中存在 (填微粒符号),用离子方程式表示蓝色褪去的可能原因: 。
(1)A C B (2)C (3)Cl2 、ClO- 、 HClO (4)C
(5)①2NaCl+Na2SO4+H2O ②ClO- ; I2+2OH-=I-+IO-+H2O
【解析】
试题分析:(1)在实验室制取Cl2时首先应该检查装置的气密性。然后再往烧瓶中加入MnO2粉末;接着往烧瓶中加入浓盐酸最后加热;顺序是A.C.B。发生反应为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。A.若提供0.4 mol HCl,MnO2不足量,应该以不足量的物质为标准,但是MnO2的量不定,因此产生的氯气在标准状况下的体积一定小于2.24 L。错误。 B.若提供0.4 mol HCl,MnO2过量,则可制得氯气2.24 L则如果0.4 mol HCl完全反应,可制得氯气2.24 L。但是随着反应的进行,盐酸变为稀盐酸,这时反应就不再发生。因此制得氯气在标准状况下的体积就小于2.24 L。错误。C.根据方程式可以看出:每有4mol的盐酸发生反应,产生标准状况下的氯气的体积为22.4L。因此若有0.4 mol HCl参与反应,则可制得氯气2.24 L。正确。D.由方程式可以看出:每有4mol的盐酸发生反应,则有2mol的盐酸贝氧化,得到氯气为1mol。因此若有0.4 mol HCl被氧化,则可制得标准状况下的氯气4.48 L.错误。(3)将Cl2通入水中,发生反应:Cl2+H2O
MnCl2+Cl2↑+2H2O。A.若提供0.4 mol HCl,MnO2不足量,应该以不足量的物质为标准,但是MnO2的量不定,因此产生的氯气在标准状况下的体积一定小于2.24 L。错误。 B.若提供0.4 mol HCl,MnO2过量,则可制得氯气2.24 L则如果0.4 mol HCl完全反应,可制得氯气2.24 L。但是随着反应的进行,盐酸变为稀盐酸,这时反应就不再发生。因此制得氯气在标准状况下的体积就小于2.24 L。错误。C.根据方程式可以看出:每有4mol的盐酸发生反应,产生标准状况下的氯气的体积为22.4L。因此若有0.4 mol HCl参与反应,则可制得氯气2.24 L。正确。D.由方程式可以看出:每有4mol的盐酸发生反应,则有2mol的盐酸贝氧化,得到氯气为1mol。因此若有0.4 mol HCl被氧化,则可制得标准状况下的氯气4.48 L.错误。(3)将Cl2通入水中,发生反应:Cl2+H2O H++Cl-+HClO。HClO是弱酸,在溶液中存在电离平衡:HClO
H++Cl-+HClO。HClO是弱酸,在溶液中存在电离平衡:HClO H++ClO-.在所得溶液中具有氧化性的含氯粒子有Cl2 、ClO-、HClO。(4)A只有入气管,而没有出气管。错误。B.Cl2的密度比空气大,要用向上排空气法收集。错误。C.是用用向上排空气法收集,由于Cl2是大气污染物,所以在排放之前进行了尾气的吸收和处理。正确。D不能收集气体。氯气被处理吸收。错误。选项为C。(5)①Cl2有氧化性,Na2SO3有还原性,二者发生反应的化学方程式:Cl2+Na2SO3+2 NaOH=2NaCl+Na2SO4+H2O。②吸收一段时间后,向其中滴加3~4滴淀粉-KI溶液,发现溶液先变蓝,是因为溶液中发生了反应:Cl2+2OH-=Cl-+ClO-+H2O。ClO-有强氧化性,能把I-氧化为I2。I2遇淀粉变为蓝色。随即又褪去,是因为又发生了反应:I2+2OH-=I-+IO-+H2O。
H++ClO-.在所得溶液中具有氧化性的含氯粒子有Cl2 、ClO-、HClO。(4)A只有入气管,而没有出气管。错误。B.Cl2的密度比空气大,要用向上排空气法收集。错误。C.是用用向上排空气法收集,由于Cl2是大气污染物,所以在排放之前进行了尾气的吸收和处理。正确。D不能收集气体。氯气被处理吸收。错误。选项为C。(5)①Cl2有氧化性,Na2SO3有还原性,二者发生反应的化学方程式:Cl2+Na2SO3+2 NaOH=2NaCl+Na2SO4+H2O。②吸收一段时间后,向其中滴加3~4滴淀粉-KI溶液,发现溶液先变蓝,是因为溶液中发生了反应:Cl2+2OH-=Cl-+ClO-+H2O。ClO-有强氧化性,能把I-氧化为I2。I2遇淀粉变为蓝色。随即又褪去,是因为又发生了反应:I2+2OH-=I-+IO-+H2O。
考点:考查Cl2的实验室制取原理、步骤、性质现象、化学方程式、离子方程式的书写及相应的计算的知识。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源:2016届江苏省淮安市协作体高一下学期期中考试化学试卷(解析版) 题型:选择题
下列属于物理变化的是
A.氯气溶于水 B.食物变质 C.用四氯化碳萃取碘水中的碘 D.光合作用
查看答案和解析>>
科目:高中化学 来源:2016届江苏省无锡江阴市高一下学期期中考试化学试卷(解析版) 题型:选择题
已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的是
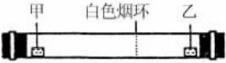
A.甲是浓氨水,乙是浓硫酸
B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸
D.甲是浓硝酸,乙是浓氨水
查看答案和解析>>
科目:高中化学 来源:2016届广东省东莞市四校高一下学期期中联考化学试卷(解析版) 题型:选择题
在一个2L的容器中,放入2mol气体A,5分钟后,测得这种气体A还剩余0.5mol,该反应中气体A的化学反应速率是:
A.1.5mol/(L·min) B.0.15mol/(L·min)
C.0.75mol/(L·min) D.0.075mol/(L·min)
查看答案和解析>>
科目:高中化学 来源:2016届广东省东莞市四校高一下学期期中联考化学试卷(解析版) 题型:选择题
下列微粒半径大小比较正确的是:
A.Na+<Mg2+<Al3+<O2- B.S2->Cl->Na+>Al3+
C.Na<Mg<Al<S D.Ca<Rb<K<Na
查看答案和解析>>
科目:高中化学 来源:2016届安徽师大附中高一下学期期中考查化学试卷(解析版) 题型:选择题
已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。
实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是

A.反应中氧化剂和还原剂的物质的量之比为2∶3
B.装置B中加入的物质可以是碱石灰或无水氯化钙
C.装置D中液体可以使干燥的红色石蕊试纸变蓝
D.为防止装置D中发生倒吸,可以改用向下排空气法收集氮气
查看答案和解析>>
科目:高中化学 来源:2016届安徽师大附中高一下学期期中考查化学试卷(解析版) 题型:选择题
某同学对一瓶Na2SO3固体样品进行如下实验:取出少量,加水完全溶解,滴入Ba(NO3)2
溶液,产生白色沉淀,再加入足量稀硝酸,仍有白色沉淀剩余。下述叙述正确的是
A.无法确定样品中钠、硫元素的质量比
B.Na2SO3已被氧化
C.加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4
D.加入稀硝酸后的沉淀一定是BaSO4
查看答案和解析>>
科目:高中化学 来源:2015河北保定某重点中学同步课时作业(必修1苏教版)4.1.2硫酸的性质和使用 题型:选择题
Zn与浓硫酸反应的化学方程式:Zn+2H2SO4(浓)====ZnSO4+SO2↑+2H2O。向100 mL 18 mol·L-1H2SO4溶液中加入足量的锌粒充分反应后,被还原的H2SO4的物质的量 ( )
A.等于1.8 mol B.小于0.9 mol
C.等于0.9 mol D.在0.9 mol和1.8 mol之间
查看答案和解析>>
科目:高中化学 来源:2015河北保定某重点中学同步作业(必修1苏教版)4.2.2氮肥的生产和使用 题型:选择题
除去NO2气体中的少量NH3,可以选用的试剂是 ( )
A.浓硫酸 B.NaOH溶液 C.稀硫酸 D.水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com