
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。
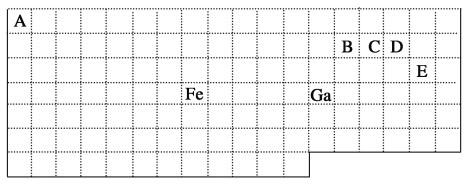
根据信息回答下列问题:
(1)周期表中基态Ga原子的最外层电子排布式为___________。
(2)Fe元素位于周期表的________分区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为_______。
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有________。
(4)根据VSEPR理论预测ED4-的空间构型为________。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子的分子式为_________(写2种)。
【答案】4s24p1 d 0 CH4、CH3OH 正四面体形 CO2、NCl3、CCl4、CO中任意两种
【解析】
根据元素在周期表的相对位置,可知A是H元素,B是C元素,C是N元素,D是O元素,E是Cl元素,然后根据元素周期表与元素原子结构、物质性质分析解答。
(1)31号Ga元素在元素周期表中位于第四周期第IIIA族,其核外最外层电子排布式是4s24p1;
(2)Fe是26号元素,原子核外电子排布式是1s22s22p63s23p63d64s2,Fe元素位于周期表第四周期第VIII族,属于d区元素;Fe与CO易形成配合物Fe(CO)5,由于配位体CO是中性分子,因此根据化合物中元素化合价代数和等于0可知:在配位化合物Fe(CO)5中铁的化合价为0价;
(3)在CH4、CO、CH3OH中,CH4、CH3OH中的碳原子都形成4个共价键,C采取sp3杂化;而CO中C原子与O原子形成共价三键,结构式是C≡O,因此C原子采用sp杂化;
(4)E为Cl,D为O,则ED4-离子为ClO4-,根据VSEPR理论,中心Cl原子的配位原子数BP=4,孤电子对数为LP=![]() =0,则价电子对数为VP=BP+LP=4+0=4,因此其空间构型为正四面体;
=0,则价电子对数为VP=BP+LP=4+0=4,因此其空间构型为正四面体;
B为C,C为N,则B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的化学式为CO2、NCl3、CCl4、CO。


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】与化学平衡类似,电离平衡的平衡常数叫作电离平衡常数(用K表示)。下表是某温度下几种常见弱酸的电离平衡常数:
酸 | 电离方程式 | 电离平衡常数 |
CH3COOH | CH3COOH | K=1.96×10-5 |
HClO | HClO | K=3.0×10-8 |
H2CO3 | H2CO3 HCO3- | K1=4.4×10-7 K2=5.6×10-11 |
H3PO4 | H3PO4 H2PO4- HPO42- | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
回答下列问题:
(1)若把CH3COOH、HClO、H2CO3、HCO3-、H3PO4、H2PO4-、HPO42-都看作是酸,则它们酸性最强的是___(填化学式,下同),最弱的是___。
(2)向NaClO溶液中通入少量的二氧化碳,发生反应的离子方程式为___。
(3)求出该温度下,0.10mol·L-1的CH3COOH溶液中的c(H+)=____mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为某机物与对应试剂的反应现象或是否反应,则这种有机物可能是( )
试剂 | 钠 | 溴水 | NaHCO3溶液 |
现象 | 放出气体 | 褪色 | 放出气体 |
A.CH2=CH-CH2-OH
B.![]()
C.CH2=CH-COOH
D.CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,向50.00mL未知浓度的氨水中逐滴加入0.5mol·L-1的HC1溶液。滴定过程中,溶液的pOH[pOH=-lgc(OH-)]与滴入HCl溶液体积的关系如图所示,则下列说法中正确的是
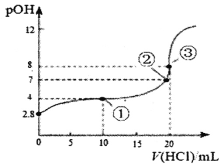
A. 图中②点所示溶液的导电能力弱于①点
B. ③点处水电离出的c(H+)=1×10-8mol·L-1
C. 图中点①所示溶液中,c(C1-)>c(NH4+)>c(OH-)>c(H+)
D. 25℃时氨水的Kb约为5×10-5.6mo1·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是常用的还原剂。在一定体积的某维生素C(化学式C6H8O6)溶液中加入a mol·L-1I2溶液V1 mL,使维生素C完全氧化,充分反应后,用Na2S2O3溶液滴定剩余的I2,消耗b mol·L-1 Na2S2O3溶液V2 mL。
已知发生的反应为:C6H8O6+I2=C6H6O6+2H++2I- , 2S2O32-+I2=S4O62-+2I-
该溶液中维生素C的物质的量是多少mol?(写出简要的计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化氢![]() 是一种有大蒜气味的、无色剧毒的强还原性气体,易在空气中自燃,一般在稀释状态下使用能降低风险。某科研小组拟用水解法制备并冷凝收集部分干燥的
是一种有大蒜气味的、无色剧毒的强还原性气体,易在空气中自燃,一般在稀释状态下使用能降低风险。某科研小组拟用水解法制备并冷凝收集部分干燥的![]() ,再利用未液化的余气继续探究其热分解情况。实验装置图及编号如下
,再利用未液化的余气继续探究其热分解情况。实验装置图及编号如下![]() 导管和部分夹持装置省略
导管和部分夹持装置省略![]() ,其中装置D是鼓泡器,用于监测
,其中装置D是鼓泡器,用于监测![]() 的流速。
的流速。
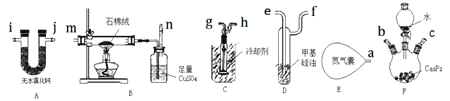
(1)写出![]() 水解法制备
水解法制备![]() 的化学反应方程式________。由于
的化学反应方程式________。由于![]() 水解反应太剧烈,为了减缓反应速率实验室可用________代替水。
水解反应太剧烈,为了减缓反应速率实验室可用________代替水。
(2)实验装置接口的正确连接顺序为![]() ________
________![]() 。
。
(3)![]() 中盛装石棉绒的仪器名称是________;装置E中装有足量的
中盛装石棉绒的仪器名称是________;装置E中装有足量的![]() ,实验中需持续通入后续装置,其作用主要有________
,实验中需持续通入后续装置,其作用主要有________![]() 答两点即可
答两点即可![]() 。
。
(4)![]() 中反应一段时间后,出现白色蜡状固体,经检验为白磷
中反应一段时间后,出现白色蜡状固体,经检验为白磷![]() 。写出该反应的化学方程式________。
。写出该反应的化学方程式________。
(5)在![]() 溶液吸收未反应的
溶液吸收未反应的![]() 气体过程中,产生
气体过程中,产生![]() 和两种常见的最高价含氧酸,反应化学方程式为________;已知
和两种常见的最高价含氧酸,反应化学方程式为________;已知![]() 足量时,
足量时,![]() 可继续被还原生成Cu单质。该小组为了测定此次制备
可继续被还原生成Cu单质。该小组为了测定此次制备![]() 的体积分数,收集到A装置出口的气体体积为
的体积分数,收集到A装置出口的气体体积为![]() 已折算为标准状况
已折算为标准状况![]() ,刚好被
,刚好被![]() 的
的![]() 溶液完全吸收,经过滤、洗涤、干燥后,得到
溶液完全吸收,经过滤、洗涤、干燥后,得到![]() 单质,则
单质,则![]() 的体积分数为________。
的体积分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物P的结构简式为![]() 。下列关于该有机物的说法不正确的是( )
。下列关于该有机物的说法不正确的是( )
A.向有机物P中直接加入银氨溶液,并水浴加热可以发生银镜反应
B.有机物P中以使溴的四氯化碳溶液退色
C.有机物P可以发生中成、水解、酯化、中和、氧化取代反应
D.1mol有机物P最多可以和2mol![]() 反应
反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA为阿伏加德罗常数的值,下列叙述不正确的是( )
A.22gN2O和22gCO2所含有的质子数均为11NA
B.18gH2O和18gD2O的中子数都为10NA
C.78gNa2O2中所含离子的数目为3NA
D.标准状况下,2.24LD2和H2的混合气体所含质子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用![]() 还原铁的氧化物并确定其组成的装置如图所示
还原铁的氧化物并确定其组成的装置如图所示![]() 粒中往往含有硫化物等杂质,焦性没食子酸溶液可吸收少量氧气
粒中往往含有硫化物等杂质,焦性没食子酸溶液可吸收少量氧气![]() 。
。
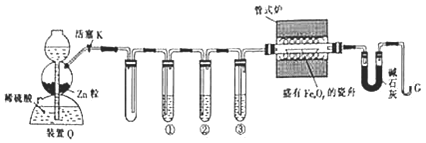
回答下列问题:
![]() 装置
装置![]() 启普发生器
启普发生器![]() 用于制备
用于制备![]() ,还可用于______
,还可用于______![]() 填字母,下同
填字母,下同![]() 。
。
A.生石灰与浓氨水制![]() B.过氧化钠与水制
B.过氧化钠与水制![]()
C.硫化铁固体与稀硝酸制![]() 大理石与稀盐酸制
大理石与稀盐酸制![]()
![]() 中依次盛装的试剂为______,
中依次盛装的试剂为______,![]() 酸性溶液中发生反应的离子方程式为______。
酸性溶液中发生反应的离子方程式为______。
A.![]() 酸性溶液、浓
酸性溶液、浓![]() 、焦性没食子酸溶液
、焦性没食子酸溶液
B.焦性没食子酸溶液、浓![]() 、
、![]() 酸性溶液
酸性溶液
C.![]() 酸性溶液、焦性没食子酸溶液、浓
酸性溶液、焦性没食子酸溶液、浓![]()
![]() “加热管式炉”和“打开活塞K”这两步操作应该先进行的是___,在这两步之间还应进行的操作是___。
“加热管式炉”和“打开活塞K”这两步操作应该先进行的是___,在这两步之间还应进行的操作是___。
![]() 反应过程中G管逸出的气体是______,其处理方法是______。
反应过程中G管逸出的气体是______,其处理方法是______。
![]() 结束反应时,应该______,待装置冷却后称量并记录相应数据。
结束反应时,应该______,待装置冷却后称量并记录相应数据。
![]() 假设反应完全后瓷舟中的固体只有Fe单质,实验中测得了下列数据:
假设反应完全后瓷舟中的固体只有Fe单质,实验中测得了下列数据:![]() 瓷舟的质量为
瓷舟的质量为![]() ;
;![]() 瓷舟和FexOy的总质量为
瓷舟和FexOy的总质量为![]() ;
;![]() 反应前U形曾及内盛物的总质量为
反应前U形曾及内盛物的总质量为![]() ;
;![]() 反应后U形管及内盛物的总质成为
反应后U形管及内盛物的总质成为![]() 。由以上数据计算并确定该铁的氧化物的化学式为______。
。由以上数据计算并确定该铁的氧化物的化学式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com