
在50 mL a mol·L-1的硝酸溶液中,加入6.4 g Cu,固体全部溶解,且还原产物只有NO2和NO。将反应后溶液用蒸馏水稀释至100 mL,测得c(NO3-)=4 mol·L-1。
(1)稀释后的溶液中c(H+)= mol·L-1
(2)若a=10,则生成的气体中NO2的物质的量为________mol
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
若上述混合气体被1 mol·L-1的NaOH溶液恰好吸收,则NaOH溶液的体积为________mL
(1)2 (2)0.05 (3)100
【解析】
试题分析:(1)在稀释后的溶液中含有Cu(NO3)2、HNO3。根据物料守恒可得n(NO3-)=2n(Cu2+)+n(H+).n(Cu2+)=6.4g÷64g/mol=0.1mol; n(NO3-)=4 mol/L×0.1L=0.4mol。所以n(H+)= 0.4mol-2×0.1mol=0.2mol.稀释后的溶液中c(H+)=n(H+)÷V=0.2mol÷0.1L=2mol/L。(2)若a=10,n(HNO3)(总)=0.05L×10mol/L=0.5molL; 根据n(HNO3)( 剩余)=0.2mol.则反应消耗的硝酸的物质的量为0.3mol.开始的硝酸为浓硝酸,发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。,随着反应的进行 硝酸变为稀硝酸,发生反应: 3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O假设产生的NO2、NO的物质的量分别为x、y.则根据方程式中Cu与硝酸的物质的量关系可得x/2+3y/2=0.1;2x+4y=0.3.解得x=0.05;y=0.05.因此生成的气体中NO2的物质的量为0.05mol。(3)由方程式可以看出n(NOx)=n(NaOH).n(NOx)=n(NO2)+n(NO)= 0.05+0.05=0.1mol。所以n(NaOH)=0.1mol.V(NaOH)=n÷C=0.1mol÷1mol/L=0.1L=100ml。
考点:考查守恒法在金属与硝酸反应的计算中的应用的知识。


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源:2016届江苏省淮安市协作体高一下学期期中考试化学试卷(解析版) 题型:选择题
人们用DNA制造出一种臂长只有7nm的纳米镊子,这种镊子能钳起分子或原子,并对它随意组合。下列分散系中,分散质微粒直径与纳米粒具有相同数量级的是
A.溶液 B.胶体 C.悬浊液 D.乳浊液
查看答案和解析>>
科目:高中化学 来源:2016届广东省东莞市四校高一下学期期中联考化学试卷(解析版) 题型:选择题
下列关于离子化合物的叙述正确的是:
A.离子化合物中都含有离子键
B.离子化合物中的阳离子只能是金属离子
C.离子化合物如能溶于水,其水溶液一定可以导电
D.溶于水可以导电的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源:2016届广东省东莞市四校高一下学期期中联考化学试卷(解析版) 题型:选择题
下列化合物中,同时含有离子键、极性共价键的是:
A.NaOH B.H2O2 C.HCl D.NaCl
查看答案和解析>>
科目:高中化学 来源:2016届安徽师大附中高一下学期期中考查化学试卷(解析版) 题型:选择题
某固体物质和某溶液在一定条件下反应,产生气体的相对分子质量(或平均相对分子质量)为45,则发生反应的物质不可能是
A.Zn和浓H2SO4 B.C和浓HNO3 C.Na2O2和NH4Cl浓溶液 D.Cu和浓HNO3
查看答案和解析>>
科目:高中化学 来源:2016届安徽师大附中高一下学期期中考查化学试卷(解析版) 题型:选择题
下列所用的酸在反应中同时表现酸性和氧化性的是
A.用浓盐酸与KMnO4反应制取Cl2
B.向蔗糖中加入浓H2SO4,固体变黑膨胀
C.用稀硫酸与CuO反应制取胆
D.用浓硝酸除去铝表面的铜镀层
查看答案和解析>>
科目:高中化学 来源:2015河北保定某重点中学同步课时作业(必修1苏教版)4.1.2硫酸的性质和使用 题型:实验题
下面是某同学在学习硫元素时的学习方案,请完善该同学的学习方案。
(1)硫原子的结构:硫原子的核内质子数为16,它的原子结构示意图是 ,从结构可以知道硫元素是一种典型的非金属元素。
(2)硫单质的物理性质:硫是一种淡黄色的 体(填“气”“液”或“固”),主要存在于火山喷发口附近或地壳的岩层里,这是硫以游离态形式存在于自然界中。硫元素在自然界中也有以化合态形式存在的,如许多金属矿石是含硫化合物,如胆矾 (填化学式)。
(3)设计如下实验探究硫和含硫化合物的相互转化:
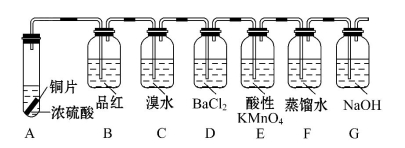
(Ⅰ)完成下列各个反应的化学方程式
①A中在加热时发生的反应
。
②C中的反应
。
(Ⅱ)记录观察到的实验现象
①B中品红溶液由红色变为 ,加热后又 ,(结论:可以根据该现象用品红溶液来证明SO2的存在与否)。
②D中没有观察到什么现象,在实验结束后往D中滴加H2O2后则可以看到 。
③E中溶液由紫红色变为无色,反应的离子方程式是
2Mn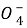 +5SO2+2H2O====2Mn2++5S
+5SO2+2H2O====2Mn2++5S +4H+
+4H+
反应中SO2是 剂(填“氧化”或“还原”)。
(Ⅲ)G的作用是吸收尾气,写出反应的离子方程式:
。
查看答案和解析>>
科目:高中化学 来源:2015河北保定某重点中学同步作业(必修1苏教版)4.2.2氮肥的生产和使用 题型:选择题
下列说法中正确的是 ( )
A.氨水和液氨不同,氨水是混合物,液氨是纯净物
B.氨保存于无色试剂瓶中
C.氨水不稳定,应保存于棕色瓶中
D.在反应NH3+H+====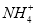 中,NH3发生氧化反应
中,NH3发生氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com