
下列所用的酸在反应中同时表现酸性和氧化性的是
A.用浓盐酸与KMnO4反应制取Cl2
B.向蔗糖中加入浓H2SO4,固体变黑膨胀
C.用稀硫酸与CuO反应制取胆
D.用浓硝酸除去铝表面的铜镀层
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:2016届江苏省沭阳县高一下学期期中调研测试化学试卷(解析版) 题型:选择题
一定条件下,可逆反应N2 + 3H2 2NH3达到化学平衡状态,下列说法一定正确的是
2NH3达到化学平衡状态,下列说法一定正确的是
A.每1 mol N≡N断裂的同时有2 mol N—H生成
B.N2、H2、NH3的浓度之比为1:3:2
C.N2减少的速率和NH3减少的速率之比为1:2
D.气体体积为初始体积的
查看答案和解析>>
科目:高中化学 来源:2016届广东省东莞市四校高一下学期期中联考化学试卷(解析版) 题型:填空题
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑
判断能否设计成原电池A. ,B. 。(填“能”或“不能”)
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是 。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲 乙(填“>”、“<“或“=” )
③请写出图中构成原电池的负极电极反应式 。
④当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为 。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入 极(填a或b,下同),电子从 极流出。
查看答案和解析>>
科目:高中化学 来源:2016届安徽师大附中高一下学期期中考查化学试卷(解析版) 题型:填空题
在50 mL a mol·L-1的硝酸溶液中,加入6.4 g Cu,固体全部溶解,且还原产物只有NO2和NO。将反应后溶液用蒸馏水稀释至100 mL,测得c(NO3-)=4 mol·L-1。
(1)稀释后的溶液中c(H+)= mol·L-1
(2)若a=10,则生成的气体中NO2的物质的量为________mol
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
若上述混合气体被1 mol·L-1的NaOH溶液恰好吸收,则NaOH溶液的体积为________mL
查看答案和解析>>
科目:高中化学 来源:2016届安徽师大附中高一下学期期中考查化学试卷(解析版) 题型:选择题
已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。
实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是

A.反应中氧化剂和还原剂的物质的量之比为2∶3
B.装置B中加入的物质可以是碱石灰或无水氯化钙
C.装置D中液体可以使干燥的红色石蕊试纸变蓝
D.为防止装置D中发生倒吸,可以改用向下排空气法收集氮气
查看答案和解析>>
科目:高中化学 来源:2016届安徽师大附中高一下学期期中考查化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.NO2通入AgNO3溶液中:3NO2+H2O=2NO3-+NO+2H+
B.过量的SO2通入NaOH溶液中:SO2+2OH-=SO32-+H2O
C.过量NaOH滴入NH4HCO3稀溶液中:NH4++OH-=NH3·H2O
D.铜片加入稀HNO3中:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源:2015河北保定某重点中学同步课时作业(必修1苏教版)4.1.2硫酸的性质和使用 题型:选择题
已知反应:①2H2S+O2====2S+2H2O;②2H2S+SO2====3S+2H2O;
③2H2S+3O2====2SO2+2H2O,将点燃的H2S气体的导管伸入盛有一定量O2的
集气瓶内,上述3个反应发生的先后顺序是 ( )
A.①②③ B.③①② C.①③② D.③②①
查看答案和解析>>
科目:高中化学 来源:2015河北保定某重点中学同步课时作业(必修1苏教版)3.1.1铝及铝合金 题型:选择题
实验室将9 g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为18 g,则该氧化物粉末可能是 ( )
A.Fe2O3和MnO2 B.MnO2和V2O5
C.Cr2O3和V2O5 D.Fe3O4和FeO
查看答案和解析>>
科目:高中化学 来源:2015河北保定某重点中学同步作业(必修1苏教版)4.1.1二氧化硫的性质和应用 题型:实验题
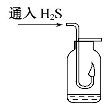
硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。

(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是
。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种: 。
(3)洗气瓶C溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量 (填“偏高”“偏低”或“无影响”)。
乙方案:实验步骤如以下流程图所示:
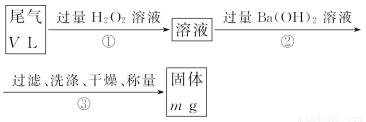
(4)写出步骤②中反应的化学方程式 。
(5)步骤③中洗涤沉淀的方法是 。
(6)通过的尾气体积为VL(已换算成标准状况)时,该尾气中二氧化硫含量(体积分数)为 (用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与乙方案相同。
(7)你认为丙方案是否合理,说明理由:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com