
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化镁、氢氧化钠 |
| B、硫酸钠、氢氧化钡 |
| C、氯化铝、氨水 |
| D、溴化亚铁、氯水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
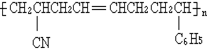 工程塑料ABS树脂(结构简式如图,式中-C6H5是苯基),合成它的单体有( )
工程塑料ABS树脂(结构简式如图,式中-C6H5是苯基),合成它的单体有( )| A、①③⑥ | B、②③⑤ |
| C、②④⑤ | D、②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3mol |
| B、11 mol |
| C、6 mol |
| D、5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、BAEDC |
| B、CDBAE |
| C、ABCDE |
| D、ECDBA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com