

���� ʵ��1����1������XΪԲ����ƿ��
��2���ζ�ǰ���ȼ��ζ����Ƿ�©ˮ���ٽ�����ϴ��Ȼ���ñ�Һ��ϴ����ע���Һ���ž��ζ���������ݲ�����Һ�棬��������¼���ζ�ǰ����ɣ�
��3�����������������Ƽ���Bװ����ʣ���HCl���μӷ�Ӧ��HCl���շֽ����ɵ�NH3��������Ӧ��NH3+HCl=
NH4Cl��������������NH3�����ʵ�����
ʵ��2����4��ȡD��Һ���Թ��У���������BaCl2��Һ���ټ������ᣬ��ɫ������ȫ�ܽ������ɴ̼�����ζ�����壬˵��D����Һ����SO32-����SO42-��
��5��װ��D����Һ����SO32-��˵���ֽ�����SO2��װ��A��D֮��ĵ���������������ɫ���壬��ɫ����Ӧ�Ƕ�����������ˮ�γɵ��Σ�װ��B����Һ���յ������ǰ�����
��6���ɣ�5���з�����֪����NH4��2SO4��400��ֽ�ʱ����NH3��SO2��H2O���ɣ�SԪ�ػ��ϼ۽��ͣ����ݵ���ת���غ㣬ֻ��ΪNԪ�ػ��ϼ����ߣ�����������������˵������N2����ƽ��д����ʽ��
��� �⣺��1��������X�Ľṹ��֪��XΪԲ����ƿ���ʴ�Ϊ��Բ����ƿ��
��2���ζ�ǰ���ȼ��ζ����Ƿ�©ˮ���ٽ�����ϴ��Ȼ���ñ�Һ��ϴ����ע���Һ���ž��ζ���������ݲ�����Һ�棬��������¼���ζ�ǰ����ɣ�����ȷ��˳��Ϊ��dbaec��
�ʴ�Ϊ��dbaec��
��3���ζ�ʣ�����ᣬ�յ�ʱ����NaOHΪ0.025L��0.2mol/L=0.005mol����ʣ��HClΪ0.005mol����μӷ�Ӧ��HClΪ0.07L��0.5mol/L-0.005mol=0.03mol���μӷ�Ӧ��HCl���շֽ����ɵ�NH3��������Ӧ��NH3+HCl=NH4Cl��������NH3�����ʵ���Ϊ0.03mol��
�ʴ�Ϊ��0.03��
��4�����װ��D����Һ����SO32-����SO42-��ʵ������������ǣ�ȡ����D��Һ���Թ��У���������BaCl2��Һ���а�ɫ�������ɣ��ټ������ᣬ��ɫ������ȫ�ܽ⣬���ɴ̼�����ζ�����壬˵��D����Һ����SO32-����SO42-��
�ʴ�Ϊ��ȡ����D��Һ���Թ��У���������BaCl2��Һ���а�ɫ�������ɣ��ټ������ᣬ��ɫ������ȫ�ܽ⣬���ɴ̼�����ζ�����壬˵��D����Һ����SO32-����SO42-��
��5��װ��D����Һ����SO32-��˵���ֽ�����SO2��װ��A��D֮��ĵ���������������ɫ���壬��ɫ����Ӧ�Ƕ�����������ˮ�γɵ��Σ�װ��B����Һ���յ������ǰ�����
�ʴ�Ϊ��NH3��
��6���ɣ�5���з�����֪����NH4��2SO4��400��ֽ�ʱ����NH3��SO2��H2O���ɣ�SԪ�ػ��ϼ۽��ͣ����ݵ���ת���غ㣬ֻ��ΪNԪ�ػ��ϼ����ߣ�����������������˵������N2���ֽⷴӦ����ʽΪ��3��NH4��2SO4$\frac{\underline{\;\;��\;\;}}{\;}$4NH3��+N2��+3SO2��+6H2O����
�ʴ�Ϊ��3��NH4��2SO4$\frac{\underline{\;\;��\;\;}}{\;}$4NH3��+N2��+3SO2��+6H2O����
���� ���⿼�黯ѧʵ�飬�漰��ѧ�������ζ�������ʵ�鷽����ơ���ѧ���㡢�����ƶϡ���ѧ����ʽ��д�ȣ��Ƕ�ѧ���ۺ������Ŀ��飬�ϺõĿ���ѧ����������������֪ʶǨ�����������Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ʯī�з��������ʯīϩ��������Ӳ�������������ʣ����Ƴɵ�������С�����ײ��ϣ���ṹ��ͼ��ʾ�����й���ʯīϩ��˵������ȷ���ǣ�������
��ʯī�з��������ʯīϩ��������Ӳ�������������ʣ����Ƴɵ�������С�����ײ��ϣ���ṹ��ͼ��ʾ�����й���ʯīϩ��˵������ȷ���ǣ�������| A�� | �������õĵ����Ժ����� | |
| B�� | ʯīϩ���������л�������۷е�ϸ� | |
| C�� | ʯīϩ�����ʯ��Ϊͬ�������� | |
| D�� | ��������ȼ�տ�������CO2��CO����ߵĻ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | W03��W�Ļ��ϼ���+3�� | |
| B�� | W03���ڷǽ��������� | |
| C�� | ������22.4L����ʱ���Եõ�$\frac{1}{3}$ mol W | |
| D�� | ����1.8gˮ����ʱ��ת��0.2 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ע��Һ���ܲ��������ЧӦ�������ڽ��� | |
| B�� | ��֬�Ǹ߷��ӻ�̨�ˮ������ɸ��ͺ�֬���� | |
| C�� | ú�к��е�ú���ͣ�����ú������ | |
| D�� | ����ϩ���ϵ��ϻ�����Ϊ�����˼ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 25��ʱ����Ũ��Ϊ0.1000mol•L-1��NaOH��Һ�ζ�20.00mLŨ�Ⱦ�Ϊ0.1000mol•L-1��������HX��HY��HZ�ζ�������ͼ��ʾ������˵����ȷ���ǣ�������
25��ʱ����Ũ��Ϊ0.1000mol•L-1��NaOH��Һ�ζ�20.00mLŨ�Ⱦ�Ϊ0.1000mol•L-1��������HX��HY��HZ�ζ�������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ���ݵζ����ߣ��ɵ�Ka��HY����10-9 | |
| B�� | ����ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳��HZ��HY��HX | |
| C�� | HY��HZ��ϣ��ﵽƽ��ʱ��c��H+��=$\frac{Ka��HY��•c��HY��}{c��{Y}^{-}��}$+c��Z-��+c��OH-�� | |
| D�� | ������HX��HY��Һ�������Ϻ���NaOH��Һ�ζ���HXǡ����ȫ��Ӧʱ��c��Na+����c��Y-����c��X-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
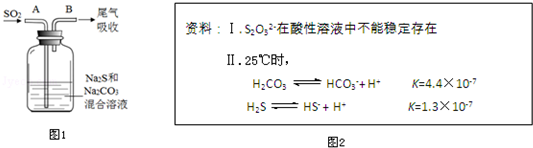
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ԭ������ | B�� | Ԫ������ | C�� | ԭ������ | D�� | ͬλ������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com