
 ���嶡������
���嶡������ ��ҵ��;�㷺�����������������Է�ȩ��֬���ȶ��������ϵȣ�ʵ�����Ա��ӡ��嶡����[��CH3��3CCl]��Ϊԭ���Ʊ����嶡�����ӣ�ʵ�鲽�����£���Ӧ��Ͳ������������б����£�
��ҵ��;�㷺�����������������Է�ȩ��֬���ȶ��������ϵȣ�ʵ�����Ա��ӡ��嶡����[��CH3��3CCl]��Ϊԭ���Ʊ����嶡�����ӣ�ʵ�鲽�����£���Ӧ��Ͳ������������б����£� ���÷�Ӧ���ڼ��ң��ų������ȣ���ʹʵ��IJ��ʽ��ͣ����ܵ�ԭ���������嶡���Ȼӷ����²��ʽ��ͣ�
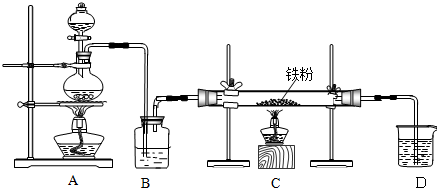
���÷�Ӧ���ڼ��ң��ų������ȣ���ʹʵ��IJ��ʽ��ͣ����ܵ�ԭ���������嶡���Ȼӷ����²��ʽ��ͣ����� ��1������ʵ��װ��ͼ��֪�������ƣ�
��2���÷�Ӧ�DZ��ӡ��嶡�������ɲ�Ʒ�ķ�Ӧ���ӽṹ�Ϸ���Ϊȡ����Ӧ���ݴ�д����ʽ����ӦΪ���ȷ�Ӧ���ᵼ���嶡���Ȼӷ���
��3����Ӧ���������ܽ���ˮ��HCl���ҷ�Ӧ�¶Ƚϸߣ����õ��۵�©����ֹ���������������ھƾ���
��4�������ж����۵�Ϳ�����ͨ�����ˮԡ�����ڻ�ΪҺ�壻
��5����������ʹ�ù�������ƿ���ζ��ܡ���Һ©����ʹ��ǰ�������©��
��6�����ݷ�Ӧ �ɼ�������嶡�����ӵ����۲������ٸ��ݲ���=$\frac{ʵ����}{������}$��100%���㣮
�ɼ�������嶡�����ӵ����۲������ٸ��ݲ���=$\frac{ʵ����}{������}$��100%���㣮
��� �⣺��1������ʵ��װ��ͼ��֪����XΪ�������ڣ���ƿ��BΪ�����ܣ�
�ʴ�Ϊ���������ڣ���ƿ��
��2���÷�Ӧ�DZ��ӡ��嶡�������ɲ�Ʒ�ķ�Ӧ���ӽṹ�Ϸ���Ϊȡ����Ӧ����Ӧ����ʽΪ ����ӦΪ���ȷ�Ӧ����ʹ�嶡���Ȼӷ����Ӷ����²����½���
����ӦΪ���ȷ�Ӧ����ʹ�嶡���Ȼӷ����Ӷ����²����½���
�ʴ�Ϊ�� �������嶡���Ȼӷ����²��ʽ��ͣ�
�������嶡���Ȼӷ����²��ʽ��ͣ�
��3����Ӧ���������ܽ���ˮ��HCl���ҷ�Ӧ�¶Ƚϸߣ����õ��۵�©����ֹ���������������ھƾ������Ա���մ��Ƥ���Ͽ��þƾ�ϴ�ӣ�
�ʴ�Ϊ����ֹ�������ƾ���
��4����ȡ�ñ���ʱ���ֱ��Ӷ������Լ�ƿ�У��ɲ�ȡ�Ĵ�ʩΪ��ͨ����ж��Լ�ƿ��ˮԡ��
�ʴ�Ϊ����ͨ����ж��Լ�ƿ��ˮԡ��
��5����������ʹ�ù�������ƿ���ζ��ܡ���Һ©����ʹ��ǰ�������©����ѡBCD��
��6�����ݷ�Ӧ��
94 150
1.6g x
x=$\frac{1.6��150}{94}$=2.55g��
����嶡�����ӵIJ���Ϊ$\frac{1.8g}{2.55g}$��100%=70.6%��
�ʴ�Ϊ��70.5%��
���� �����л���ĺϳ�Ϊ���壬���黯ѧʵ�飬��Ŀ�ۺ��Խϴ��漰��ʵ��ԭ�������⡢��װ�õķ������ۡ���ʵ��������ѡ����ơ�ʵ�鷽����ơ����ʷ����ᴿ����ѧ����ȣ��Ѷ��еȣ��Ƕ�ѧ���ۺ������Ŀ��飮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

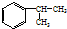 ��A�ĺ��б�����ͬ���칹�壨��A�⣩��7�֣����к˴Ź���������ʾΪ2��壬�ҷ������Ϊ3��1��ͬ���칹����
��A�ĺ��б�����ͬ���칹�壨��A�⣩��7�֣����к˴Ź���������ʾΪ2��壬�ҷ������Ϊ3��1��ͬ���칹���� ��д�ṹ��ʽ����
��д�ṹ��ʽ���� +nHCHO$��_{��}^{����}$
+nHCHO$��_{��}^{����}$ +nH2O��
+nH2O�� G��
G�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
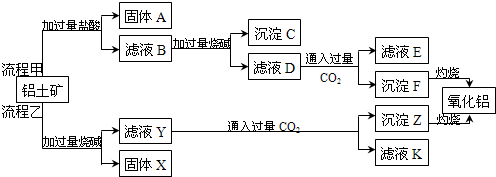
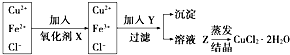 ��ҵ����ȡ������CuCl2•2H2O����Ҫ�����ǣ�
��ҵ����ȡ������CuCl2•2H2O����Ҫ�����ǣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����������������ʣ�ʵ�鲽�����£�
����������������ʣ�ʵ�鲽�����£� ˮ�γɵĹ������е�Ϊ85�棻��ʵ���м���ױ�����ˮ����������С�ĵؼ���5mLŨ���ᣬҡ�����Ⱥ����1��2����ʯ����װ��ʵ��װ�ã���85��95���º��¼��ȷ�Ӧ1.5Сʱ��
ˮ�γɵĹ������е�Ϊ85�棻��ʵ���м���ױ�����ˮ����������С�ĵؼ���5mLŨ���ᣬҡ�����Ⱥ����1��2����ʯ����װ��ʵ��װ�ã���85��95���º��¼��ȷ�Ӧ1.5Сʱ��| ���� | ������ | ��ɫ״̬ | ����ܶ� | �۵㣨�棩 | �е㣨�棩 |
| ˮ������� | 152 | ��ɫҺ�� | 1.18 | -8.6 | 224 |
| ˮ���� | 138 | ��ɫ���� | 1.44 | 158 | 210 |
| �״� | 32 | ��ɫҺ�� | 0.792 | -97 | 64.7 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
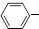 C2H5��g��?
C2H5��g��?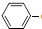 CH=CH2��g��+H2��g����H=akJ��mol-1����һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ�IJ������ݼ��±���
CH=CH2��g��+H2��g����H=akJ��mol-1����һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ�IJ������ݼ��±���| ʱ��/min | 0 | 10 | 20 | 30 | 40 |
| n���ұ���/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n������ϩ��/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
| A�� | ��Ӧ��ǰ20 min��ƽ������Ϊv��H2��=0.004mol•L-1•min-1 | |
| B�� | ���������������䣬�����¶ȣ�ƽ��ʱ��c���ұ���=0.08mol•L-1����a��0 | |
| C�� | ���������������䣬�������г��벻���뷴Ӧ��ˮ������Ϊϡ�ͼ������ұ���ת����Ϊ50.0% | |
| D�� | ��ͬ�¶��£���ʼʱ�������г���0.10mol�ұ���0.10mol����ϩ��0.30molH2���ﵽƽ��ǰv��������v���棩 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.2mol/L | B�� | 1.5mol/L | C�� | 1.6mol/L | D�� | 2.0mol/L |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com