
| A�������������£�44.8 L����������ֽ��22.4 L������22.4 L��������270 kJ���� |
| B�������������£�1 mol������1 mol������Ӧ����2 molҺ̬������ų���������270 kJ |
| C�������������£�1 mol������ 1 mol�����������ܺʹ��� 2 mol��������������� |
| D�������Ȼ�ѧ����ʽ���ɱ�ʾΪ��1/2 H2 (g) +1/2 F2 (g)="==" HF (g) ��H = ��135 kJ�� mol-1 |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��S����б����S����������Ϊͬ���칹�� |
| B����H3�� + 0.33 kJ��mol-1 ,��б��ת��Ϊ������ķ�Ӧ�����ȷ�Ӧ |
| C��S(��б��s) = S(������s) ��H3��0��������ȵ�б���ȶ� |
| D��S(��б��s) = S(������s) ��H3��0����б����������ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A�� �� ��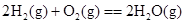 |
| B��C(ʯī)+O2(g)===CO2(g) C(���ʯ)+O2(g)===CO2(g) (ʯī�Ƚ��ʯ�ȶ�) |
C�� ���� ���� |
D�� �� ��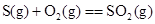 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������ᷴӦ | B�����ȵ�ľ̿��CO2��Ӧ |
| C��������ԭ����ͭ | D��Ba(OH)2��8H2O������NH4Cl����ķ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A���÷�ӦΪ���ȷ�Ӧ |
| B���÷�ӦΪ���ȷ�Ӧ |
| C����Ӧ�������������������������� |
| D���÷�Ӧֻ���ڼ��������²��ܽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ȷ�Ӧ | B�������кͷ�Ӧ |
| C����ѩ�ڻ� | D����ɫֲ��Ĺ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������������ȼ�յ��Ȼ�ѧ����ʽ�ǣ�P4��s��+5O2��g��=P4O10��s�� ��H=-745.8kJ��mol-1 |
| B������ת���ɰ���ʱ�ų����� |
| C��31g�������̺�������Ϊ738.5k |
| D�����ױȰ����ȶ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com