
|
已知在相同条件下,气体的密度与它的摩尔质量呈正比.一只气球若放在空气中静止不动,那么在相同条件下,该气球放在下列气体中会下沉的是 | |
| [ ] | |
A. |
H2 |
B. |
Cl2 |
C. |
CO2 |
D. |
O2 |
科目:高中化学 来源: 题型:
| 4 |
| 3Vt |
| 4 |
| 3Vt |
查看答案和解析>>
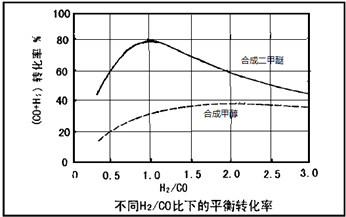
科目:高中化学 来源: 题型:阅读理解
| 反应过程 | 化学方程式 | △H(kJ?mol-1) |
| 甲醇合成反应 | 2H2(g)+CO(g)=CH3OH(g) | -90.8 |
| 水煤气变换反应 | CO(g)+H2O(g)═CO2(g)+H2(g) | -41.3 |
| 甲醇脱水反应 | 2CH3OH(g)=CH3OCH3(g)+H2O(g) | -23.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com