
【题目】某化学实验小组用酸性KMnO4溶液与草酸(H2C2O4)溶液反应,研究外界条件对反应速率的影响,实验操作及现象如下:
编号 | 实验操作 | 实验现象 |
I | 向一支试管中先加入1 mL 0.01 mol/L酸性KMnO4溶液,再加入1滴3 mol/L硫酸和9滴蒸馏水,最后加入1 mL 0.1 mol/L草酸溶液 | 前10 min内溶液紫色无明显变化,后颜色逐渐变浅,30 min后几乎变为无色 |
II | 向另一支试管中先加入1 mL 0.01 mol/L酸性KMnO4溶液,再加入10滴3 mol/L硫酸,最后加入1 mL 0.1 mol/L草酸溶液 | 80 s内溶液紫色无明显变化,后颜色迅速变浅,约150 s后几乎变为无色 |
(1)写出高锰酸钾与草酸反应的离子方程式:______________________________。
(2)由实验I、II可得出的结论是_______________________________。
(3)关于实验II中80 s后溶液颜色迅速变浅的原因,该小组提出猜想:反应中生成的Mn2+对该反应有催化作用。利用提供的试剂设计实验III,验证猜想。提供的试剂:0.01 mol/L酸性 KMnO4溶液,0.1 mol/L草酸溶液,3 mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水补全实验III的操作:向试管中先加入1 mL 0.01 mol/L酸性KMnO4溶液,_______,最后加入1 mL 0.1 mol/L草酸溶液。
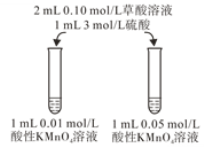
(4)该小组拟采用如图所示的实验方案继续探究KMnO4溶液浓度对反应速率的影响。你认为他们的实验方案______(填“合理”或“不合理”),理由是___________。
【答案】5H2C2O4+2MnO4-+6H+==2Mn2++10CO2↑+8H2O 其他条件相同时,H+(或硫酸)浓度越大,反应速率越快 再加入10滴3 mol/L硫酸,然后加入少量MnSO4固体 不合理 KMnO4溶液浓度不同,溶液起始颜色深浅不同,无法通过比较褪色时间长短判断反应快慢
【解析】
⑴高锰酸钾与草酸反应生成锰离子、二氧化碳、水。
⑵实验I、II其他条件相同,只是氢离子浓度不相同,氢离子浓度越大,变色所需时间越短,反应速率越快。
⑶为了验证实验II中80 s后溶液颜色迅速变浅的是否有锰离子其催化作用,应其他条件相同,只改变锰离子的量。
⑷高锰酸钾浓度不同,则高锰酸钾溶液颜色深浅不同,不能通过褪色时间长短来判断应快慢。
⑴高锰酸钾与草酸反应生成锰离子、二氧化碳、水,其离子方程式:5H2C2O4+2MnO4-+6H+ = 2Mn2++10CO2↑+8H2O;故答案为:5H2C2O4+2MnO4-+6H+ = 2Mn2++10CO2↑+8H2O。
⑵实验I、II其他条件相同,只是氢离子浓度不相同,氢离子浓度越大,变色所需时间越短,反应速率越快,因此实验I、II可得出的结论是其他条件相同时,H+(或硫酸)浓度越大,反应速率越快;故答案为:其他条件相同时,H+(或硫酸)浓度越大,反应速率越快。
⑶为了验证实验II中80 s后溶液颜色迅速变浅的是否有锰离子其催化作用,应其他条件相同,只改变锰离子的量,因此向试管中先加入1 mL 0.01 molL1酸性KMnO4溶液,再加入10滴3 molL1硫酸,然后加入少量MnSO4固体,最后加入1 mL 0.1 molL1草酸溶液;故答案为:再加入10滴3 molL1硫酸,然后加入少量MnSO4固体。
⑷由于高锰酸钾浓度不同,则高锰酸钾溶液颜色深浅不同,不能通过褪色时间长短来判断应快慢,因此他们的实验方案不合理;故答案为:不合理;KMnO4溶液浓度不同,溶液起始颜色深浅不同,无法通过比较褪色时间长短判断反应快慢。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】25℃时将10mLpH=11的氨水加水稀释至100mL,下列判断正确的是
A.稀释后溶液的pH=7B.氨水的电离度增大,溶液中所有离子的浓度均减小
C.稀释过程中![]() 增大D.pH = 11氨水的浓度为0.001mol/L
增大D.pH = 11氨水的浓度为0.001mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
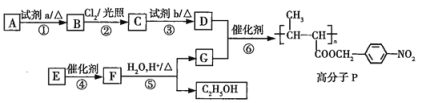
【题目】功能高分子![]() 的合成路线如图所示:
的合成路线如图所示:
(1)![]() 的分子式是
的分子式是![]() ,其结构简式是__________________。
,其结构简式是__________________。
(2)试剂![]() 是__________________。
是__________________。
(3)反应③的化学方程式:__________________。
(4)![]() 的分子式是
的分子式是![]() 。
。![]() 中含有的官能团:__________________。
中含有的官能团:__________________。
(5)反应④的反应类型是__________________。
(6)反应⑤的化学方程式:___________________________。
(7)已知:![]() 。以乙烯为起始原料,选用必要的无机试剂合成
。以乙烯为起始原料,选用必要的无机试剂合成![]() ,写出合成路线____________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线____________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化锂(Li2O)是离子晶体,其晶格能可以通过图所示循环进行计算。下列说法错误的是
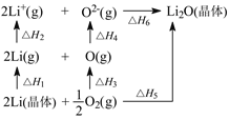
A.O=O键键能为ΔH3
B.Li原子的第一电离能为0.5ΔH2
C.Li2O的晶格能为ΔH6取正值
D.ΔH1+ΔH2+ΔH3+ΔH4+ΔH6=ΔH5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298 K时,在20.0mL 0.10mol/LH2SO4溶液中滴入0.10 mol/L的NaOH溶液,溶液的pH与所加NaOH溶液的体积关系如图所示。下列叙述正确的是
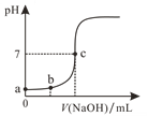
A.滴定过程最好用甲基橙作指示剂
B.a点溶液的pH=1.0
C.b点溶液中c(H+)=0.05mol/L
D.c点对应的NaOH溶液体积为20.0mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁锂是制作电池的材料,其制备过程可以简化成如图所示。下列说法错误的是( )
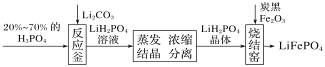
A.蒸发需要的硅酸盐材料仪器有:烧杯、酒精灯、玻璃棒、泥三角
B.反应釜中反应的化学方程式为2H3PO4+Li2CO3=2LiH2PO4+H2O+CO2↑
C.分离的操作是过滤
D.烧结窑中氧化铁与炭黑发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组在实验室通过6NaClO3 + CH3OH + 3H2SO4 = 6ClO2 + 5H2O + 3Na2SO4 + CO2制备ClO2,并将其转化为便于运输和储存的NaClO2固体,实验装置如图所示。(已知ClO2沸点为10℃,浓度较高时易发生爆炸)下列说法正确的是
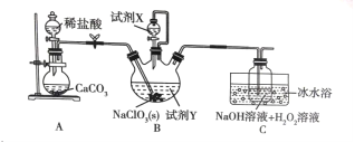
A.试剂X是甲醇
B.B中开始反应后立即停止通二氧化碳
C.此实验可以不用冰水浴
D.C中发生的反应方程式为:2ClO2+2NaOH+H2O2=2NaClO2+2H2O+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如下图所示,下列关于RCl5分子的说法中正确的是( )
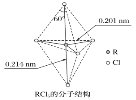
A. 每个原子都达到8电子稳定结构
B. 分子中5个R—Cl键键能不相同
C. 键角(Cl—R—Cl)有90°、120°、180°几种
D. RCl5受热后会分解生成分子RCl3,RCl5和RCl3都是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关橡胶的叙述正确的是( )
A.从废轮胎上刮下的橡胶粉末可溶于有机溶剂
B.天然橡胶的成分是顺式聚异戊二烯![]() ,能溶于汽油
,能溶于汽油
C.天然橡胶![]() 和杜仲胶
和杜仲胶![]() 互为同分异构体
互为同分异构体
D.硅橡胶![]() 属于无机橡胶,是无机高分子化合物
属于无机橡胶,是无机高分子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com