
| A. | 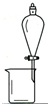 用CCl4提取溴水中的Br2 用CCl4提取溴水中的Br2 | B. | 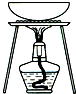 从KI和I2的固体混合物中回收I2 从KI和I2的固体混合物中回收I2 | ||
| C. | 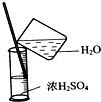 稀释浓硫酸 稀释浓硫酸 | D. | 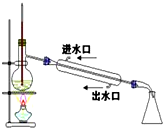 工业酒精制备无水酒精 工业酒精制备无水酒精 |
分析 A.用CCl4提取溴水中的Br2,应该采用萃取方法,需要的仪器有分液漏斗、烧杯;
B.碘单质易升华;
C.量筒只能量取溶液,不能溶解或稀释药品,且稀释浓硫酸时应该将浓硫酸倒入水中;
D.蒸馏时温度计测量馏分温度,且冷凝管中上口是出水口、下口是进水口.
解答 解:A.用CCl4提取溴水中的Br2,应该采用萃取方法,需要的仪器有分液漏斗、烧杯,符合条件,故A正确;
B.加热后,碘单质易升华,剩余的是KI,采用该方法得不到碘单质,故B错误;
C.量筒只能量取溶液但不能溶解或稀释药品,要稀释浓硫酸需要烧杯,且稀释浓硫酸时应该将浓硫酸倒入水中,防止溅出液体而产生安全事故,故C错误;
D.乙醇和水互溶,应该采用蒸馏方法分离,蒸馏时温度计测量馏分温度,且冷凝管中上口是出水口、下口是进水口,故D错误;
故选A.
点评 本题考查实验方案评价,涉及基本操作、仪器的选取等知识点,明确实验原理及基本操作规范性是解本题关键,题目难度不大.


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ②⑤ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑦ | B. | ③④⑤⑥ | C. | ①②⑤⑦ | D. | ①②⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验 | ① | ② | ③ | ④ |
| V(HNO3)/mL | 50 | 100 | 150 | 200 |
| V(NO)/L | 1.344 | 2.688 | 3.36 | 3.36 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业制取硝酸时尾气用氢氧化钠溶液吸收 | |
| B. | 氯气泄露时,应用蘸有肥皂水的湿毛巾捂住口鼻到安全区域 | |
| C. | 家中做卫生保洁时,严禁漂白粉与浓盐酸混合使用,否则会产生有毒气体 | |
| D. | 家中发生天然气泄露时,应立即使用室内电话报警 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
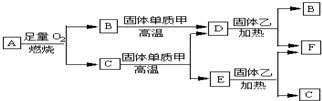
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com