
| A、v(A)=0.5 mol?L-1?s-1 |
| B、v(B)=0.3 mol?L-1?s-1 |
| C、v(C)=0.7 mol?L-1?s-1 |
| D、v(D)=1 mol?L-1?s-1 |
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
| A、②⑤ | B、①③ |
| C、②③⑤ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属腐蚀就是金属失去电子被还原的过程 |
| B、将水库中的水闸(钢板)与外加直流电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀 |
| C、纯银质物品久置表面变暗,是银发生吸氧腐蚀的结果 |
| D、钢板上的铁铆钉处在潮湿的空气中直接发生反应:Fe-3e-═Fe3+,继而形成铁锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol O2所含的原子数目为NA |
| B、0.5mol H2O的质量为9g |
| C、16g CH4分子含有的电子数目为NA |
| D、标准状况下,11.2L氢气含有分子的物质的量是0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1,3-丁二烯(CH2=CH-CH=CH2)与等物质的量的Br2发生加成反应 |
B、2-氯丁烷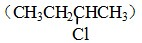 与NaOH乙醇溶液共热发生消去HCl分子的反应 与NaOH乙醇溶液共热发生消去HCl分子的反应 |
| C、丙炔与足量的溴水发生的加成反应 |
| D、CH2=CH-CH3与HBr发生的加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、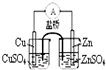 如图能组成Zn、Cu原电池 |
B、 如图能证明非金属性C>Si |
C、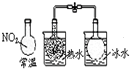 如图说明反应2NO2?N2O4,△H>0 |
D、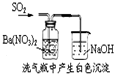 如图白色沉淀为BaSO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com