
���� ��1������20%���ܶ�Ϊ1.2g/mL��������������Һ����������ʵ���Ũ��c=$\frac{1000���ѡ�w%}{M}$��
��2����װ�����Ͻ���Թ��еμ�������20%NaOH��Һ���������������ɣ�����������������Һ��Ӧ����ƫ�����ƺ�������
��3����ʵ��һ���Թ�����μ���6mol/L����������������ʼʱ��������������Һ��Ӧ�������μ�������ƫ��������Һ�����ᷴӦ�����������������������μ�����������������Ӧ�����ܽ⣬ԭ��Һ�в�������ȫ�ܽ⣬��ʱ��Һ��dz��ɫ�����������ͺϽ��е�����Ӧ�����Ȼ�������Һ���ݾ���һ��ʱ�����Һ���ػ�ɫ���������ӱ�����Ϊ�����ӣ�
��4������������ͺϽ��е�����Ӧ�����Ȼ�������Һ����ֹһ��ʱ����dz��ɫ��Ϊ�ػ�ɫ���������ӱ�����Ϊ�����ӣ�
��5����Ӧ����˵����������Ҫ�ɷ�����������
��� �⣺��1������20%���ܶ�Ϊ1.2g/mL��������������Һ����������ʵ���Ũ��c=$\frac{1000��1.2��20%}{40}$mol/L=6mol/L������20%���ܶ�Ϊ1.2g/mL��������������Һ��6mol/L����������ʵ���Ũ����ͬ��
�ʴ�Ϊ��=��
��2����װ�����Ͻ���Թ��еμ�������20%NaOH��Һ���������������ɣ�����������������Һ��Ӧ����ƫ�����ƺ�������2Al+2NaOH+2H2O��2NaAlO2+3H2����
�ʴ�Ϊ��2Al+2NaOH+2H2O��2NaAlO2+3H2����
��3����ʵ��һ���Թ�����μ���6mol/L���������������ٿ�ʼû�����������ǿ�ʼʱ��������������Һ��Ӧ����Ӧ�����ӷ���ʽΪA��H++OH-��H2O��
���а�ɫ��״�������ɣ������μ�������ƫ��������Һ�����ᷴӦ��������������������Ӧ�����ӷ���ʽΪ��AlO2-+H ++H2O��Al��OH��3�����۰�ɫ������ʧ�������μ�����������������Ӧ�����ܽ⣬��Ӧ�����ӷ���ʽΪ��Al��OH��3+3H+��Al3++3H2O����ԭ��Һ�в�������ȫ�ܽ⣬��Ӧ�����ӷ���ʽΪFe+2H+=Fe2++H2������ʱ��Һ��dz��ɫ�����������ͺϽ��е�����Ӧ�����Ȼ�������Һ���ݾ���һ��ʱ�����Һ���ػ�ɫ���������ӱ�����Ϊ�����ӣ�
�ʴ�Ϊ��A��B��C��
��4������������ͺϽ��е�����Ӧ�����Ȼ�������Һ����ֹһ��ʱ����dz��ɫ��Ϊ�ػ�ɫ���������ӱ�����Ϊ�����ӣ�
�ʴ�Ϊ����Һ��Fe2+������ΪFe3+��
��5������������֪�����ɷ�Ϊ�������ĺϽ�֤��������ȷ��
�ʴ�Ϊ��������
���� ���⿼������ҺŨ�ȼ��㡢�Ͻ�ɷֵ�ʵ��̽���ͷ�Ӧ���̷����жϡ���Ҫ�������仯�������ʵ�����Ӧ�ã����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
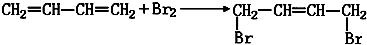

 ��C
��C ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | þԭ�ӵļ۵����������� | |
| B�� | þ����Ũ��������ᣬ���治�ܶۻ����������� | |
| C�� | þ�����ڿ����к���ʢCO2�ļ���ƿ��ȼ�գ������������� | |
| D�� | ����Ӳ�ȡ���չ�ԡ��۵����þ�á��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ�ӵ�ʵ������ | B�� | ���������������� | ||
| C�� | ����̼-12ԭ��������$\frac{1}{12}$ | D�� | ���ԭ�������ĵ�λ��Kg |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ������NH4Cl��NaNO2��Һ�������N2 | |
| B�� | SnCl4��ˮ�ķ�Ӧ��SnCl4+2H2O�TSnO2+4HCl | |
| C�� | �˹���Ҷ��ȡ���飺CO2+2H2O$\frac{\underline{\;\;\;\;\;\;\;��\;\;\;\;\;\;\;}}{�˹���Ҷ}$CH4+2O2 | |
| D�� | �����鶾��4Ag+2H2S+O2�T2Ag2S+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ɫ��������NO�����ܺ�CO2 | |
| B�� | ���г�����BaSO4�����ܺ�BaCO3 | |
| C�� | �϶����ڵ�������Al3+��SO42-��NO3-��Mg2+���϶������ڵ�������Ba2+��Fe2+��CO32-��I-������ȷ����������K+��Cl- | |
| D�� | ���к���ɫ����ͨ��ˮ�з�����Ӧ�����ӷ���ʽΪ��3NO2+H2O�TH++NO3-+2NO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| n��M����n��H2O�� | Mת���� | H2Oת���� |
| 1��1 | 0.5 | 0.5 |
| 1��2 | 0.67 | 0.33 |
| 1��3 | 0.75 | 0.25 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com