
现将2molA和1molB加入2L密闭容器中发生反应:2A(g)+B(g)  2C(g),分别在Tl和T2时测得生成物C的物质的量随时间变化如图所示,下列说法正确的是
2C(g),分别在Tl和T2时测得生成物C的物质的量随时间变化如图所示,下列说法正确的是
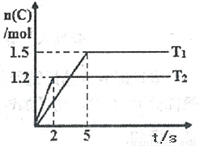
A. T1<T2
B. 该反应在温度为T1时达到平衡时,容器中A与C的物质的量浓度相等
C. 温度为T2时,2s内B的平均速率为0.3mol·L-1·s-l
D. 温度为T1时,达平衡时反应物A的转化率为60%
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:简答题
含硫化物是自然界中最为重要的自然资源之一,在生产生活中应用非常广泛。
(1)燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点。以下是用硫和氮的氧化物之间的相互转化联合进行的脱硫和脱硝技术反应的热化学方程式。
NO2(g)+SO2(g)+H2O(l)=H2SO4(l) +NO(g) △H=a kJ·mol-1
2NO(g)+O2(g)=2NO2(g) △H=b kJ·mol-1
① 反应2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l) 的△H=_______KJ/mol-1。
② 将SO2通入硫酸铁溶液也能发生类似的反应。请写出该反应的离子方程式____________ 。
(2)MnSO4是重要的基础锰盐。工业上,生产MnSO4的方法有多种。
①一种较为环保的方法是:利用纤维素水解产物还原软锰矿的方法生产MnSO4,其反应方程式如下:(C6H10O5)n+nH2SO4→n(C6H11O5)HSO4
n(C6H11O5)HSO4 +nH2O →n C6H12O6+nH2SO4
C6H12O6 +12H2SO4+12MnO2→12MnSO4+6CO2↑+18H2O
从理论上讲,每生产1吨MnSO4需要的纤维素的质量为____吨。
②软锰矿中都含有一定量的砷的化合物,如果不除砷很难达到饲料级的生产标
准。工业上常用氧化剂来除去其中的砷。可以除去砷的氧化剂有:ClO-、KMnO4、(NH4)2S2O8、O3、H2O2等,但在实际生产中,选用的氧化剂是软锰矿,可能的原因是_________。
③在生产MnSO4的浸出渣中常会产生一些硫磺,可以利用四氯乙烯来回收硫磺,
回收硫磺过程中受外界影响较大的因素主要有:萃取温度、液固比等。下图1是上述3种因素对萃取硫磺质量影响的关系图。

请根据以上图表信息,选择最佳的萃取温度和液固比_____________。
(3)有人设想用电化学法将SO2转化为H2SO4的原理如图2所示。

① 该电解质溶液中质子的流向是_____;(填“从正极流向负极”或“从负极流向正极”)
② 写出该电池负极反应的电极反应方程式:_________
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第二次模考化学试卷(解析版) 题型:填空题
实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:软锰矿与过量固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4。请回答:
(1)软锰矿制备K2MnO4的化学方程式是_______________________;
(2)K2MnO4制备KMnO4的离子方程式是_______________;
(3)若用2.5g软锰矿(含MnO2 80%)进行上述实验,KMnO4的理论产量为_______________。
(4)KMnO4能与热的经硫酸酸化的Na2C2O4溶液反应生成Mn2+和CO2,该反应的化学方程式是________________________;
(5)上述制得KMnO4产品0.165g,恰好与0.335g Na2C2O4反应完全,该KMnO4的纯度为___。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第二次模考化学试卷(解析版) 题型:选择题
化学与生活、环境密切相关,下列说法正确的是
A. 可以用淀粉检验加碘食盐中是否含有碘元素
B. 适量饮酒对身体有利的原因是酒精不能使蛋白质变性
C. PM2.5亦称可入肺颗粒物,表面积大,能吸附有毒有害物质
D. 使用生物酶降解生活污水中的有机物,可以防止水体富营养化
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三3月选考化学试卷(解析版) 题型:推断题
A是一种常见的烃,相同条件下相对氢气的密度为13,D能与小苏打反应产生气体,它们之间存在如下图所示的转化关系(反应所需条件已略去):

请回答:
(1)D中含有官能团的名称是________________。
(2)反应⑤发生的条件是加热和催化剂,其化学方程式为________________。
(3)检验乙醛中所含官能团可以选用的试剂是________________。
(4)下列说法正确的是________________。
a.上述反应中属于加成反应的只有①和④ b.除去C中含有D可加生石灰蒸馏
c.工业上获得大量B可通过石油裂化工艺 d.等物质的量B和C完全燃烧耗氧量相同
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三3月选考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A. 油脂是热值最高的营养物质,可以制造肥皂和油漆
B. 利用二氧化碳制造全降解塑料,符合绿色化学理念
C. 脱脂棉、滤纸、蚕丝的主要成分均为纤维素,完全水解能得到葡萄糖
D. 酒精、福尔马林用于杀菌消毒的原理都是使蛋白质变性
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三3月选考化学试卷(解析版) 题型:选择题
下列关于能源的说法不正确的是
A. 植物通过光合作用,将太阳能转化为生物质能
B. 在农村推广建造沼气池,是对生物质能的有效利用
C. 天然气的主要成分是甲烷,是一种可再生的清洁能源
D. 氢能是重要的清洁能源,在蓝绿藻、微生物和太阳光作用下使水分解制氢是目前科学家研究的新方法之一
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一下学期开学考试化学试卷(解析版) 题型:选择题
镁铝合金4.08 g溶于250 ml 2mol/L的盐酸中,标准状况下放出气体的体积为4.48 L,向反应后的溶液中加入500 ml NaOH溶液,充分反应后最终产生白色沉淀。下列有关说法不正确的是( )
A. 4.08 g镁铝合金中含有镁和铝的质量分别为1.92g、2.16g
B. 生成沉淀的最大质量为10.88 g
C. 若白色沉淀只有Mg(OH)2,该NaOH溶液的浓度至少为0.96mol/L
D. 溶解4.08 g镁铝合金时,剩余盐酸的物质的量为0.1 mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷(解析版) 题型:选择题
一定量的盐酸跟过量锌粉反应时,为了减缓反应速率但又不影响生成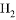 的总量,可采取的措施是( )
的总量,可采取的措施是( )
A. 加入少量 固体 B. 加入少量
固体 B. 加入少量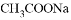 固体
固体
C. 加入少量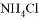 固体 D. 加入少量
固体 D. 加入少量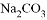 固体
固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com