
分析 (1)依据电解过程中电子守恒,结合氧气生成的电极反应计算电子转移物质的量,依据析出金属质量和物质的量计算摩尔质量,分析判断金属;
(2)依据电子守恒计算电解过程中氢氧根离子减小和溶液中氢离子增加物质的量相同计算电解后溶液的酸溶液浓度.
解答 解:(1)n(O2)=$\frac{0.224L}{22.4L/mol}$=0.01mol,则转移电子n(e-)=0.01×4=0.04mol,依据电子得失守恒及+2价金属,所以n(金属)=0.02mol,n=$\frac{m}{M}$得到,M=$\frac{1.28g}{0.02mol}$=64g/mol;则该金属的名称为铜,
答:该金属的名称为铜;
(2)依据反应4OH--4e-=O2↑+2H2O可知每转移4个电子会产生4个氢离子,由于n(e-)=0.04mol,得到n(H+)=0.04mol,c(H2SO4)=$\frac{n}{V}$=$\frac{0.02mol}{0.1L}$=0.2mol/L,
答:通电后硫酸溶液的物质的量浓度为0.2mol/L.
点评 本题考查了电解池原理分析,电解过程中电子守恒,电极反应的计算应用,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
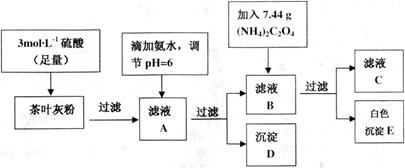
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸可能过量 | |
| B. | 不溶物中一定含有Fe | |
| C. | 不溶物中一定含有Cu,但不一定含有Fe | |
| D. | 滤液中一定含有Fe2(SO4)3,但不一定含有FeSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 LCl2分别与铁和铜反应时,失电子数目均为NA | |
| B. | 1mol Na2O2与CO2足量反应时,转移NA个电子 | |
| C. | 1mol•L-1的NaOH溶液中含Na+数目为NA | |
| D. | 1mol Na2O2晶体中含有的阴离子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,结构简式H2C=CH2.
,结构简式H2C=CH2. ,反应类型是加聚反应.
,反应类型是加聚反应. )与乙醇(
)与乙醇( )反应生成酯(
)反应生成酯( )和水的反应机理,反应过程中酸分子断裂C-O单键,醇分子断裂O-H键.试完成下列反应方程式:
)和水的反应机理,反应过程中酸分子断裂C-O单键,醇分子断裂O-H键.试完成下列反应方程式: +CH3CH2-18O-H$\stackrel{一定条件}{→}$CH3CO18OCH2CH3+H2O.
+CH3CH2-18O-H$\stackrel{一定条件}{→}$CH3CO18OCH2CH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浓硫酸配制稀硫酸时,浓硫酸缓慢加入水中,并用玻璃棒不断搅拌 | |
| B. | 用酒精和汽油都可以萃取碘水中的碘 | |
| C. | 潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量 | |
| D. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com