
下列有关实验操作、现象和解释(或结论)都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
|
| A. | A | B. | B | C. | C | D. | D |
考点:
化学实验方案的评价;难溶电解质的溶解平衡及沉淀转化的本质;二价Fe离子和三价Fe离子的检验;铝金属及其化合物的性质实验;氨的制取和性质.
专题:
实验评价题.
分析:
A.铁过量,反应生成硝酸亚铁;
B.AgI的溶解度比AgCl的小;
C.Al与稀硝酸发生氧化还原反应生成NO;
D.浓氨水中存在NH3.H2O⇌NH4++OH﹣,碱遇红色石蕊试纸变蓝.
解答:
解:A.过量的Fe粉中加入稀HNO3,反应生成硝酸亚铁,滴入KSCN溶液,溶液不显红色,故A错误;
B.AgI的溶解度比AgCl的小,则AgI沉淀中滴入稀KCl溶液,不会生成白色沉淀,故B错误;
C.Al与稀硝酸发生氧化还原反应生成NO、硝酸铝和水,观察到气泡冒出,故C错误;
D.浓氨水中存在NH3.H2O⇌NH4++OH﹣,碱遇红色石蕊试纸变蓝,则说明浓氨水呈碱性,故D正确;
故选D.
点评:
本题考查化学实验方案的评价,明确发生的化学反应是解答本题的关键,注意发生的反应与实验现象的关系,选项B为易错点,题目难度中等.


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
2010年上海世博会主题是“城市,让生活更美好”,试回答下列问题:
(1)为确保世博会期间申城空气质量优良率达到95%以上,世博会期间的空气质量状况监测中,不需要监测的指标是 .
a.可吸入颗粒物(PM10)b.NO2浓度 c.SO2浓度 d.CO2浓度;
(2)为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量.对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为 .
(3)为2010年世博会期间提供科学有效的环境质量保障方案,白龙港污水处理厂升级改造,处理废水时加入KAl(SO4)2•12H2O或碱式氯化铝的作用是 ;通入臭氧或二氧化氯的作用是消毒剂.某农村地区为获得饮用水,在将地表水取回家后,常使用漂白粉或漂白精片进行杀菌消毒,其原理可用化学方程式表示为 .
(4)近日,世博会中国馆﹣﹣“东方之冠”,它由钢筋混凝土、7000多块红色铝板和1200多块玻璃等建成.其中部分玻璃为石英玻璃,它化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧黄铜(Cu、Zn合金,含少量杂质Fe)制备胆矾晶体(CuSO4·5H2O)及副产物ZnO。制备流程图如下:
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)。
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 沉淀完全的pH | 3.0 | 8.8 | 8.9 |
请回答下列问题:
(1)加入ZnO调节pH=a的目的是______________,a的范围是 。
(2)由不溶物E生成溶液D的化学方程式为____________________________。
(3)滤液A中加入H2O2反应的离子方程式为 。
(4)由溶液D制胆矾晶体包含的主要操作步骤是 。
(5)下列试剂可作为Y试剂的是______。
A.ZnO B.NaOH C.Na2CO3 D.ZnSO4
若在滤液C中逐滴加入盐酸直到过量,则产生的现象是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是( )
A. n(Cl2):n(Fe)=5:4 5Cl2+4Fe  2FeCl2+2FeCl3
2FeCl2+2FeCl3
B. n(Cl2):n(FeBr2)=1:1 Fe2++2Br﹣+Cl2═Fe3++Br2+2Cl﹣
C. n(MnO4﹣):n(H2O2)=2:3 2MnO4﹣+3H2O2+6H+═2Mn2++4O2↑+6H2O
D. n(Fe):n[HNO3(稀)]=1:3 4Fe+12H++3NO3﹣═3Fe2++Fe3++3NO↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学中很多“规律”都有其使用范围,下列根据有关“规律”推出的结论合理的是( )
|
| A. | 根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 |
|
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
|
| C. | 根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性 |
|
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象预测正确的是( )
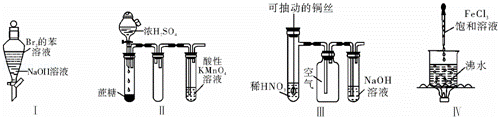
|
| A. | 实验Ⅰ:振荡后静置,上层溶液颜色保持不变 |
|
| B. | 实验Ⅱ:酸性KMnO4溶液中出现气泡,但颜色不变 |
|
| C. | 实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
|
| D. | 实验Ⅳ:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的.已知:
氧化性:IO3﹣>Fe3+>I2;还原性:S2O32﹣>I﹣
3I2+6OH﹣═IO3﹣+5I﹣+3H2O;KI+I2⇌KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.
①加KSCN溶液显红色,该红色物质是(用化学式表示);CCl4中显紫红色的物质 (用电子式表示).
②第二份试液中加入足量KI固体后,反应的离子方程式为 、 .
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失.
写出潮湿环境下KI与氧气反应的化学方程式: .
将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质作为食盐加碘剂是否合适? (填“是”或“否”),并说明理由 .
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失.下列物质中有可能作为稳定剂的是 .
A.Na2S2O3 B.AlCl3 C.Na2CO3 D.NaNO2.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列应用不涉及氧化还原反应的是( )
A.Na2O2用作呼吸面具的供氧剂
B.工业上电解熔融状态的Al2O3制备Al
C.工业上利用合成氨实现人工固氮
D.实验室用NH4Cl和Ca(OH)2制备NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com