
科目: 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:选择题
下列实验中,对应的现象以及结论都正确且两者具有因果关系是( )
选项 | 实验 | 现象 | 结论 |
A. | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
B. | 将铜粉加入1.0mol·L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
C. | 向FeCl2溶液中加入Na2O2粉末 | 出现红褐色沉淀和无色气体 | FeCl2溶液部分变质 |
D. | 将0.1mol·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol·L-1CuSO4溶液 | 先有白色沉淀生成后变为浅蓝色沉淀 | Cu(OH)2的Ksp比Mg(OH)2的小 |
查看答案和解析>>
科目: 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.高温下,可用焦炭和石英砂(SiO2)制取高纯度硅
B.CO2和钠在一定条件下可以得到金刚石和碳酸钠,反应中氧化剂和还原剂之比是4:1
C.用高纯度硅作为光导纤维的主要材料
D.现代海战通过喷放液体SiCl4(极易水解)和液氨可产生烟幕,其主要成分是NH4Cl
查看答案和解析>>
科目: 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:选择题
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的混合气体体积为(设反应中HNO3被还原成NO)( )
A.0.224L B.0.448L C.0.672L D.0.896L
查看答案和解析>>
科目: 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:选择题
某实验小组对一含有Al3+的未知溶液进行分析:往该溶液逐滴滴加某浓度NaOH溶液,所加NaOH溶液体积(ml)与产生沉淀的物质的量(mol)的关系如下图所示:下列说法错误的是( )

A.该未知溶液中至少含有3种阳离子
B.滴加的NaOH溶液的物质的量浓度为5 mol•L﹣1
C.若将最终沉淀过滤、洗涤、灼烧,其质量一定为6 g
D.若溶液中仅有两种金属阳离子,且另一种离子为二价阳离子,则a=10
查看答案和解析>>
科目: 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:推断题
常见无机物A、B、C、D存在如图转化关系:

(1)若D是氯碱工业的主要产品,B有两性氢氧化物,则反应 ②的离子方程式是: 。
②的离子方程式是: 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为 。
(3)若A为常见挥发性强酸,D是生产生活中用量最大用途最广的金属单质,,则B的化学式可能是 ,写出反应②的离子方程式为 。
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,则反应③的化学方程式 。
(5)若A、B、C的水溶液均显碱性,焰色反应均为黄色,D为CO2,用离子方程式解释B溶液显碱性的原因(用离子方程式表示)___________,举出C的一种用途_______。
查看答案和解析>>
科目: 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:填空题
(本题12分)
Ⅰ.某厂废水中含KCN,其浓度为0.01mol·L-1,现用氯氧化法处理,发生如下反应(化合物 中N化合价均为-3价):
中N化合价均为-3价):
(1)KCN+2KOH+Cl2=KOCN+2KCl+H2O被氧化的元素是______________。(用元素符号表示)
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:

(3)若将10 L含KCN的浓度为0.01mol· L-1的废水中KCN氧化除去,最少需要氯气_______mol。
Ⅱ.某实验小组为了测定(3)中溶液多余Cl2的含量,常用Na2S2O3标准溶液进行定量测定。
(4)现实验室需用480mL一定浓度的Na2S2O3溶液,配制该溶液所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需 。
(5)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42﹣,因此Na2S2O3常用作脱氯剂,该反应的离子方程式为 。
(6)现取(3)中溶液20.00mL,用a mol·L-1 Na2S2O3溶液进行滴定,经过平行实验测得消耗Na2S2O3标准溶液b mL,计算废液中Cl2的浓度为 mol·L-1 (用含a 、b的表达式表示) 。
查看答案和解析>>
科目: 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:实验题
三氯化硼(BCl3)是一种重要的化工原料,可用于制取乙硼烷(B2H6),也可作有机合成催化剂。某兴趣小组拟选用下列装置制备BCl3(已知BCl3的沸点为12.5 ℃,熔点为-107.3 ℃;2B+6HCl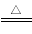 2BCl3↑+3H2↑。
2BCl3↑+3H2↑。
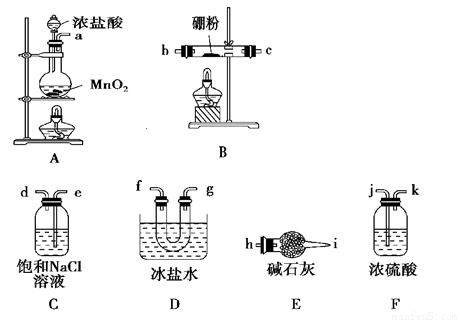
请回答下列问题:
(1)装置B中发生反应的化学方程式为 。
(2)按气流方向连接各装置的接口,顺序为a-( )- ( )- ( )- ( )- ( )-( )-f-g-h。连接好装置后的实验操作是__________________________。
(3)装置D的作用是 ;实验中若不用装置C,可能产生的危险是 。
(4)BCl3遇水发生水解观察到大量的白雾,生成两种酸,其反应的化学方程式为:_____________。
(5)装置E的作用除了可以吸收多余Cl2外,还起到的作用是__________________。
查看答案和解析>>
科目: 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:实验题
工业上用某矿渣(主要成分是Cu2O,少量杂质是Al2O3、Fe2O3和SiO2)提取铜的操作流程如下:
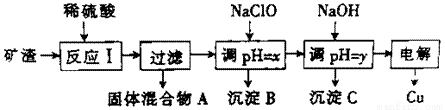
已知:①Cu2O+2H+=Cu+Cu2++H2O ②某些金属氢氧化物开始测沉淀和完全沉淀时的pH
沉淀物 |
|
|
|
|
开始沉淀pH | 5.4 | 4.0 | 2.2 | 5.8 |
沉淀完成pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)反应I中,与铁元素有关反应的离子方程式为 、 。
(2)y的数值范围是 。
(3)以上步骤中的NaOH可以用__________代替(填字母)
A.CuO B.NH4Cl C.Cu(OH)2
(4)电解过程中,阳极产物可能为_____________________。
(5)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为 。
查看答案和解析>>
科目: 来源:2017届广东省惠州市高三上学期调研模拟二化学试卷(解析版) 题型:选择题
在一定条件下,等物质的量的氯气与碘单质反应,得到一种红棕色液体ICl,ICl有很强的氧化性。现有下列两个反应:①2ICl+2Zn=ZnCl2+ZnI2;②ICl+H2O=HCl+HIO,下列叙述正确的是
A.Cl2与I2生成ICl是非氧化还原反应
B.反应①中,每生成1 mol ZnCl2时转移2mol电子
C.反应①中,ZnI2既是氧化产物又是还原产物
D.反应②中,ICl既是氧化剂又是还原剂
查看答案和解析>>
科目: 来源:2017届广东省惠州市高三上学期调研模拟二化学试卷(解析版) 题型:选择题
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是

A.工业上通过电解熔融状态MgCl2制取金属镁
B .用澄清的石灰水可鉴别NaHCO3和Na2CO3
.用澄清的石灰水可鉴别NaHCO3和Na2CO3
C.在第②、④步骤中,溴元素均被氧化
D.制取NaHCO3的反应是利用其溶解度小于NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com