
2008-2009学年度台儿庄区第一学期九年级期中素质教育质量检测
化学试卷
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,第Ⅰ卷1至4页,第Ⅱ卷5至8页,共100分。考试时间90分钟。
可能用到的相对原子质量:
H:1 O:
第Ⅰ卷(选择题 共48分)
一、选择题(本大题包括24个小题,每小题2分,共48分。每小题只有一个选项最符合题目要求。)
1.下列实验操作正确的是
A.实验完毕用嘴吹灭酒精灯火焰 B.将实验剩余的药品放回原试剂瓶
C.用药匙或纸槽把固体粉末送入试管 D.用嘴品尝实验室药品的味道
2.下列变化中属于化学变化的是
A.空气液化 B.矿石粉碎 C.高粱酿酒 D.海水晒盐
3.据报道,一高校对南京某湖湖底淤泥的一项调查实验查明,底层沉积的淤泥中铅、镍、铬、锌等重金属含量,已经超过了南京城市的土壤的重金属含量。这里提到的铅、镍、铬、锌是指
A.元素 B.原子 C.分子 D.单质
4.现有仪器:①烧杯 ②漏斗 ③量筒 ④酒精灯 ⑤托盘天平 ⑥玻璃棒等,用氯化钠固体配制一定质量分数的氯化钠溶液时,需用到的仪器有
A.①③⑤⑥ B.②③④⑤ C.①③④⑥ D.①②⑤⑥
5.以下观点中,与科学知识相违背的是
A.玉兰花香扑鼻而来,说明分子在不断地运动
B.原子是由原子核和核外电子构成的
C.物质都是由离子构成的
D.电解水得到氢气和氧气的事实,说明水分子含有氢原子和氧原子
6.下列有关酒精灯使用或存放的图示错误的是
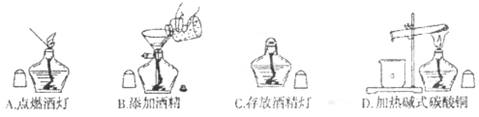
7.医生发现N2O(俗名“笑气”)在医疗上具有特殊功能。以下哪种物质中氯元素的化合价与N2O中氮元素的化合价相同
A.NaClO3 B.NaClO
8.甲原子与乙原子的质量比为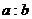 ,而乙原子与碳原子的质量比为
,而乙原子与碳原子的质量比为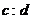 ,则甲原子的相对原子质量为
,则甲原子的相对原子质量为
A.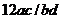 B.
B.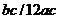 C.
C.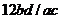 D.
D.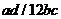
9.最近俄罗斯科学家利用第72号元素铪和第74号元素钨精确测定出月球至少比地球早700万年形成。铪、钨两种元素原子的本质不同是
A.核内质子数目 B.核内中子数目 C.核外电子数目 D.相对原子质量
10.我们饮用的水是原水净化所得,自来水厂科学合理的净水过程是
A.原水→加絮凝剂→沉淀→过滤→吸附→消毒→净水
B.原水→加絮凝剂→消毒→过滤→沉淀→吸附→净水
C.原水→过滤→消毒→加絮凝剂→吸附→沉淀→净水
D.原水→消毒→加絮凝剂→吸附→沉淀→过滤→净水
11.下表列出了不同温度下每立方厘米活性炭所能吸附的常见气体的体积。分析表中数据与气体组成、性质等的关系,你认为下列结论正确的是
H2
CO2
O2
N2
Cl2
气体的沸点(℃)
-252
-78
-183
-196
-34
被吸附的体积(mL)
4.5
97
35
11
494
A.气体分子所含原子个数多时,气体易被吸附
B.沸点越低的气体,越易被吸附
C.气体是化合物时,易被吸附
D.气体的相对分子质量越大,越易被吸附
12.下列关于化学的说法中错误的是
A.利用化学方法可以制造出自然界不存在的新物质
B.在化学变化中分子可以破裂重新组合成新分子
C.在化学变化中分子和原子都可以重新组合成新的分子和原子
D.元素周期律的发现使化学学习和研究有了一定的规律可循
13.下列关于实验现象的描述正确的是
A.磷在氧气中燃烧,产生大量白雾
B.木炭在氧气中燃烧,发出白色火焰,生成使澄清石灰水变浑浊的气体
C.镁带在空气中燃烧,发出耀眼的白光,放出大量的热,生成白色固体
D.铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
14.把肥皂水分别加到盛水的a、b两个烧杯中,a中产生的泡沫较少,浮渣较多,b中产生的泡沫较多。下列结论正确的是
A.a中盛的是硬水
B.b中盛的是硬水
C.a中溶有较少的可溶性钙和镁的化合物
D.b中溶有较多的可溶性钙和镁的化合物
15.马赫同学观察了原子结构示意图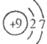 :通过分析、推理得到2条结论:
:通过分析、推理得到2条结论:
①该元素属于金属元素;②在化学反应中容易失去电子。他的结论中
A.①②均正确 B.①②均错误
C.①正确、②错误 D.①错误、②正确
16.下图是1994和2004年某城市的一天各个时刻监测到的空气中二氧化硫的含量,下列说法不正确的是
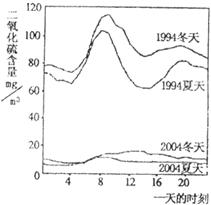
A.曲线显示冬天天气中的二氧化硫含量比夏天高
B.曲线显示了1994年一天中大约8点左右二氧化硫的含量较高
C.二氧化硫的含量在10年间降低的原因可能是加强了燃料的脱硫和控制了二氧化硫的排放
D.二氧化硫污染的主要来源是汽车排放的尾气,控制污染的方法是禁止使用汽车
17.“神舟七号”载人航天飞船发射成功,极大地增强了我们的民族自豪感,在航天飞船的失重环境中,下列实验操作最难完成的是
A.蒸馏 B.蒸发 C.溶解 D.过滤
18.从分子、原子的角度认识化学反应是创造新分子的基础,下图中●、○分别表示不同元素的原子,图中表示的反应与实际相符的是
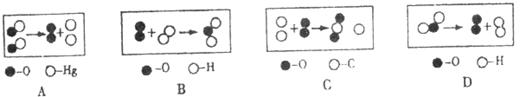
19.将一定量的NaOH溶于
A.25.6% B.25% C.78% D.22%
20.超导材料为具有零电阻及反磁性的物质,以Y2O3、BaCO3和CuO为原料经研磨烧结可合成一种高温超导物质Y2Ba4Cu6Ox,假设在研磨烧结过程中各元素的化合价无变化,则x的值为
A.12 B.
21.某同学用量筒准确量取20mL某液体,倒出部分后,俯视凹液面最低处,读数为11mL,则该同学实际倒出的液体体积是
A.大于9mL B.小于9mL
C.等于9mL D.可能大于也可能小于9mL
22.下列符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是
A.C60 B.Au C.O2 D.H
23.在下列各组相关内容的比较中,前者一定小于后者的是
A.通常状态下的液态水与受热后的水蒸气中分子间的间隔
B.SO3与SO2中硫元素的化合价
C.Al2O3与Fe2O3中氧元素的质量分数
D.过氧化氢的分解反应使用催化剂与不使用催化剂的反应速率
24.将溶质质量分数为10%的NaCl溶液
①蒸发
A.仅② B.①③ C.①④ D.②③
第Ⅱ卷(非选择题 共52分)
可能用到的相对原子质量:O:16 I:127 K:39
二、理解与应用(本大题包括7个小题,每空1分,共26分)
25.写出下列粒子的符号:
氢原子_________ 氧离子_________ 氧分子_________ 氧化铁_________
26.写出下列粒子符号的含义:
2P2O5_________ 2Na_________ SO2_________ 4H2O_________
27.地壳中含量最多的元素和地壳中含量最多的金属元素组成的化合物的化学式为_______。
28.在硫、铁、镁、磷、石蜡、过氧化氢、高锰酸钾等物质中,选择合适的物质,按要求写出反应的文字表达式,指出是化合反应还是分解反应?
(1)照明弹的原理____________________________________( )
(2)烟幕弹的原理____________________________________( )
(3)在空气中不易燃烧,在氧气中经点燃可燃烧_______________________( )
(4)在催化剂作用下能生成水和一种供呼吸的气体_____________________( )
29.下列各组物质,每组中均有一种与其他物质类别不同,请在横线上填写这种物质的名称:
(1)食醋、牛奶、加碘盐、水_________;
(2)二氧化碳、氧气、过氧化氢、二氧化硫_________;
(3)铜、铁、碳、铝_________。
30.判断下列关于化学反应的说法是否正确,在正确说法后的横线上画“√”,在错误说法后的横线上用表达式举出一个否定的例子:
(1)分解反应的反应物仅有一种物质。___________________________
(2)氧化反应一定属于化合反应。_______________________________
(3)在空气中不能燃烧的物质在氧气中也不能燃烧。_______________
31.自来水消毒过程中通常会发生化学反应,其反应的微观过程可用下图表示:
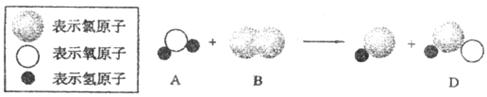
(1)请写出该反应的表达式:___________________________。
(2)A物质属于_________。(填物质分类)
(3)分析以上微观过程模拟图,你能总结出的一条结论是______________________。
三、实验探究题(共7分)
32.过氧化氢(H2O2)溶液在二氧化锰(MnO2)作催化剂的条件下能迅速分解生成氧气(O2)和水(H2O)。分液漏斗可以通过调节活塞控制液体的滴加速度。请根据下图回答下列问题:
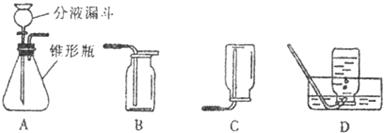
(1)分液漏斗中应放入的物质是_________,锥形瓶中应放入的物质是_________。
(2)写出该方法制取氧气的文字表达式_________________;要收集一瓶纯净的氧气,应选择装置_________(填字母)。
(3)某同学在观察到锥形瓶内有大量气泡时,开始用B装置收集氧气,过一段时间后,用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃。其原因是__________ __________________________。
(4)若实验时用此法代替KMnO4加热制取O2,优点是_________(填编号)。
①生成物只有氧气 ②不需加热 ③需加热
(5)装置A中反应很剧烈,据此提出实验安全注意事项是_________(填编号)。
①控制液体的滴加速率 ②用体积较小的锥形瓶 ③加热反应物
四、简答题(共7分)
33.元素周期表是学习和研究化学的重要工具,下图是元素周期表的一部分。
族
周期
IA
0
1
1H
1.008
ⅡA
ⅢA
ⅣA
VA
ⅥA
ⅦA
2He
4.003
2
3Li
6.991
4Be
9.012
5B
10.81
12.01
7N
14.01
8O
16.00
19.00
10Ne
20.18
3
11Na
22.99
12Mg
24.31
13Al
26.98
14Si
28.09
15P
30.97
16S
32.02
17Cl
35.45
18Ar
39.95
(1)很多科学家对元素周期表的发现和完善做出了重大贡献,请写出其中一位科学家的名字:_________。
(2)查出碳的相对原子质量:_________,写出16号元素的元素符号:_________。
(3)表中不同种元素最本质的区别是_________(填序号)。
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
(4)利用元素周期表,人们对元素的认识进入全新的飞跃时期,近日,俄罗斯科学家宣布他们将人工合成第118号元素,则此元素的核电荷数为_________。
(5)周期表中每一个横行叫做一个周期。第三周期开头元素和靠近尾部元素的原子结构示意图分别为 ,它们的单质易发生如下图所示变化:
,它们的单质易发生如下图所示变化:

根据以上信息,可以得到的结论是___________________________________。
五、分析与计算题(共12分)
34.碘元素(化学符号为I)具有预防和治疗地方性甲状腺肿的作用,人体缺碘时易患大脖子病。为了消除碘缺乏病,我国政府规定居民的食用盐必须是加碘食盐,简称碘盐。所谓碘盐就是在食盐中加入一定的碘酸钾,下表为广东省盐业公司专营的精制碘盐包装袋上的部分说明文字。请回答下列问题:
配料表
食用盐、碘酸钾
含碘量
(20―40mg)/kg
保质期
18个月
食用方法
待食物烹调好后再放碘盐,勿长时间炖炒
储藏指南
避热、避光、密封、防潮
(1)已知碘酸钾的化学式为KIO3,试计算:
①碘酸钾的相对分子质量。 ②碘酸钾中碘元素的质量分数。
③多少克碘酸钾中含有20mg碘?
(2)由食用方法和储存方法可推测碘酸钾的化学性质之一是__________________。
(3)
①这里标明的含量是指( )
A.碘单质 B.碘元素 C.碘原子 D.碘分子
②已知一个成年人每天大约需0.15mg碘,假设这些碘主要是从碘盐中摄取的,则一个成年人每天需要食用碘盐多少克?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com