2009年商丘市高三第二次模拟考试试题
高 三 化 学
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分。考试时间为90分钟。
注意事项:
1.姓名和座号写在第5页指定位置,选择题答案填在第5页的答题栏内。
2.考试后只交第Ⅱ卷5-8页。
可能用到的相对原子质量:O=16 H=1 C=12 Fe=56 Cl=35.5 N=14
第Ⅰ卷(选择题,共48分)
一、选择题(每小题只有一个正确选项,3分×16=48分)
1.正确掌握化学用语是学好化学的基础。下列有关表述中正确的一组是
试题详情
A.C2H4和C4H8两物质中碳的质量分数相同,它们一定是同系物
试题详情
B.16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体
试题详情
C.S2-的结构示意图为: ,NH4Cl的电子式为:
,NH4Cl的电子式为: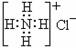
试题详情
D.SiH4、CH4、NH4+的空间构型均为正四面体型;C2H4、苯为平面型分子
试题详情
试题详情
①正常雨水的pH为7.0;酸雨的pH小于7.0
②严格执行机动车尾气排放标准有利于防止大气污染
③三大营养素糖类、油脂、蛋白质中,油脂是热能最高的营养素
④用纯碱(Na2CO3)热溶液洗涤餐具上的油污
⑤氯水使红墨水褪色原理和CH2=CH2使Br2的CCl4溶液褪色原理相同
⑥血液、烟水晶和雾都是胶体
A.①②③ B.
②④⑤⑥ C.②③④ ⑥ D.③④⑤
试题详情
3.某无色溶液中,若加入溴水,溴水褪色,若加入NH4HCO3,固体溶解并产生刺激性气味的气体,则该溶液中可能大量存在的离子组是
A.Na+、K+、C1-、OH- B.Na+、Mg2+、S2-、C1O-
C.H+、Na+、SO42-、NO3- D.K+、Ca2+、OH-、SO32-
试题详情
4.下列条件下,两瓶气体所含的原子数一定相等的是
①同质量不同密度的CO和N2 ②同温同体积的H2和Cl2
③同体积同密度的C2H4和C3H6 ④同压同体积的N2O和CO2
A.①③ B.
①② C.
②④ D.
③④
试题详情
5.下列溶液中,不能区别SO2和CO2气体的是
①石灰水 ②H2S溶液 ③KMnO4溶液 ④溴水 ⑤酸化的Ba(NO3)2溶液
⑥品红溶液
A.①⑤ B.②③④⑤⑥ C.只有① D.①③
试题详情
6.下列说法正确的是
A.不用其他试剂无法鉴别下列四种溶液:
Na2CO3
、Al2(SO4)3、、NaCl、NaHSO4
B.可以用分液漏斗分离下列三组液态混合物:
硝基苯和水;油酸和水;乙酸乙酯和乙醇
C.熔融氢氧化钠要在耐高温的石英坩埚中
D.实验室保存少量液溴和白磷常用水封
试题详情
7.将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应:
试题详情
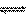 H2(g)+Br2(g)
2HBr(g);△H<0,平衡时Br2(g)的转化率为a;若初始条件
H2(g)+Br2(g)
2HBr(g);△H<0,平衡时Br2(g)的转化率为a;若初始条件
相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
A.a>b B.a=b C.a<b D.无法确定
试题详情
8.溶液中有如下反应(未配平):
FeSO4+NaClO3+H2SO4→Fe2(SO4)3+NaCl+H2O
有关叙述正确的是:
A. 当有1mol电子转移时,消耗硫酸1mol
试题详情
B. 消耗3mol Fe2+,有0.5mol ClO3―被氧化
C. 反应中氧化剂和还原剂物质的量之比为6:1
D. 若用浓HNO3 代替NaClO3,当生成等量的Fe3+时,n(HNO3)>n(NaClO3)
试题详情
9.下列判断不正确的是
试题详情
A.pH=3的盐酸溶液和pH=11的氨水溶液等体积混合后溶液显碱性
试题详情
B.pH=2的HA溶液与pH=12的MOH溶液任意比例混合后有:
试题详情
c(H+)
+ c(M+) === c(OH-)
+ c(A-)
试题详情
C.0.1mol/L的NaHA溶液其pH = 4,则c(HA-)
> c(H+) > c(H2A)
> c(A2-)
试题详情
D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后有:
试题详情
c(CH3COO-)
+ 2c(OH-) === 2c(H+) + c(CH3COOH)
试题详情
10.在硫酸铝、硫酸钾和明矾的混合溶液中,如果SO42-的离子浓度为0.2mol/L,当加入等体积0.2mol/LKOH溶液时,生成的沉淀恰好完全溶解。则反应后溶液中K+离子的浓度最接近于
试题详情
A.0.125mol•L-1
B.0.225mol•L-1 C.0.250mol•L-1 D.0.450mol•L-1
试题详情
11.下列离子方程式书写正确的是 A.在Fe(OH)3胶体中加入HI溶液:Fe(OH)3 + 3H+ == Fe3+ + 3H2O
A.在Fe(OH)3胶体中加入HI溶液:Fe(OH)3 + 3H+ == Fe3+ + 3H2O
试题详情
B.在稀氨水中通入少量CO2:NH3•H2O
+ CO2 == NH4+ + HCO3-
试题详情
C.向澄清石灰水中加入足量NaHCO3溶液: Ca2+ + OH- + HCO3-
== CaCO3↓+ H2O
Ca2+ + OH- + HCO3-
== CaCO3↓+ H2O
试题详情
D.在酸性KMnO4溶液中加入H2O2: 2MnO4- + 5H2O2 + 6H+ == 2Mn2+
+ 5O2↑+ 8H2O
2MnO4- + 5H2O2 + 6H+ == 2Mn2+
+ 5O2↑+ 8H2O
试题详情
12.在120℃时,将2LH2O、1LN2、1LCO、1LO2和2LCO2组成的混合气体依次缓缓通过过量的热铜粉,过量过氧化钠和过量炽热木炭粉的三个反应管。经充分反应后,恢复到原来温度和压强。其气体体积是
试题详情
试题详情
13.A、B、C为三种短周期元素,A、B在同周期,A、C的最低价阴离子分别为A2-、C-,B2+和C-具有相同的电子层结构。下列说法正确的是
A.原子序数C>A>B B.原子半径B>A>C
C.离子半径C->B2+>A2- D.原子核外最外层电子数B>A>C
试题详情
14.在含有ngHNO3的稀溶液中,投入5.6g铁粉恰好完全溶解,若有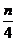 gHNO3被还原成NO(无其他还原产物),则n的值不可能是
gHNO3被还原成NO(无其他还原产物),则n的值不可能是
试题详情
A.12.6 B.16.8 C.18.9 D.25.2
试题详情
15.类比是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观事实。下列各种类比推测的说法中正确的是
试题详情
①已知Fe与S能直接化合生成FeS,推测Cu与S可直接化合生成CuS
试题详情
②已知CaCO3与稀硝酸反应生成CO2,推测CaSO3与稀硝酸反应生成SO2
试题详情
③已知CO2分子是直线型结构,推测CS2分子也是直线型结构
试题详情
④已知Fe与CuSO4溶液反应,推测Fe与AgNO3溶液也能反应
试题详情
⑤已知NaOH是强电解质,其饱和溶液导电能力很强,Ca(OH)2也是强电解质,推测其饱和溶液导电能力也很强
试题详情
A.①③④ B.①②⑤ C.③④ D.③④⑤
试题详情
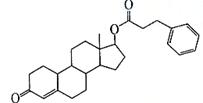 16.苯丙酸诺龙是一种兴奋剂,结构简式为:
16.苯丙酸诺龙是一种兴奋剂,结构简式为:
有关该物质的说法正确的是
A.其分子式为C27H32O3
B.最多可与6 mol H2发生加成反应
C.能使溴的四氯化碳溶液褪色
D.在NaOH 溶液中水解后可生成两种盐
2009年商丘市高三第二次模拟考试
|
座号 高 三 化 学 题号 一 二 三 四 五 总分 得分 合分人(签名) 登分人(签名)_____________
|
得分 评卷人 题 号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 答 案 第Ⅱ卷 (非选择题,共52分)
|
得分 评卷人
试题详情
二.(本题包括1小题,共14分) 17.(4分)Ⅰ.下列六种晶体:A.水晶,B.冰醋酸,C.氢氧化钠,D.白磷, E.晶体氩,F.金刚石。用序号回答下列问题: ⑴直接由原子构成的晶体是____________________________; ⑵受热熔化过程中不存在化学键变化的是_____________________________, 需克服共价键的是_________________________。 ⑶晶体A、B、C、E、F熔点由高到低的排列顺序为____________________________。 Ⅱ.(10分) 置换、化合、复分解是三种基本反应类型,而H2O在各种化学反应中扮演不同的“角色”。下面围绕水的各反应全部来自现行教材。下列问题所涉及的答案可能有多种,只需答出一种情况即可: ⑴H2O作反应物的置换反应 ①________________________(填化学式)和H2O能在加热或高温条件下进行; ②产生O2的反应,其化学方程式:______________________________________; ⑵H2O作生成物的置换反应: 加热条件下的置换,其反应物可是_____________________________(填化学式); ⑶水解反应 ① 气体产物可用于焊接金属,其化学方程式: ______________________________________________________________; ②1分子的_____________________(填名称)水解之后有2分子同种物质生成; ⑷H2O作反应物的化合反应: ① 有含碱金属元素的物质参与的三种物质间的化合反应,其化学方程式: ______________________________________________________________; ② 有电子得失且三种物质参与的化合反应,其产物的颜色与状态是 试题详情
_____________________________。
|
得分 评卷人
试题详情
三、(本题包括2小题,本题共20分) 18.(10分)短周期元素A、B、C、D原子序数依次增大,且只有C为金属元素。A、C位于同一主族,B的最外层电子数是次外层的3倍,B、C的最外层电子数之和与D的最外层电子数相等。 ⑴D的最高价氧化物对应水化物的名称为______________________________; ⑵C2B2中含有的化学键类型为________________________________________; ⑶由上述四种元素中的三种组成的某种盐,水溶液显碱性,是家用消毒剂的主要成分。将该盐溶液滴入Kl淀粉溶液中,溶液变为蓝色,则反应的离子方程式为 _______________________________________________________________________; ⑷用石墨电极电解化合物CD的饱和溶液,阴极的电极反应式为: ______________________________________________________; 若反应后溶液的体积为200mL,测得pH为13,则阳极得到的气体质量为_______; ⑸1 g A的气态单质与B的气态单质反应生成气态A2B时放出Q kJ热量,该反应的热化学方程式为_________________________________________________________。 试题详情
 19.(10分)下图表示某典型金属单质A与其化合物之间的转化关系(某些产物和反应条件已略去)。已知:图中所示物质中的组成元素均为短周期元素,化合物C中含有两种金属元素,反应⑤用于工业制取A,反应⑥的产物过滤后得到化合物D的溶液呈碱性。 19.(10分)下图表示某典型金属单质A与其化合物之间的转化关系(某些产物和反应条件已略去)。已知:图中所示物质中的组成元素均为短周期元素,化合物C中含有两种金属元素,反应⑤用于工业制取A,反应⑥的产物过滤后得到化合物D的溶液呈碱性。
(1)一步实现图中①至⑥的转化关系中一定属于复分解反应的是________ (填序号)。 (2)写出一步实现反应④所需加入的化学试剂(填化学式);___________________。 (3)写出反应①的离子反应方程式:________________________________________。 (4)B→C的转化有多种途径,试写出其中两种不同反应类型的化学反应方程式: _________________________________________________________________; _________________________________________________________________。
|
得分 评卷人
试题详情
四.(本题包括1小题,共9分) 20.(9分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。(由实验装置引起的实验误差忽略不计)。 试题详情

Ⅰ.探究浓硫酸的某些性质 (1)称量E的质量;按照图示连接装置,检查装置的气密性。简述检验发生装置气密性的方法__________________________________________________________ ___________________________________________________________________。 (2)将m g铁碳合金样品放入A中,再加入适量的浓硫酸。仪器A的名称为______。未点燃酒精灯前,A、B均无明显现象,其原因是:________________________ ____________________________________________________________________。 (3)点燃酒精灯一段时间后,A、B中可观察到明显的现象。 写出A中碳发生反应的化学方程式______________________________________。 B中的现象是 。 (4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式 (只写一个)_________________________________________________________。 (5)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是______________________________________________________。 Ⅱ.测定铁的质量分数 (6)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。铁碳合金中铁的质量分数为________________________________________(写表达式), (7)某同学认为上述方法较复杂,使用右图所示的装置和其他常用实验仪器测定某些数据即可。为了快速准确的计算出铁的质 试题详情
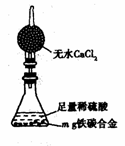 量分数,最简便的实验操作是 (填写序号)。 量分数,最简便的实验操作是 (填写序号)。
A.用排水法测定H2的体积 B.反应结束后,过滤、洗涤、干燥、称量残渣的质量 C.测定反应前后装置和药品的总质量
|
得分 评卷人 五.(本题包括1小题,共9分)
试题详情
21.(9分)已知醛在一定条件下可以发生如下转化: 试题详情
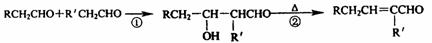
物质B是一种可以作为药物的芳香族化合物,请根据下图(所有无机产物均已略去)中各有机物的转变关系回答问题: 试题详情
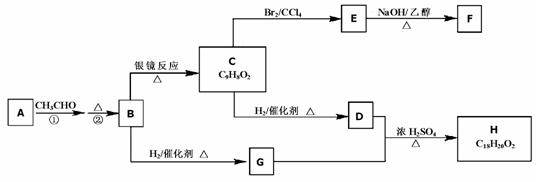
(图中C为:C9H8O2;H为:C18H20O2) (1)A分子所含官能团为:_______________,B的结构简式为:_______________; (2)E→F的反应类型是 _________________________________(填序号)。 a. 还原反应 b. 加成反应
c. 取代反应 d. 消去反应 (3)G、D反应生成H的化学方程式是: ______________________________________________________________________。 (4)G有多种同分异构体,其中能与金属钠反应且苯环上只有一个取代基的同分异构体的结构简式为:(不包括G本身) _________________________________________________________________ _________________________________________________________________。 2009年商丘市高三第二次模拟考试 试题详情
一.
选择题:(3分×16=48分) 题 号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 答 案 D C A A C D A D C B D D B A C C 二.(本题共14分) 17:Ⅰ.(4分,每空1分)(1)AEF;(2)BDE ;AF;(3)F>A>C>B>E。 Ⅱ.(10分)本题答案有开放性,合理即可给分。 ⑴①C(或Fe) (1分) ②2F2+2H2O=4HF+O2 ; (2分) ⑵CuO(Fe2O3等)(1分) ⑶①CaC2+2H2O=Ca(OH)2+C2H2↑ ;(2分)
②麦芽糖;(1分) ⑷①Na2CO3+CO2+H2O=2NaHCO3 ;(2分) ②红褐色固体。(1分) 三.(本题共20分) 18.(10分)(1)高氯酸 (1分) (2)离子键和非极性键 (1分) (3)2I-+ClO-+H2O=I2+Cl-+2OH- (2分) (4)2H++2e- = H2↑ (2分)
0.71g (2分) (5)2H2(g)+O2(g)=2H2O(g) ΔH=-4QkJ/mol (2分) 19.(10分) (1)③④⑥(2分) (2)Ca(OH)2
或 Ba(OH)2(2分) (3)2Na + 2H2O
= 2Na++ 2OH- + H2↑(2分) (4)氧化还原:2Al +
2NaOH + 2H2O = 2NaAlO2 + 3H2↑ (2分) 非氧化还原:AlCl3
+ 4NaOH = NaAlO2 +3NaCl +2H2O (2分) 或Al(OH)3 +
NaOH = NaAlO2 + 2H2O
或Al2O3
+ 2NaOH = 2NaAlO2 + H2O (其它合理答案酌情给分) 四. (本题共9分)
(每空1分) 20.Ⅰ(1)关闭分液漏斗的活塞,在B中加水至浸没长导管口,用酒精灯微热(或用手热),长导管口有气泡冒出,停止加热,长导管内形成一段水柱,说明装置的气密性良好。 (2)圆底烧瓶; 常温下,Fe在浓硫酸中钝化,碳不与浓硫酸反应 (3)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O; 品红溶液逐渐褪色 CO2↑+2SO2↑+2H2O; 品红溶液逐渐褪色 (4)2Fe3++Fe=3Fe2+(或Fe+2H+=Fe2++H2↑) (5)铁碳在酸溶液中形成原电池 Ⅱ(6) (7)C (7)C 五.(本题共9分) 21.
| | | | | | | | | | | | | | | | | |




 ,NH4Cl的电子式为:
,NH4Cl的电子式为: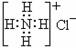

 H2(g)+Br2(g)
2HBr(g);△H<0,平衡时Br2(g)的转化率为a;若初始条件
H2(g)+Br2(g)
2HBr(g);△H<0,平衡时Br2(g)的转化率为a;若初始条件








 A.在Fe(OH)3胶体中加入HI溶液:Fe(OH)3 + 3H+ == Fe3+ + 3H2O
A.在Fe(OH)3胶体中加入HI溶液:Fe(OH)3 + 3H+ == Fe3+ + 3H2O

 Ca2+ + OH- + HCO3-
== CaCO3↓+ H2O
Ca2+ + OH- + HCO3-
== CaCO3↓+ H2O
 2MnO4- + 5H2O2 + 6H+ == 2Mn2+
+ 5O2↑+ 8H2O
2MnO4- + 5H2O2 + 6H+ == 2Mn2+
+ 5O2↑+ 8H2O
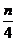 gHNO3被还原成NO(无其他还原产物),则n的值不可能是
gHNO3被还原成NO(无其他还原产物),则n的值不可能是






 16.苯丙酸诺龙是一种兴奋剂,结构简式为:
16.苯丙酸诺龙是一种兴奋剂,结构简式为: