
题目列表(包括答案和解析)
3.血糖的平衡对于保证高等动物体内各种组织和器官的能
量供应有着非常重要的意义。下图表示某高等动物体内血糖
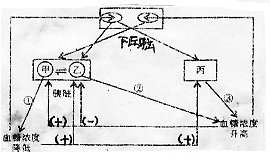
平衡的调节示意图(图中甲.乙.丙表示结构,①.②.③表
示激素;“(+)”表示促进作用,“(一)”表示抑制作用)。下列
说法中,不正确的是
A.结构甲是胰岛B细胞,结构乙是胰岛A细胞,结构丙是肾上腺
B.结构乙增加分泌激素②会抑制结构甲分泌激素①
C.结构丙分泌的激素③和结构乙分泌的激素②在调节血糖浓度方面是协同作用
D.血糖平衡的调节方式包括激素调节和神经调节
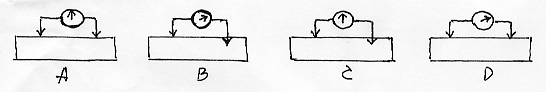
2.当神经纤维处于静息状态时,下列能正确表示并能测量出静息电位的示意图是
1.下列关于几种化学元素与光合作用关系的叙述,正确的是
A.O2是光合作用的产物,缺O2影响叶绿素的合成
B.O是组成有机物的基本元素之一,光合作用制造的有机物中的氧来自水
C.P是组成ATP的必需元素,光合作用的光反应和暗反应过程中均有ATP合成
D.C是组成糖类的基本元素,在光合作用中C元素从CO2先后经C3和C5形成(CH2O)
(二)(1)高茎和抗病 (2)甲;DdTt×ddTt (3)限制性内切酶;DNA连接酶;无氮 (4)细胞质遗传;母本在减数分裂形成卵细胞时,细胞质中的遗传物质是随机地、不均等地分配到卵细胞中的
31.(每空2分,共18分)(1)吞噬细胞;抗原决定簇
(2)核糖体、内质网、高尔基体
(3)实验过程:
第二步:在甲组体内注射生理盐水配制的R型活菌液,在乙组体内注射等量生理盐水;
第三步:一段时间后,再分别给甲、乙两组注射等量的用生理盐水配制的S型活菌液,观察两组小鼠的生活状况
实验预期:
①若甲组小鼠存活,而乙组小鼠死亡,说明抗R型细菌的抗体也能抗S型细菌(R型细菌可以作为S型细菌的疫苗);
②若甲、乙两组小鼠都死亡,说明抗R型细菌的抗体不能抗S型细菌(R型细菌不可以作为S型细菌的疫苗)
(一)(1)[⑤]组织液 (2)[③]毛细血管壁 (3)胰岛素;胰高血糖素
(二)下表是科研人员所做的三组水稻杂交实验的统计数据(D和d表示水稻株高的显、隐性基因,T和t表示抗性的显、隐性基因)。据表回答以下问题:
|
|
亲本组合 |
Fl表现型和株数 |
|||
|
组别 |
表现型 |
高茎抗病 |
高茎易染病 |
矮茎抗病 |
矮茎易染病 |
|
甲 |
高茎抗病×矮茎抗病 |
627 |
203 |
617 |
212 |
|
乙 |
高茎抗病×矮茎易染病 |
724 |
0 |
0 |
0 |
|
丙 |
高茎易染病×矮茎抗病 |
517 |
523 |
499 |
507 |
(1)上述两对性状中,显性性状是 。
(2)获得纯合矮茎抗病个体比例最大的杂交组合是 ,亲本的基因型是 。
(3)科学家设想把根瘤菌的固氮基因转移到小麦根系的微生物中,获取根瘤菌固氮的基因所用的工具酶是 ;在形成重组DNA的过程中,能使两条DNA分子末端之间的缝隙相互连接的工具酶是 。如果这一重组能够实现,欲检测固氮基因是否表达,可以将转基因小麦根系的微生物培养在 培养基上,观察其是否能够生存。
(4)水稻正常植株叶片为绿色,患遗传病后植株的叶片具有白色条斑,或为不能成活的白化苗。显微观察发现,白化苗和白色条斑处的叶肉细胞不含叶绿体。为了探索该病的遗传机理,用人工授粉的方法进行了如下实验:
|
多次重复该实验,发现后代的性状分离比每次均有较大差距,无法归纳出确定比值。分析实验结果可知该病的遗传方式是 。此实验的后代中不同性状的个体的比例是随机的,其原因是 。
31.(18分)请依据英国细菌学家格里菲思的肺炎双球菌转化实验,回答以下问题:
(1)肺炎双球菌初次进入小鼠体内后,一般先要经过 的摄取和处理,将其内部隐蔽的 暴露出来,并呈递给T细胞。
(2)小鼠体内能产生抗肺炎双球菌抗体的细胞中,与产生抗体有关的细胞器除了线粒体外还有 。
(3)有人设想抗R型细菌的抗体也可能抗S型细菌(R型细菌可以作为抗S型细菌的疫苗)。请为他设计一个实验验证这一想法:
实验目的:验证抗R型细菌的抗体是否能抗S型细菌(R型细菌可否作为S型细菌的疫苗)。
实验原理:动物体受到外界抗原性物质刺激可以产生特异性抗体,将抗原消灭。
实验材料:小鼠若干只、S型活菌、R型活菌、生理盐水、注射器等。(提示:可用生理盐水配制一定浓度的活菌液,但浓度和剂量不作要求)
实验过程:第一步:取小鼠若干只,均等地分成两组,分别命名为甲组和乙组;
第二步:
第三步:
实验预期:① 结论:
② 结论:
生物答案:
1-5 B C D B D
30.(每空2分,共24分)
14.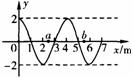 一列简谐横波沿
一列简谐横波沿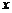 轴传播,周期
轴传播,周期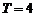 s,
s,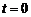 时刻的波形如图所示,此时平衡位置位于
时刻的波形如图所示,此时平衡位置位于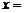 1m处的质点正在向下运动,若
1m处的质点正在向下运动,若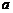 、
、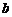 两质点平衡位置的坐标分别
两质点平衡位置的坐标分别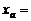 2.5m,
2.5m,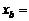 5.5m,则( )
5.5m,则( )
A.该波沿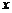 轴正向传播,波速为1m/s
轴正向传播,波速为1m/s
B.当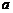 点处在波峰时,
点处在波峰时,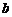 质点恰在波谷
质点恰在波谷
C.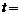 0.5s时,
0.5s时,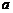 在平衡位置且正向上运动
在平衡位置且正向上运动
D.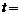 1.5s时,
1.5s时,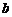 在波峰位置
在波峰位置
15.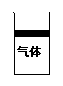 如图所示,一导热性能良好的气缸,常温下用一活塞密封一定量的气体(可看作理想气体),活塞可无摩擦上下滑动,且气体不会漏出,若外界温度突然降低,大气压保持不变,待稳定后,下列说法正确的是( )
如图所示,一导热性能良好的气缸,常温下用一活塞密封一定量的气体(可看作理想气体),活塞可无摩擦上下滑动,且气体不会漏出,若外界温度突然降低,大气压保持不变,待稳定后,下列说法正确的是( )
A.外界对气体做功,气体内能增加
B.外界对气体做功,气体内能减小
C.气体分子单位时间内与单位面积器壁碰撞次数减少
D.气体分子单位时间内与单位面积器壁碰撞次数增加
16.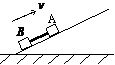 如图所示,滑块
如图所示,滑块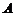 、
、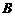 用轻杆相连,以某速度一起靠惯性冲上一固定斜面,在沿斜面上滑过程中,下列说法正确的是( )
用轻杆相连,以某速度一起靠惯性冲上一固定斜面,在沿斜面上滑过程中,下列说法正确的是( )
A.若斜面光滑,杆可能被压缩
B.若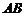 与斜面间滑动摩擦因数相同(不为零),杆一定被压缩
与斜面间滑动摩擦因数相同(不为零),杆一定被压缩
C.若斜面光滑或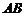 与斜面间滑动摩擦因数相同时,杆对
与斜面间滑动摩擦因数相同时,杆对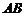 都无作用力
都无作用力
D.因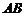 质量关系未知,所以杆上有无弹力无法确定
质量关系未知,所以杆上有无弹力无法确定
17.如图所示,实线为未标明方向的电场线,虚线为一电子在该电场中只受电场力作用的运动轨迹,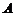 、
、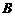 为轨迹上两点,则下列说法正确的是( )
为轨迹上两点,则下列说法正确的是( )
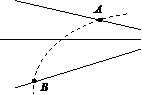 A.电子在
A.电子在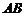 加速度关系
加速度关系 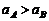
B.电子在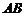 速度关系
速度关系 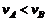
C.电子在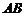 电势能关系
电势能关系 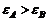
D.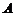 、
、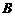 电势关系
电势关系 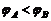
18.“滤速器”装置的示意图如下,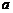 、
、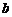 为水平放置的平行金属板,一束具有各种不同速率的电子沿水平方向经小孔
为水平放置的平行金属板,一束具有各种不同速率的电子沿水平方向经小孔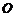 进入
进入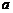 、
、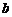 两极板之间,为了选取具有某种特定速率的电子,可在
两极板之间,为了选取具有某种特定速率的电子,可在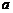 、
、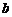 间加上电压,并沿垂直于纸面的方向加一匀强磁场,使所选电子仍能够沿水平直线
间加上电压,并沿垂直于纸面的方向加一匀强磁场,使所选电子仍能够沿水平直线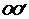 运动,由
运动,由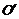 射出,不计重力作用,可能达到上述目的的办法是( )
射出,不计重力作用,可能达到上述目的的办法是( )
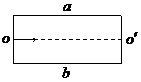 A.使
A.使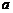 板电势高于
板电势高于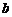 板,磁场方向垂直纸面向里
板,磁场方向垂直纸面向里
B.使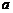 板电势低于
板电势低于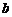 板,磁场方向垂直纸面向里
板,磁场方向垂直纸面向里
C.使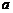 板电势高于
板电势高于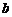 板,磁场方向垂直纸面向外
板,磁场方向垂直纸面向外
D.使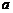 板电势低于
板电势低于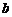 板,磁场方向垂直纸面向外
板,磁场方向垂直纸面向外
19.在如图所示的电路中,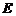 为电源电动势,
为电源电动势,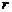 为电源内阻,
为电源内阻,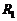 和
和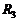 均为定值电阻,
均为定值电阻,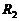 为滑动变阻器。当
为滑动变阻器。当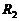 的滑动触点在
的滑动触点在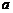 端时合上开关
端时合上开关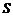 ,此时三个电表A1、A2和V的示数分别为
,此时三个电表A1、A2和V的示数分别为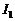 、
、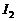 和
和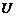 ,现将
,现将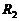 的滑动触点向
的滑动触点向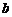 端移动,则三个电表示数的变化情况是( )
端移动,则三个电表示数的变化情况是( )
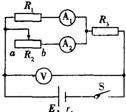 A.
A.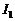 增大,
增大,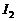 不变,
不变,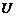 增大
增大
B.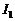 减小,
减小,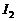 增大,
增大,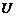 减小
减小
C.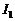 增大,
增大,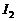 减小,
减小,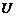 增大
增大
D.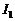 减小,
减小,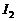 不变,
不变,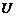 减小
减小
20.据媒体报道,嫦娥一号卫星环月工作轨道为圆轨道,轨道高度200km,运动周期127分钟,若还知道引力常量和月球平均半径,不计地球引力对卫星影响,仅利用以上条件能求出的是( )
A.月球表面的重力加速度 B.月球对卫星的吸引力
C.月球的质量 D.月球绕地球公转周期
21.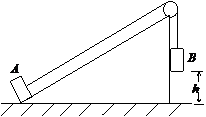 如图所示,完全相同的小滑块用轻绳穿过定滑轮相连。
如图所示,完全相同的小滑块用轻绳穿过定滑轮相连。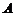 开始静止在足够长固定斜面底端,
开始静止在足够长固定斜面底端,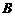 用手拖住,离地面高为
用手拖住,离地面高为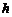 ,绳刚好被拉紧,不计一切摩擦,斜面倾角为30°,由静止释放
,绳刚好被拉紧,不计一切摩擦,斜面倾角为30°,由静止释放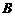 后,且
后,且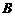 与地面碰撞不反弹,则
与地面碰撞不反弹,则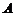 可能达到的最大高度为( )
可能达到的最大高度为( )
A.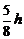 B.
B.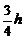 C.
C.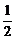
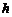 D.
D. 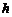
第Ⅱ卷 非选择题
本卷共10题,共174分
22.(18分)
(1)(6分)某同学练习使用50分度的游标卡尺和螺旋测微器,其测量刻度如图所示,则游标卡尺读数为 cm,螺旋测微器读数为 mm。
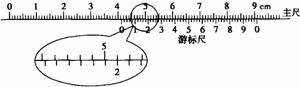
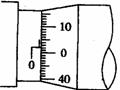
(2)(12分)在用伏安法测定电阻值约为4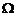 的金属丝的电阻时,除被测电阻丝外,还有如下实验器材供选择:
的金属丝的电阻时,除被测电阻丝外,还有如下实验器材供选择:
A.直流电源:电动势约4.5V,内阻很小
B.电流表A1:量程0-0.6A,内阻约为0.125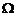
C.电流表A2:量程0-3.0A,内阻约为0.025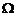
D.电压表V1:量程0-3V,内阻约为3k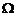
E.电压表V2:量程0-15V,内阻约为15k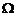
F.滑动变阻器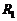 :最大阻值20
:最大阻值20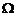
G.滑动变阻器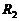 :最大阻值50
:最大阻值50
H.开关、导线若干
为了提高实验的测量精度和仪器操作的方便,在可供选择的器材中,应该选用的电流表是 ,电压表是 ,滑动变阻器是 (填仪器的字母代号)。
(3)根据所选的器材,用铅笔在图示的虚线方框中画出完整的实验电路图。

23. (16分)利用皮带运送石料是现在矿场常用的自动化运载设备,其示意图如下,石料由
(16分)利用皮带运送石料是现在矿场常用的自动化运载设备,其示意图如下,石料由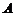 端静止释放,达
端静止释放,达 端水平飞出,恰落在装载车车厢内。今测得水平部分
端水平飞出,恰落在装载车车厢内。今测得水平部分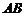 段长
段长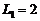 m,倾斜部分
m,倾斜部分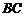 段长
段长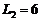 m,
m,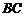 与水平面夹角30°,石料与
与水平面夹角30°,石料与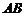 、
、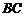 段动摩擦因数分别为
段动摩擦因数分别为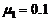 ,
,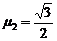 ,滑轮大小影响不计,忽略石料达
,滑轮大小影响不计,忽略石料达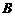 处速度大小的变化,传送带以
处速度大小的变化,传送带以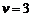 m/s速度运转过程。
m/s速度运转过程。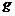 取10m/s2。求:
取10m/s2。求:
(1)石料达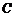 端处的速度
端处的速度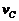 ?
?
(2)运载车车厢距地面高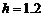 m,则运载车厢中心距
m,则运载车厢中心距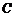 端水平距离
端水平距离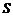 为多少?
为多少?
24.(18分)竖直平面内的轨道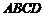 由水平滑道
由水平滑道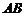 与光滑的四分之一圆弧滑道
与光滑的四分之一圆弧滑道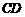 组成,
组成,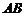 恰与
恰与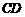 在
在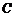 点相切,轨道放在光滑的水平面上,如图,一个质量为
点相切,轨道放在光滑的水平面上,如图,一个质量为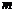 的小物块(可视为质点)从轨道
的小物块(可视为质点)从轨道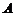 端以初动能
端以初动能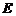 冲上水平滑道
冲上水平滑道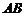 沿轨道运动,由
沿轨道运动,由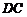 弧滑下后停在水平滑道
弧滑下后停在水平滑道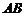 的中点。已知水平滑道
的中点。已知水平滑道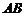 长为
长为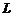 ,轨道
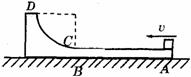
,轨道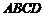 的质量为3
的质量为3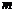 。求:
。求:
 (1)小物块在水平滑道上受到的摩擦力大小。
(1)小物块在水平滑道上受到的摩擦力大小。
(2)为了保证小物块不从滑道的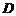 端离开滑道,圆弧滑道的半径
端离开滑道,圆弧滑道的半径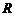 至少是多大?
至少是多大?
25.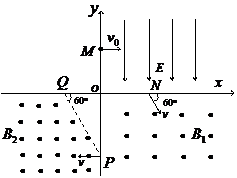 (20分)在平面直角坐标系
(20分)在平面直角坐标系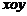 中,第Ⅰ象限存在沿
中,第Ⅰ象限存在沿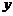 轴负方向的匀强电场,第Ⅲ、Ⅳ象限存在有理想边界垂直纸面向外的匀强磁场,第Ⅳ象限磁场磁感应强度
轴负方向的匀强电场,第Ⅲ、Ⅳ象限存在有理想边界垂直纸面向外的匀强磁场,第Ⅳ象限磁场磁感应强度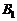 ,第Ⅲ象限磁场边界
,第Ⅲ象限磁场边界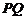 与
与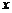 轴夹角60°,如图所示。一质量为
轴夹角60°,如图所示。一质量为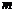 ,电荷量为
,电荷量为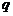 的带正电的粒子从
的带正电的粒子从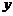 轴正半轴上的
轴正半轴上的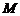 点以速度
点以速度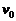 垂直于
垂直于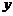 轴射入电场,经
轴射入电场,经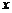 轴上的
轴上的 点与
点与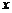 轴正方向成60°角射入第Ⅳ象限,恰沿
轴正方向成60°角射入第Ⅳ象限,恰沿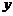 轴负半轴上
轴负半轴上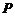 点垂直于
点垂直于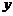 轴进入第三象限,最后经坐标原点
轴进入第三象限,最后经坐标原点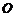 又进入第一象限,不计粒子重力。求:
又进入第一象限,不计粒子重力。求:
(1)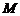 、
、 两点间的电势差
两点间的电势差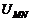 ;
;
(2)粒子由 点到
点到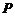 点的时间;
点的时间;
(3)第Ⅲ象限磁场磁感应强度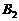 。
。
26.(16分)下表由元素周期表的前三周期去掉副族上方的空白区域后组合而成,表中虚线处为ⅡA、ⅢA族的连接处。请用相应的化学用语回答下列问题:
|
a |
|
|
|
|
|
|
|
|
b |
 |
 |
c |
d |
e |
f |
|
|
g |
|
h |
|
|
|
|
|
(1)写出仅由e形成的两种带有相同电荷数的阴离子的符号: 、 。
(2)h的单质能与g元素的最高价氧化物对应的水化物的溶液反应,请写出该反应的离子方程式 。
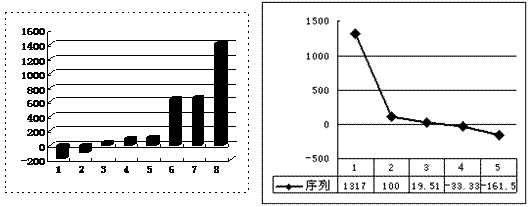
(3)上左图是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则其中柱形“8”代表 。(填化学式)
(4)b、c、d、e、f的氢化物的沸点(℃)直角坐标图(上右图),序列“5”的氢化物的名称是 ,序列“2”的氢化物的结构式为 。
(5)单质a和单质e可以设计为新型燃料电池,电解质为KOH溶液,则单质a在该
燃料电池的______极发生电极反应,电极反应式为 。
27.I.(8分)对于反应2A+B 2C的反应过程中C的百分含量随温度变化如图10-6所示,则:
2C的反应过程中C的百分含量随温度变化如图10-6所示,则:
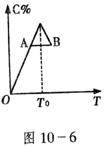
(1)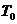 对应的v(正)与v(逆)的关系是_____________________________。
对应的v(正)与v(逆)的关系是_____________________________。
(2)正反应为____________________热反应。
(3)A、B两点正反应速率的大小关系是________________________。
(4)温度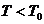 时,C%逐渐增大的原因是__________________________。
时,C%逐渐增大的原因是__________________________。
II.(9分)有一种pH为12的NaOH溶液100 mL,要使它的pH降到11,
(1)如果加入蒸馏水,应加____________mL;(溶液总体积允许相加。下同)
(2)如果加入pH=10的NaOH溶液,应加______________mL;
(3)如果加入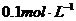 的盐酸,应加__________________mL。
的盐酸,应加__________________mL。
28.(15分)有一透明溶液,已知其中可能含有Mg2+、Cu2+、Fe2+、Al3+、NH4+、K+、SO42-、HCO3-。当加入一种淡黄色粉末状固体物质时,有刺激性气味的混合气体放出,同时生成白色沉淀。当加入0.4mol淡黄色粉末时,共收集到0.3mol混合气体,且此时生成的沉淀最多。此后继续加入淡黄色粉末时,沉淀量逐渐减少,至加入0.45mol粉末后,沉淀量由0.3mol减少至0.2mol,再加入粉末后,沉淀就不再减少。由此实验现象及数据判断:
(1)淡黄色粉末的名称为 ;
(2)溶液中肯定有 离子,肯定没有 离子,可能有________离子;
(3)加入淡黄色粉末的物质的量由0.4mol至0.45mol时,沉淀部分消失,反应的离子方程式为 ;
(4)溶液中阳离子的物质的量之比为(H+及没有确定的离子除外) 。
29.(12分)“铝和氯化铜溶液反应”实验中预料之外现象的研究
化学实验中预料之外的现象往往包含我们还没有认识的事物规律。下面是某同学进行“铝和氯化铜溶液反应”实验时观察到的预料之外的现象:
①铝丝表面附上的铜没有紧密吸附在铝丝的表面而是呈蓬松的海绵状;②反应一段时间后有大量气泡逸出,且在一段时间内气泡越来越快,经点燃能发出爆鸣声,证明是氢气。
“科学研究还离不开合理的猜想和假设。”该同学先从理论上猜想铝丝表面产生氢气的多种可能原因,再设计实验验证自己的猜想。
实验操作及现象记录:
取4根去油去锈的铝丝为A组直接和下列溶液反应,4根下半截缠上细铜丝的铝丝为B组和下列溶液反应,再取前面实验中得到的附有海绵状铜的4根铝丝洗净后作为C组和下列溶液反应作比较,实验现象记录如下:
|
|
热水 |
硫酸铜溶液(2.0mol/L) |
氯化铝热溶液(2.0mol/L) |
饱和氯化钠 热溶液 |
|
A |
只在开始时 有少量气泡 |
气泡较多,但比同浓度的氯化铜溶液少 |
有气泡, 比热水多 |
气泡比热水稍多,但比氯化铝溶液少 |
|
B |
气泡比相应A多 |
气泡比相应A多 |
气泡比相应A多 |
气泡比相应A多 |
|
C |
气泡比相应B多 |
气泡比相应B多 |
气泡比相应B多 |
气泡比相应B多 |
 实验现象说明氢气的生成原因是多种因素作用的结果。试推测该同学原来的猜想有哪些(不一定填满,不够也可以自己添加):
实验现象说明氢气的生成原因是多种因素作用的结果。试推测该同学原来的猜想有哪些(不一定填满,不够也可以自己添加):
(1)反应生成的铜和铝组成原电池促进铝和水反应;
(2) ;
(3) ;
(4) ;
(5) 。
30.(24分)(一)右图为人体局部组织示意图,据图回答有关问题:(在“[]”中填标号,在“ ”上填文字)
(1)若某人长期营养不良,血浆中蛋白质降低,会引起图中[ ] 部分的液体增多。
(2)在发生过敏反应时[ ] 通透性会增强。
(3)如果该图为胰岛的局部组织,一名健康的成年人摄取大量的葡萄糖,1h后,比较B端的液体与A端的液体中,含量会明显增加的激素是 ;与此激素有拮抗作用,且由胰岛分泌的激素是 。
13.用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的
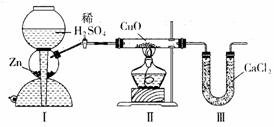 质量差和U形管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是(
)
质量差和U形管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是(
)
A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝
D.CuO没有全部被还原
12.检验溶液中是否含有某种离子,下列操作及判断正确的是( )
A.加入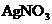 溶液,有白色沉淀生成,证明有
溶液,有白色沉淀生成,证明有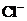
B.加入BaCl2溶液,析出白色沉淀,加过量HNO3溶液,沉淀不消失,证明含有SO42-
C.加浓NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝的气体,证明含有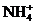
D.加入盐酸,放出使澄清石灰水变浑浊的气体,证明含有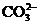
11.下列离子方程式书写正确的是 ( )
A.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2+ + OH- + H+ + SO42- == BaSO4↓+ H2O
B.将过量的NaOH溶液滴入同浓度的少量Ca(HCO3)2溶液
Ca2+ + 2HCO3-+2OH-====CaCO3↓+ 2H2O + CO32-
C.醋酸钡溶液和硫酸反应:Ba2++SO42-== BaSO4↓
D.向酸性FeSO4溶液中加H2O2溶液:
2Fe2+ + 2H2O2 + 4H+ ==2Fe3+ + 4H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com