
题目列表(包括答案和解析)
1.赫尔希和蔡斯分别用35S和32P标记T2噬菌体的蛋白质和DNA分子,下列被标记的部位组合正确的是
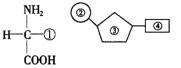
A.①② B.①③
C.①④ D.②④
(可能用到的相对原子质量:H-1,O-16,N-14,S-32)
31.(20分)为探究0.1mg/L的萘乙酸(生长素类似物之一)对种子萌发的影响,某生物兴趣小组要进行实验研究。若你是其中一员,请你根据下面提供的实验材料和用具完成实验方案的设计,并预测可能的实验结果。
材料用具:干燥的萝卜种子若干,小烧杯2个,垫有滤纸的培养皿2个,0.1mg/L的萘乙酸溶液,蒸馏水,量筒。
(1)实验假设: 。
(2)方法步骤:
第一步: 。
第二步:在两个小烧杯中各放入若干粒干燥的萝卜种子,浸泡24h。
第三步:取2个垫有滤纸的培养皿,
,然后,盖上培养皿盖,放在22℃恒温箱中培养。
第四步:一周后, 。
(3)预测可能的实验结果:
① ;
② ;
③ 。
(4)方法步骤的第三步中“盖上培养皿盖”的目的是 ;
。
(5)若该浓度萘乙酸对萝卜种子萌发有促进作用,要进一步探索萘乙酸促进种子萌发的最适浓度,应该对上述实验方案中的方法步骤做哪些主要补充。
。
30、(22分)I.(16分)石刁柏(嫩茎俗称芦笋)是一种名贵蔬菜.为XY型性别决定的雌、雄异株植物。野生型石刁柏叶窄,产量低,在某野生种群中,发现生长着少数几株阔叶石刁柏(突变型),雌株、雄株均有,雄株的产量高于雌株。
(1)要大面积扩大种植突变型石刁柏,可用 方法来大量繁殖。有人认为阔叶突变型植株是由于基因突变或具有多倍体特点的缘故。请设计一个简单实验来直接鉴定突变型的出现是基因突变还是染色体组加倍所致?
(2)若已证实阔叶为基因突变所致,有两种可能:一是显性突变,二是隐性突变,请设计一个简单实验方案加以判定。(要求写出杂交组合,杂交结果,得出结论)
(3)若已证实阔叶为显性突变所致,突变基因可能位于常染色体上,也可能位于x染色体上。请设计一个简单实验方案加以判定。(要求写出杂合组合,杂交结果,得出结论)
(4)若野生石刁柏种群在历经数百年后,窄叶基因频率由98%变为10%,则石刁柏是否已发生了进化,为什么?
(II) (6分)油菜细胞代谢产生的中间代谢产物磷酸烯醇式丙酮酸(PEP)运向种子后有两条转变途径,如图甲所示,其中酶a和酶b分别由基因A和基因B控制合成。研究人员根据这一机制培育出了产油率由原来的35%提高到58%的油菜新品种。
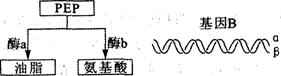
(1)在基因B中,α链是模板链,转录出α’ 链,研究人员通过一定方法使新品种中的β链也能转录,形成β’链,a’和β’形成双链mRNA,从而提高了油菜产油率。为什么基因β转录出双链mRNA就能提高油脂产量?
(2)上述过程说明,基因控制性状的途径之一是:
29.(本题包括A、B两题,共16分)
A.(8分)有机物A和B无论以何种比例混合,其组成的混合物中所含原子的核外电子总数均不变,若A是分子中含8个氢原子的烃,B是分子中含3个碳原子的烃的含氧衍生物,试回答下列问题:
(1)若相对分子质量之差为2,试写出两组符合上述条件的A、B的组合的分子式。
①A: B:
②A: B:
(2)若相对分子质量相等,试写出一组符合题干条件的A、B的组合的结构简式。
A: B:
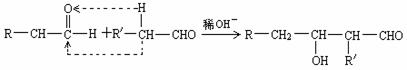 B.(8分)已知适宜的条件下,醛分子间可按下式发生反应:
B.(8分)已知适宜的条件下,醛分子间可按下式发生反应:
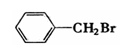
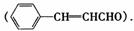
试用化学方程式表示以乙醛、 为主要原料制备肉桂醛
(其它无机原料自选)并指出各反应类型:
①
②
③
④ 。
28.(12分)某化学兴趣小组探究铜跟浓硫酸的反应情况:
取6.4g铜片和10ml 18mol/L浓硫酸放在圆底烧瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余,同时他们根据所学的化学知识认为还有较多的硫酸剩余。
(1)请写出铜跟浓硫酸反应的化学方程式 。
(2)可以证明有余酸的实验方案可以是 。(填写字母编号,多选扣分)
A.再加入足量镁粉 B.再滴入足量BaCl2溶液
C.再加入足量银粉 D.再滴入足量Na2CO3溶液
(3)可以证明有余酸的实验方案还可以是:测定反应后混合溶液中Cu2+的量。将反应后的溶液用蒸馏水稀释至100mL,加入足量Na2S溶液,充分反应,过滤出沉淀,洗涤,干燥,称量为A克。写出生成沉淀的离子反应方程式 。如果在反应后的溶液中直接加入足量Na2S溶液,充分反应后,过滤出沉淀,洗涤,干燥,称量为B克,则B可能 A(填“>”、“<”或“=”),用化学方程式说明原因 。
(4)上述实验方案中,能够计算余酸浓度的数据除测算产生气体的物质的量或反应掉铜的物质的量外,尚缺少的测量数据是 。
27.(14分)A-N均为中学化学中的常见物质,其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料,单质M是目前使用量最大的金属,常温下B、E、F为气体,G为无色液体,这些物质在一定条件下存在如下转化关系,其中有些反应物或生成物已经略去。回答下列问题:
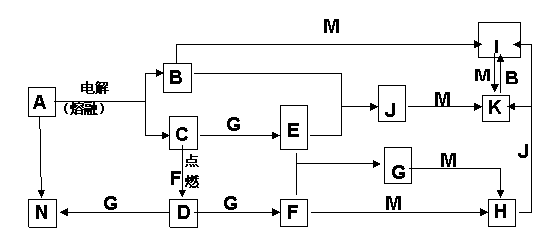
(1) H的化学式为__________ ,D的电子式 ______________________
(2)B与N反应的离子方程式为__________________________________。
(3)D与G反应的化学方程式为__________________________________。
(4)I可用于净化水,其原因为__________________________ _________ _______________________________________。(用相关的反应方程式和简要文字回答)。
(5)通常状况下, 1 g气体E在气体F中完全燃烧生成液态G时放出热量为a kJ,请写出表示E燃烧热的热化学方程式____________ ________________。
(6)I与NaOH溶液反应生成的沉淀再与NaOH和NaClO的混合液作用,是制备理想的绿色水处理剂(Na2MO4)的一种方法,试写出此反应的化学方程式_______________________。
26.(18分)下表由元素周期表的前三周期去掉副族上方的空白区域后组合而成,表中虚线处为ⅡA,ⅢA族的连接处。请回答下列问题:
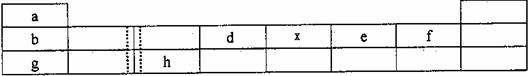
(1)写出由e形成的两种带有相同电荷数阴离子的符号: 、 。
(2)b、d、X、e、f的氢化物的沸点(℃)直角坐标图中(下图1),序列“5”的氢化物的名称是 ,序列“2”的氢化物的结构式为 。
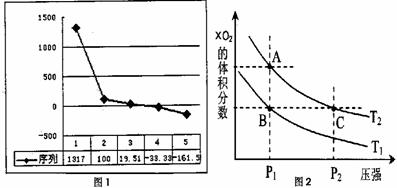
(3) X可形成多种氧化物,如XO、XO2、X2O4等。
①对反应X2O4(g) 2XO2(g);ΔH> 0,在温度为T1、T2时,平衡体系中XO2的体积分数随压强变化曲线如上右图2所示。下列说法正确的是
2XO2(g);ΔH> 0,在温度为T1、T2时,平衡体系中XO2的体积分数随压强变化曲线如上右图2所示。下列说法正确的是
A.A、C两点的反应速率:A>C
B.B、C两点的气体的平均相对分子质量:B<C
C.A、C两点气体的颜色:A深,C浅
D.由状态B到状态A,可以用加热的方法
②在100℃时,将0.400mol的XO2气体充入2 L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
|
时间(s) |
0 |
20 |
40 |
60 |
80 |
|
n(XO2)/mol |
0.40 |
n1 |
0.26 |
n3 |
n4 |
|
n(X2O4)/mol |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
在上述条件下,n3 n4(填“>”、“<”或“=”),从反应开始直至20 s时,XO2的平均反应速率为_____mol·(L·s)-1。
③若在相同情况下最初向该容器充入的是X2O4气体,要达到上述同样的平衡状态,X2O4的起始浓度是_____________mol·L-1。
④计算③中条件下达到平衡后混合气体的平均相对分子质量:____________。(结果保留小数点后一位)。
25.(20分)如图所示,在x轴上方有水平向左的匀强电场E1, 在x轴下方有竖直向上的匀强电场E2,且E1= E2=mg/q,在x轴下方的虚线(虚线与y轴成450)右侧有垂直纸面向外的匀强磁场,磁感应强度为B.有一长为L的轻绳一端固定在第一象限内的O'点且可绕O'点在竖直平面内转动,另一端栓有一质量为m的小球,小球带电荷量为+ q,OO'间距为L与x 轴成450,先将小球放在O'正上方绳恰好伸直后静止释放,当小球进入磁场时的瞬间绳子绷断.
 求
(1) 小球刚进入磁场区域时的速度
求
(1) 小球刚进入磁场区域时的速度
(2) 小球从进入磁场到第一次打在
x轴运动的时间及此时的坐标.
24.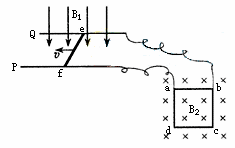 (18分)如图所示,P、Q为水平面内平行放置的金属长直导轨,间距为L1,处在磁感应强度大小为B1、方向竖直向下的匀强磁场中.一根质量为M、电阻为r的导体杆ef垂直于P、Q放在导轨上,导体杆ef与P、Q导轨之间的动摩擦因素为μ.在外力作用下导体杆ef向左做匀速直线运动.质量为m、每边电阻均为r、边长为L2的正方形金属框abcd置于竖直平面内,两顶点a、b通过细导线与导轨相连,金属框处在磁感应强度大小为B2、方向垂直框面向里的匀强磁场中,金属框恰好处于静止状态.不计其余电阻和细导线对a、b点的作用力.求:
(18分)如图所示,P、Q为水平面内平行放置的金属长直导轨,间距为L1,处在磁感应强度大小为B1、方向竖直向下的匀强磁场中.一根质量为M、电阻为r的导体杆ef垂直于P、Q放在导轨上,导体杆ef与P、Q导轨之间的动摩擦因素为μ.在外力作用下导体杆ef向左做匀速直线运动.质量为m、每边电阻均为r、边长为L2的正方形金属框abcd置于竖直平面内,两顶点a、b通过细导线与导轨相连,金属框处在磁感应强度大小为B2、方向垂直框面向里的匀强磁场中,金属框恰好处于静止状态.不计其余电阻和细导线对a、b点的作用力.求:
(1)通过ab边的电流Iab;
(2)导体杆ef做匀速直线运动的速度v;
(3)外力做功的功率P外;
(4)t时间内,导体杆ef向左移动时克服摩擦力所做的功.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com