
题目列表(包括答案和解析)
6.下列粒子中,与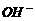 具有相同质子数和电子数的粒子是
具有相同质子数和电子数的粒子是
A. B.
B.
C. D.
D.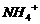
5.下列各组元素中,属于同一周期的是
A.C、O、S B.Si、P、Cl
C.Li、Na、K D.F、Cl、Br
4.下列原子结构示意图中,能正确表示 的是
的是
A.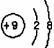 B.
B.
C. D.
D.
3.下列原子中,半径最小的是
A.F B. B.Cl
C.Br D.I
2.在 原子里具有的粒子是
原子里具有的粒子是
A.质子、中子、电子 B.质子、中子
C.质子、电子 D.中子、电子
1.据报道, (钬)具有放射性,可有效地治疗肝癌。下列关于
(钬)具有放射性,可有效地治疗肝癌。下列关于 的表述中,不正确的是
的表述中,不正确的是
A.质子数为67 B.中子数为67
C.核外电子数为67 D.质量数为166
26.喀麦隆的“杀人湖”曾于1986年使1800多名附近居民在一夜之间神秘死去,后经科学家考察发现,湖底有火山口,聚集了大量二氧化碳和二氧化硫等有毒气体,在200m深的湖底,每立方米湖水中竟溶解了8m3的有毒气体。
⑴为了测定从湖底取出的水样中SO2的含量,可在一定量的水样中加入一定量的碘(过量),再用已知浓度的硫代硫酸钠溶液与过量的碘反应,该反应为:2Na2S2O3+I2=2NaI+Na2S4O6
①碘和水样中SO2反应的化学方程式: 。
②用硫代硫酸钠与过量的碘反应时,先在水样中加1~2滴 ,当出现 (填现象),恰好完全反应。
③若在20mL水样中加入碘Wg,用去VmL C mol/L的Na2S2O3溶液,则水样中SO2的浓度为多少?(写出有关计算过程)
⑵为了测定从湖底抽出的有毒气体中CO2的含量,需将CO2变成沉淀,然后测其质量,通过计算求出CO2的含量,从下图中选择必要的装置(导管等省略)设计实验将CO2转变为沉淀。
①其所选装置的连接顺序是(按从上到下,从左到右的顺序) 。
②将气体两次通过酸性KMnO4溶液的目的是
③是否需要装置B,为什么? 。
④为了测得沉淀的质量,还需进行的操作是 ;还需要的仪器有 。
25.拟用下图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去,必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
|
气体 |
a |
b |
c |
d |
|
HCl |
浓H2SO4 |
NaCl |
NaOH溶液 |
浓H2SO4 |
|
Cl2 |
浓HCl |
KMnO4 |
饱和NaCl溶液 |
浓H2SO4 |
|
H2S |
HCl |
FeS |
饱和NaHS溶液 |
浓H2SO4 |
|
SO2 |
浓H2SO4 |
Na2SO3 |
-- |
浓H2SO4 |
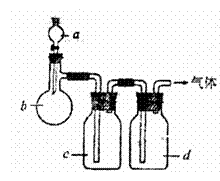 (1)上述方法中可以得到干燥、纯净的气体是
。(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)
(1)上述方法中可以得到干燥、纯净的气体是
。(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)
①气体 ,理由是 。
②气体 ,理由是 。
③气体 ,理由是 。
④气体 ,理由是 。
24.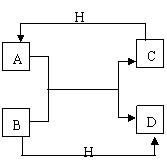


 已知A、B、C、D是中学化学常见的不同微粒。它们之间在化学反应时存在如下关系:
已知A、B、C、D是中学化学常见的不同微粒。它们之间在化学反应时存在如下关系:
⑴ 如果A、B、C、D均是10电子的微粒,且A不是双
原子分子,请写出:
A的结构式 ;D的电子式
⑵ 如果A、B、C、D均是10电子的微粒,且A是双原
子分子,则C为 ;A与B在溶液中反应的
离子方程式: 。
⑶ 如果A、C是18电子的微粒,B、D均是10电子的微粒,
则A是 ,B是 ,A、B反应的离子方程式 。
23.用下图所示装置进行实验,将A逐滴加入B中:
(1)若A为浓H2SO4,B为第三周期金属元素的单质,
其在常温下难与水反应;C为品红溶液,实验中观察到溶液褪色,则B是 (化学式),B与浓H2SO4反应的方学方程式为 ;反应后往烧杯中加入沸水,又可观察到试管C中的现象为 。
(2)若B为Na2CO3,C为Na2CO3饱和溶液溶液,实验中观察到小试管内溶液变浑浊,则酸A应具有的性质是 。然后往烧杯中加入沸水,可观察到试管C中的现象是 ,试分析该现象的原因: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com