
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
36ЁЂ(4Зж)26.5%
НтЮіЃКЩшNaHSO3ЮЊxmolЃЌNa2SO3ЮЊymolЃЌ
вРЬтвтга
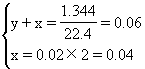
Ёрx=0.04(mol) y=0.02(mol)
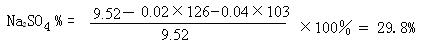
БОзЪСЯгЩЁЖЦпВЪНЬг§ЭјЁЗ ЬсЙЉЃЁ
35ЃЎ(6Зж)(1)(1Зж)113 ~ 450ЁцЃЛ(2)Ѓ2ЁЂ+4ЁЂ+6ЃЛ(1Зж)(3)H2TeЃОH2SeЃОH2SЃЛ(1Зж)
(4)ЛЙдад (1Зж)ЁЁ 2H2Se + O2 == 2H2O + 2SeЃЛ(1Зж)
(5)A12Te3 + ( 6H2O)вЛ-2A1(OH)3Ё§ +3H2TeЁќ (1ЗжЃЌСЌНгЗћКХВЛПлЗж)
34ЁЂ(8Зж)НтЮіЃКЙЬЬЌЕЅжЪAФмгыПеЦјжаЕФбѕЦјЗДгІЩњГЩЦјЬхЮяжЪBЃЌдђAПЩФмЮЊCЛђSЕШЃЌМйЖЈЮЊSЃЌдђBЮЊSO2ЃЌCЮЊSO3ЃЌЫќУЧЕФЯрЖдЗжзгжЪСПЮЊ64ЁУ80ЃН4ЁУ5ЃЌЧЁКУгыЬтвтЯрЗћ(ЭЌЪБвВжЄУїAВЛЪЧC)ЃЌдђDЮЊH2SO4ЃЌЫќЪЧвЛжжживЊЕФЙЄвЕдСЯЃЌгыЬтвтвВЯрЗћЃЌНјвЛВНжЄУїAЮЊSЁЃEЮЊH2SO3ЁЃ
Д№АИЃК(1)H2+S H2S(аДГЩПЩФцЗДгІвВе§ШЗ)ЁЃ
H2S(аДГЩПЩФцЗДгІвВе§ШЗ)ЁЃ
(2)H2SO3 + 2H2S=3S + 3H2OЁЃ
(3)C+2H2SO4(ХЈ) CO2
Ёќ+2SO2 Ёќ+2H2OЛђCu+ 2H2SO4(ХЈ)
CO2
Ёќ+2SO2 Ёќ+2H2OЛђCu+ 2H2SO4(ХЈ) CuSO4
+SO2 Ёќ+ 2H2OЕШЁЃ
CuSO4
+SO2 Ёќ+ 2H2OЕШЁЃ
(4)H2SO3 +2OH- = SO32- + 2H2OЁЃ
33ЁЂ(10Зж)НтЮіЃКвђЮЊетЫФжждЊЫиЮЊЭЌвЛЖЬжмЦкдЊЫиЃЌWКЭXЮЊН№ЪєдЊЫиЃЌЧвИїздЕФзюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮяПЩвдЗДгІЩњбЮКЭЫЎЃЌЫљвдWЮЊNaЃЌXЮЊAlЃЌNaгыYаЮГЩNa2YЃЌЫЕУїYЮЊЃ2МлЃЌМДYЮЊSЃЌдђZЮЊClЁЃ
Д№АИЃК(1)Al(OH)3+OH-ЃНAlO2-+2H2OЁЃ
(2)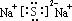
ЁЁ(3)SO2+Cl2+2H2OЃНH2SO4+ 2HClЁЃ
(4)HClЃОH2SЁЃ(5)S2-ЁЁ Cl-ЁЁ Na+ЁЁ Ca2+
32ЁЂ(5Зж)SiO2ЃЛCaSiO3ЃЛNa2SiO3ЃЛSiЃЛH4SiO4(H2SiO3 )
31ЃЎ(17Зж)
ЁЁ (2)вЧЦїЃКЪдЙмЁЂОЦОЋЕЦЁЂНКЭЗЕЮЙм(Иї1Зж)
ЁЁ (3)(ЙВ12ЗжЃЌУППе1Зж)
(4)ЪЕбщНсТлЃКЭЌжмЦкдЊЫиН№ЪєадвРДЮМѕШѕЃЛЗЧН№ЪєадвРДЮдіЧП
(5)3Na2SiO3+2H3PO4=3H2SiO3Ё§+2Na3PO4
36ЃЎ(4Зж)гаNa2SO4ЁЂNa2SO3ЁЂNaHSO3ЕФЛьКЯЮяЙВ9.52gЃЌгызуСПбЮЫсЗДгІЃЌЗХГі1.344L(БъзМзДПі)ЦјЬхЃЛСэШЁЯрЭЌжЪСПЕФИУЛьКЯЮягыNaOHШмвКЗДгІЃЌЯћКФ20mL 2molЃЏLЕФNaOHШмвКЃЌЧѓNa2SO4ЕФжЪСПЗжЪ§ЁЃ
КтЫЎжабЇ2008-2009бЇФъЖШЕкЖўбЇЦкЦкжаПМЪд
ИпвЛЛЏбЇЪдОэ
1-30ЕЅЯюбЁдёЬтЃЌУПаЁЬт2Зж
BABBDЃЌBABAAЃЌCDCACЃЌADCBDЃЌDCDACЃЌBDBAD
35ЁЂ(6Зж)ЙщФЩећРэЪЧПЦбЇбЇЯАЕФживЊЗНЗЈжЎвЛЁЃдкбЇЯАСЫбѕзхдЊЫиЕФИїжжаджЪКѓЃЌПЩЙщФЩећРэГіШчЯТБэЫљЪОЕФБэИё(ВПЗж)ЁЃЁЁ
|
аджЪ\дЊЫи |
8O |
16S |
34Se |
52Te |
|
ЕЅжЪШлЕу(Ёц) |
-218.4 |
113 |
ЁЁ |
450 |
|
ЕЅжЪЗаЕу(Ёц) |
-183 |
444.6 |
685 |
1390 |
|
жївЊЛЏКЯМл |
-2 |
-2,+4,+6 |
-2,+4,+6 |
ЁЁ |
|
дзгАыОЖ |
ж№НЅдіДѓ |
|||
|
ЕЅжЪгыH2ЗДгІЧщПі |
ЕуШМЪБвзЛЏКЯ |
МгШШЛЏКЯ |
МгШШФбЛЏКЯ |
ВЛФмжБНгЛЏКЯ |
ЧыИљОнБэ2ЛиД№ЯТСаЮЪЬтЃК
(1)ЮјЕФШлЕуЗЖЮЇПЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (2)экЕФЛЏКЯМлПЩФмгаЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3)СђЁЂЮјЃЌэкЕФЧтЛЏЮяЫЎШмвКЕФЫсадгЩЧПжСШѕЫГађЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ(ЬюЛЏбЇЪН)ЁЃ
(4)ЧтЮјЫсгаНЯЧПЕФ_________(ЬюЁАбѕЛЏадЁБЛђЁАЛЙдадЁБ)ЃЌвђДЫЗХдкПеЦјжаГЄЦкБЃДцвзБфжЪЃЌЦфПЩФмЗЂЩњЕФЛЏбЇЗНГЬЪНЮЊ____________________________________
(5)ЙЄвЕЩЯAl2Te3ПЩгУРДжЦБИH2TeЃЌЭъГЩЯТСаЛЏбЇЗНГЬЪНЃК
____A12Te3 + (ЁЁЁЁ ) ЁњA1(OH)3Ё§ +H2TeЁќ
34ЁЂ(8Зж)ЯТЭМБэЪОФГЙЬЬЌЕЅжЪAМАЦфЛЏКЯЮяжЎМфЕФзЊЛЏЙиЯЕ(ФГаЉВњЮяКЭЗДгІЬѕМўвбТдШЅ)ЁЃЛЏКЯЮяBдкГЃЮТГЃбЙЯТЮЊЦјЬхЃЌBКЭCЕФЯрЖдЗжзгжЪСПжЎБШЮЊ4ЃК5ЃЌЛЏКЯЮяDЪЧживЊЕФЙЄвЕдСЯЁЃ
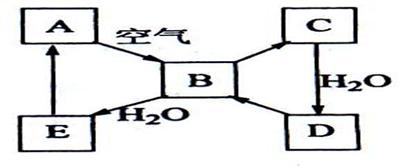
(1)аДГіAдкМгШШЬѕМўЯТгыH2ЗДгІЕФЛЏбЇЗНГЬЪН
___________________________________________________
(2)аДГіEгыAЕФЧтЛЏЮяЗДгІЩњГЩAЕФЛЏбЇЗНГЬЪН_________________
(3)аДГівЛИігЩDЩњГЩBЕФЛЏбЇЗНГЬЪН____________________ЃЛ
(4)НЋ5mL0.10molЁЄLЃ1ЕФEШмвКгы10mL0.10 molЁЄLЃ1ЕФNaOHШмвКЛьКЯЁЃ
аДГіЗДгІЕФРызгЗНГЬЪН__________________________________________ЃЛ
33ЃЎ(10 Зж)WЁЂXЁЂYЁЂZЪЧдзгађЪ§вРДЮдіДѓЕФЭЌвЛЖЬЭЌЦкдЊЫиЃЌWЁЂXЪЧН№ЪєдЊЫиЃЌYЁЂZЪЧЗЧН№ЪєдЊЫиЁЃ
(1)WЁЂXИїздЕФзюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮяПЩвдЗДгІЩњбЮКЭЫЎЃЌИУЗДгІЕФРызгЗНГЬЪНЮЊ____________________ЁЃ
(2)WгыY ПЩаЮГЩЛЏКЯЮяW2YЃЌИУЛЏКЯЮяЕФЕчзгЪНЮЊ______________ЁЃ
(3)YЕФЕЭМлбѕЛЏЮяЭЈШыZЕЅжЪЕФЫЎШмвКжаЃЌЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_____________ЁЃ
(4)БШНЯYЁЂZЦјЬЌЧтЛЏЮяЕФЮШЖЈад_____ЃО_______(гУЗжзгЪНБэЪО)
(5)WЁЂXЁЂYЁЂZЫФжждЊЫиМђЕЅРызгЕФРызгАыОЖгЩДѓЕНаЁЕФЫГађЪЧЃК_____ЃО_____ЃО______ЃО______ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com