
题目列表(包括答案和解析)
7.氧氰(OCN)2的性质与卤素单质的性质相似,在化学上称为拟卤素。氧氰(OCN)2不可能存在的化学键类型有
A.非极性共价键 B.极性共价键 C.共价三键 D.离子键
6.下列叙述中可以说明金属甲的活动性比金属乙的活动性强的是
A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能跟稀盐酸反应放出氢气而乙不能
D.将甲、乙作电极组成原电池时,甲是负极
5.解释下列物质性质的变化规律与物质结构间的因果关系时,与键能无关的变化规律是
①HF、HCl、HBr、HI的热稳定性依次减弱 ②NH3易液化
③F2、C12、Br2、I2的熔、沸点逐渐升高 ④H2S的熔沸点小于H2O的熔沸点
⑤NaF、NaCl、NaBr、NaI的熔点依次减低
A.①③④ B.③④ C.②③④ D.全部
4.有关物质结构的叙述正确的是
A.有较强共价键存在的物质熔沸点一定很高
B.共价化合物任何状态下都不可以导电
C.只含有共价键的物质不一定是共价化合物
D.在离子化合物中不可能存在非极性共价键
3. 从化学键的角度看,化学反应的实质是“旧化学键的断裂和新化学键的形成”,下列变化中既有旧化学键断裂,又有新化学键形成的是
从化学键的角度看,化学反应的实质是“旧化学键的断裂和新化学键的形成”,下列变化中既有旧化学键断裂,又有新化学键形成的是
A.酒精溶于水 B.二氧化碳变成干冰
C.氯化钠受热熔化 D.CaO作为干燥剂吸水
2.银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
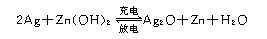
此电池放电时,负极上发生反应的物质是
A.Ag B.Zn(OH)2 C.Zn D.Ag2O
1.哈雷彗星上碳的两种同位素12C、13C原子个数之比为65∶1,而地球上12C和13C原子个数比为89∶1,地球上碳元素相对原子质量是12.011,那么,哈雷彗星上碳元素相对原子质量应是
A.12.000 B.12.009 C.12.015 D.12.980
22.(10分)第一题:如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
①原子核对核外电子的吸引力 ②形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):
|
|
锂 |
X |
Y |
|
失去第一个电子 |
519 |
502 |
580 |
|
失去第二个电子 |
7296 |
4570 |
1820 |
|
失去第三个电子 |
11799 |
6920 |
2750 |
|
失去第四个电子 |
|
9550 |
11600 |
(1)通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量。 。(2分)
(2)表中X可能为第三周期元素中的 (填元素名称)。Y是周期表中 族元素。
(3)第二周期元素中, (填元素符号)元素原子失去核外第一个电子需要的能量最多。
第二题:现有四组物质的熔点数据如下表:
|
A组 |
B组 |
C组 |
D组 |
|
金刚石:3550℃ |
Li:181℃ |
HF:-83℃ |
NaCl:801℃ |
|
硅晶体:1410℃ |
Na:98℃ |
HCl:-115℃ |
KCl:776℃ |
|
硼晶体:2300℃ |
K:64℃ |
HBr:-89℃ |
RbCl:718℃ |
|
二氧化硅:1723℃ |
Rb:39℃ |
HI:-51℃ |
CsCl:645℃ |
据此回答下列问题:
(1)A组属于 晶体,其熔化时克服的微粒间的作用力是 ;
(2)B组晶体共同的物理性质是 (填序号);
①有金属光泽 ②导电性 ③导热性 ④延展性 ⑤易溶于有机溶剂中
(3)C组HF熔点反常是由于 ;
(4)D组晶体可能具有的性质是 (填序号);
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
21.(10分)已知A、B、C、D、E是短周期中的五种元素,它们的原子序数依次增大。A和B可形成常见化合物BA4 ,一个BA4 分子中电子总数为10;C原子的最外层电子数是核外电子总数的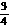 ;D与C同一主族,E-比C2-多一个电子层。试回答:
;D与C同一主族,E-比C2-多一个电子层。试回答:
(1)D与E两元素相比较,非金属性较强的是_______(填元素名称),请你自选试剂设计实验验证该结论(说明试剂、简单操作、实验现象) ;
(2)A、C、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子且甲有18个电子,乙有l0个电子,则甲与乙反应的离子方程式为 ;
(3)B和C形成的一种化合物是参与大气循环的气体,写出它的电子式________
(4)A和C也可形成一种18电子分子,写出该分子的结构式__________________
20.(22分)(1)所含元素超过18种的周期是第 周期。
(2)下列曲线分别表示元素的某种性质与核电荷的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:
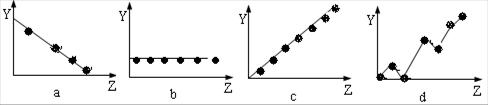
①ⅡA族元素的价电子数 ;②第3周期元素的最高化合价 ;
(3)Pb是82号元素,铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO2-4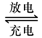 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题:
①Pb在元素周期表中的位置_ _______
②放电时:正极的电极反应式是______________;当消耗Pb 10.35g时,外电路通过________ mol电子,理论上负板的质量增加________g。
③反应中2mol PbSO4和2molH2O的总能量比1molPb和1mol PbO2和2mol硫酸的总能量_______(“高”、“低”、“无法判断”)
(4)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,书写正极反应式__________________________________________
试计算产生氢气的体积(标准状况)___________________
(5)下列反应断裂旧化学键需要的能量比形成新化学键放出的能量多的有_________
①煅烧石灰石 ②氨水和醋酸混合 ③液化石油气燃烧
④Ba(OH)2•8H2O固体和氯化铵固体充分混合 ⑤在家中用铁钉和醋酸制取少许氢气
⑥人体内的呼吸作用 ⑦绿色植物的光合作用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com