
题目列表(包括答案和解析)
26.(18分)下表列出了A~R九种元素在周期表中的位置:
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
|
|
|
E |
|
F |
|
|
|
3 |
A |
C |
D |
|
|
|
G |
R |
|
4 |
B |
|
|
|
|
|
H |
|
⑴这九种元素分别为(填元素符号,以下同)A ,B ,C ,D
E F G H R .
⑵化学性质最不活泼的是 。
⑶A、C、D三种元素的氧化物对应的水化物中,其中碱性最强的是 。
⑷①、③、④三种元素形成的离子,离子半径由大到小的顺序是 。
⑸F元素氢化物的化学式为 ;该氢化物常温下和元素B发生反应的化学方程式为 ;所得溶液的PH 7。
⑹H和A形成化合物的化学式为 ,该化合物高温灼烧时的火焰呈 色。
⑺G元素和H元素两者核电荷数之差是 。
25.(4分)在Cl2、KCl、NH3、NaOH等物质中,只含极性共价键的是 ,只含非极性共价键的是 ,只含离子键的是 ,既含离子键,又含有共价键的是 。
24.(8分) (1)写出下列粒子的结构示意图:
C Na+
(2)写出下列粒子的电子式:
CI O H2O CO2
(3)用电子式表示下列物质的形成过程:
Na CI .
HCI .
23.元素性质随着原子序数的递增呈现周期性变化的原因是
A.元素原子的核外电子排布呈周期性变化 B.元素原子的电子层数呈周期性变化
C.元素的化合价呈周期性变化 D.元素原子半径呈周期性变化
Ⅱ卷(共54分)
22. 除去CO2中少量的SO2气体,最好将混合气体通入( )
A.NaOH溶液 B.澄清石灰水 C.饱和NaHCO3溶液 D.Na2CO3溶液
21.关于SO 2和Cl2的漂白性的说法中正确的是 ( )
A.SO2和Cl2都可使品红溶液褪色,但本质不同
B.SO2和Cl2使品红褪色的本质相同
C.SO2和Cl2都可使湿润的蓝色石蕊试纸先变红后褪色
D.SO2和Cl2以等物质的量混合后通入品红溶液,品红溶液褪色更快
20.下列关于氧族元素性质的叙述中,正确的是 ( )
A.都能生成+6价的化合物 B.都能与金属直接化合
C.原子的最外层电子数都是6 D.都能生成稳定的氢化物
19.某粒子用 Rn-表示,下列关于该粒子的叙述不正确的是( ) A.所含质子数=A-n B.所含中子数=A-Z C.所含电子数=Z+n D.所带电荷数=n
18.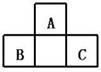 A、B、C均为短周期元素,它们在周期表中的位置如右图.
A、B、C均为短周期元素,它们在周期表中的位置如右图.
已知B、C两元素在周期表中族序数之和是A元素族序数的
2倍;B、C元素的原子序数之和是A元素原子序数的4倍,
则A、B、C 所在的一组是( )
A.Be、Na、Al B.B、Mg、Si C.O、P、Cl D.C、Al、P
17.下列各组元素中,按最高正价递增顺序排列的是
A.C.N、O、F B.K、Mg、C.S
C.F、Cl、Br、I D.Li、Na、K、Rb
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com