
题目列表(包括答案和解析)
26、(共14分)由乙醇制溴乙烷的反应原理如下:
NaBr+H2SO4=NaHSO4+HBr↑ C2H5OH+HBr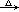 C2H5Br+H2O
C2H5Br+H2O
已知:溴乙烷的沸点为38.4℃,乙醇的沸点为78.3℃,溴化氢的沸点为-67℃。
分子量:乙醇 46 ,溴乙烷 109 ,溴化钠 103
实验室制取溴乙烷的步骤如下:
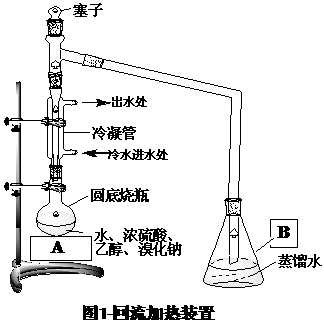
①如图1,在圆底烧瓶中放入20mL水,慢慢加入29mL98%浓硫酸,混和均匀并冷却至室温。再加入乙醇11.6mL(0.20mol),混和后加入24.7g(0.24mol)研细的溴化钠,充分振荡后,加几粒沸石,搭建回流加热装置(冷凝管的作用是冷凝回流挥发出来的乙醇、溴乙烷等,使反应物乙醇反应充分,提高产品的产率。),A处为水浴加热。
②加热一段时间后在圆底烧瓶中有溴乙烷生成,还有乙烯、乙醚和溴等副产物生成。
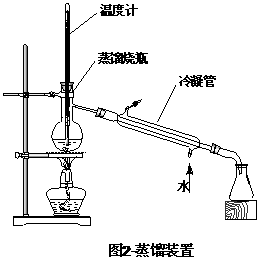
③反应结束后将圆底烧瓶中反应混合物经过除杂处理后,再转移到蒸馏装置中蒸馏,如图2,蒸馏分离得到纯净的溴乙烷。
⑴请写出可能发生副反应的化学方程式(注意条件、温度)并判断反应类型。
产生乙烯气体: ,反应类型: 反应。
产生乙醚: 。
⑵氢溴酸与浓硫酸共热能发生反应,生成三种物质,有两种是气体,其中一种是红棕色气体,反应化学方程式为: 。
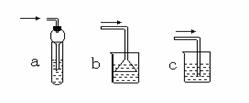
⑶B处为逸出的溴化氢气体吸收装置。导管口接近液面位置,但不伸入液面下,以防倒吸。下列装置能替代装置B,既能吸收HBr气体,又能防止液体倒吸的是 。(选填字母)
⑷回流加热反应结束后,得到的溴乙烷产品中含有溴、乙醚、乙烯等杂质可通过适量的浓硫酸、NaHSO3水溶液等试剂洗涤除去(依据:①乙醚、乙烯可溶解于浓硫酸,溴乙烷不溶于浓硫酸;②Br2+HSO3-+H2O=2Br-+SO42-+3H+)。上述每步除杂操作中,欲得到无色的溴乙烷,还需采取多次的 (填操作名称)方法分离才能得到溴乙烷;操作选用的仪器名称 。
⑸指出图2-蒸馏装置中仪器装置上的一处错误: 。
⑹请写出乙醇的一种用途: 。
⑺图1-回流加热装置中加入适量的水,其作用有: 。
⑻已知原料用量(物质的量):浓硫酸>溴化钠>乙醇,本实验产品理论产量为 g。
南安一中高 一(下)期末化学 理科 考试试卷评分标准
25、(共7分)实验室为了从苯和苯酚的混合物中分离出苯酚,通常采用以下的实验步骤和方法。
(1)往混合物中加入足量的 (填试剂的化学式)溶液后振荡、分层;
(2)将上述混合液通过分液漏斗进行分离;
(3)取下层液体,向其中通入足量的二氧化碳气体,实验现象: ;此步涉及到的化学反应方程式:
;
接着再进行分离,得到目标产物,为了检验苯酚,可取少量有机物并加入 (填试剂名称)。
24、(共3分)在下列物质中:
①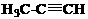 ②C3H8
③CH3-C≡C-CH2-CH3
②C3H8
③CH3-C≡C-CH2-CH3
④ 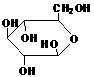 ⑤
⑤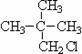 ⑥
⑥ 
⑦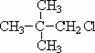 ⑧
⑧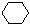 ⑨
⑨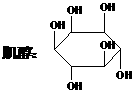
⑩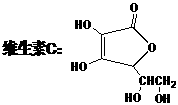

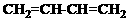
属于同系物的是 ,属于同种物质的是 ,属于同分异构体的是 。(填序号)
23、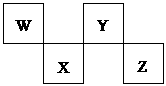 (共9分)W、X、Y、Z 4种短周期元素在元素周期表中位置如图所示,其中Z位于ⅥA族。请回答下列问题。
(共9分)W、X、Y、Z 4种短周期元素在元素周期表中位置如图所示,其中Z位于ⅥA族。请回答下列问题。
⑴W原子结构示意图为 。
⑵能说明Z的非金属性比X非金属性强的事实是
。
⑶X与氧元素形成的化合物 (填化学式),写出该化合物与碳酸钠反应的化学方程式: 。
⑷比X原子序数小1的元素 (填元素名称),该元素对应的最高价氧化物的水化物可以通过氨水与该元素的可溶性盐相互反应来制得,请写出离子反应方程式:
。
⑸请写出比X原子序数大3的元素所形成的氢化物的电子式 。
22、(共4分)现有Na2CO3、NaHCO3、Ca(OH)2、BaCl2、H2SO4、HNO3、CuO六种物质,从中选择适当的物质相互反应,写出满足下列要求的离子反应方程式。(已知:CaSO4微溶,CuO为黑色难溶于水物质)
①反应后得到蓝色溶液:
②有难溶于水且不溶于稀硝酸的白色沉淀生成:
21、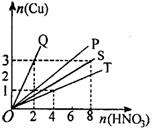 (共3分)铜和硝酸反应的物质的量的关系如图所示,纵坐标表示消耗铜的物质的量,横坐标表示消耗硝酸的物质的量,坐标图中各条线表示下列反应:
(共3分)铜和硝酸反应的物质的量的关系如图所示,纵坐标表示消耗铜的物质的量,横坐标表示消耗硝酸的物质的量,坐标图中各条线表示下列反应:
A. Cu和浓HNO3
B . Cu和稀HNO3
C . Cu和被还原的HNO3(浓)
D . Cu和被还原的HNO3(稀)
其中(填选项)
(1)Q表示反应 ;
(2)P表示反应 ;
(3)T表示反应 。
20、质子核磁共振谱是研究有机物结构的重要方法之一。在研究的化合物分子中:所处环境完全相同的氢原子在谱图中出现同一种信号峰。下列有机物分子在氢核磁共振谱中出现四种信号峰的是 ( )
A (CH3)2CHCH2CH3 B CH3CH2OH C C6H6 D CH3CH2OCH2CH3
第Ⅱ卷
19、37g某一元醇与足量的金属钠完全反应,在标准状况下得到5.6L氢气,该物质可能是( )
A.C4H9OH B.C2H5OH C.C3H7OH D.CH3OH
18、纯净的氯仿可作麻醉剂,但氯仿在保管中常因见光后被空气中的氧气氧化而生成有毒的光气:2CHCl3+O2→2HCl+2COCl2(光气)。为防止发生事故,在使用前需检验氯仿是否变质,为此,应选用的试剂是( )
A NaOH溶液 B Br2水 C AgNO3溶液 D 淀粉KI试液
17、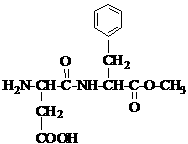 2009年6月,委内瑞拉卫生部宣布,停止在该国市场上销售“零度”可口可乐,原因是这种可乐含有对人体有害的成分。其中,因使用甜味剂阿斯巴甜(ASPARTAME)一度引发人们的质疑。阿斯巴甜是一种常见的食品添加剂。然而随着近年英国、意大利等地出现了阿斯巴甜的致癌说,这种添加剂开始备受争议。其结构简式如右图所示。下列关于阿斯巴甜的说法不正确的是( )
2009年6月,委内瑞拉卫生部宣布,停止在该国市场上销售“零度”可口可乐,原因是这种可乐含有对人体有害的成分。其中,因使用甜味剂阿斯巴甜(ASPARTAME)一度引发人们的质疑。阿斯巴甜是一种常见的食品添加剂。然而随着近年英国、意大利等地出现了阿斯巴甜的致癌说,这种添加剂开始备受争议。其结构简式如右图所示。下列关于阿斯巴甜的说法不正确的是( )
A.它在一定条件下能发生取代、加成反应。
B.阿斯巴甜分子式为C14H18N2O5。
C.若使用阿斯巴甜是安全的前提下,糖尿病患者可以使用阿斯巴甜替代蔗糖。
D.阿斯巴甜属于蛋白质。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com