
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
2.»γΆΦΥυ ΨΒΡΉΑ÷Ο÷–Θ§ΡήΙΜΉι≥…‘≠Βγ≥ΊΘ§≤ζ…ζΒγΝςΒΡ «(ΓΓΓΓ )
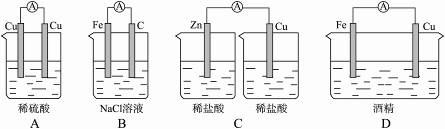
ΫβΈωΘΚΗυΨίΙΙ≥…‘≠Βγ≥ΊΒΡΧθΦΰ±Ί–κΆ§ ±¬ζΉψΘΚ(1)“Σ”–ΜνΕ·–‘≤ΜΆ§ΒΡΝΫΗωΒγΦΪΓΘ»γΫπ τ”κΫπ τΘ§Ϋπ τ”κΖ«Ϋπ τ(»γ ·ΡΪ)Β»ΓΘ(2)“Σ”–ΒγΫβ÷ »ή“ΚΘ§»γΥαΓΔΦνΜρ―Έ»ή“ΚΕΦΩ…“‘ΓΘ(3)“Σ”–ΒΦœΏΘ§Ρή–Έ≥…±’ΚœΜΊ¬ΖΓΘ
”…¥ΥΧθΦΰΫχ––≈–ΕœΘΚAœν÷–ΝΫΗωΒγΦΪΒΡΫπ τ–‘œύΆ§Θ§≤ΜΖϊΚœΧθΦΰ(1)ΓΘCœν÷–ΟΜ”–ΙΙ≥…±’ΚœΜΊ¬ΖΘ§≤ΜΖϊΚœΧθΦΰ(3)ΓΘDœν÷–ΟΜ”–ΒγΫβ÷ »ή“ΚΘ§ΨΤΨΪ «Ζ«ΒγΫβ÷ ΓΘΥυ“‘÷Μ”–BœνΖϊΚœΧθΦΰΓΘ
¥πΑΗΘΚB
1.Ή‘––≥ΒΓΔΒγΕ·Ή‘––≥ΒΓΔΤ’Ά®Τϊ≥ΒœϊΚΡΡήΝΩΒΡάύ–ΆΖ÷±π «(ΓΓΓΓ )
ΔΌ…ζΈοΡήΓΓ ΔΎΚΥΡήΓΓ ΔέΒγΡήΓΓ ΔήΧΪ―τΡήΓΓ ΔίΜ·―ßΡή
A.ΔΌΔήΔίΓΓΓΓΓΓΓΓΓΓΓΓ B.ΔΌΔέΔίΓΓΓΓΓΓΓΓΓΓΓΓΓΓ C.ΔΌΔΎΔέΓΓΓΓΓΓΓΓΓΓΓΓΓΓ D.ΔΌΔέΔή
ΫβΈωΘΚ»ΥΤοΉ‘––≥Β «ΫΪ…ζΈοΡήΉΣΜ·ΈΣΜζ–ΒΡήΘΜΒγΕ·Ή‘––≥Β «ΫΪ–νΒγ≥ΊΒΡΒγΡήΉΣΜ·ΈΣΜζ–ΒΡήΘΜΤ’Ά®Τϊ≥Β «ΫΪΤϊ”ΆΒΡΜ·―ßΡήΉΣΜ·ΈΣΜζ–ΒΡήΘ§Υυ“‘B―Γœν’ΐ»ΖΓΘ
¥πΑΗΘΚB
4.1 mol«βΤχ»Φ…’ ±‘ΦΖ≈»»286 kJΘ§ΕχΟΩ«ßΩΥΤϊ”Ά»Φ…’ ±‘ΦΖ≈»»4 600 kJΓΘ«βΤχ±Μ»œΈΣ «±Ψ άΦΆΧφ¥ζΩσΈο»ΦΝœΒΡάμœκΡή‘¥ΓΘ ‘ ω«βΤχΉςΈΣΡή‘¥ΒΡ»ΐΗω÷ς“Σ”≈ΒψΘΚ
ΔΌ______________________ΘΜΔΎ______________________ΘΜΔέ______________________ΓΘ
Ω…¥”H2ΚΆΤϊ”ΆΒΡ»Φ…’≤ζΈοΒΡ“λΆ§ΒψΕ‘±»ΒΟ≥ωΫα¬έΘΚ
≤ζΈοΘΚH2…ζ≥…H2OΘ§Τϊ”Ά…ζ≥…H2OΓΔCO2Θ§ΜΙ”–…ΌΝΩCOΓΔSO2Β»Έέ»ΨΈοΘΜ
Ζ≈»»ΘΚΟΩ«ßΩΥΤϊ”Ά»Φ…’ ±‘ΦΖ≈≥ω4 600 kJΘ§ΟΩ«ßΩΥH2Ζ≈≥ω286ΓΝ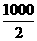 =143
000 kJΘ§ «Τϊ”ΆΒΡ3.1±ΕΓΘ
=143
000 kJΘ§ «Τϊ”ΆΒΡ3.1±ΕΓΘ
H2Ω…ά¥Ή‘Υ°Θ§Τϊ”Ά“Σ”… ·”ΆΖ÷ΝσΜρΝ―Μ·≤ζ…ζΓΘ
¥πΑΗΘΚΔΌά¥‘¥ΖαΗΜΓΓ ΔΎΒΞΈΜ÷ ΝΩΒΡ«βΤχ»Φ…’ ±Ζ≈≥ω»»ΝΩΕύΓΓ Δέ»Φ…’Κσ≤Μ≤ζ…ζΈέ»ΨΈο
10Ζ÷÷”―ΒΝΖ(«ΩΜ·άύ―ΒΝΖΘ§Ω…”Ο”ΎΩΈ÷–)
3. –≥Γ…œ≥ω έΒΡΓΑ»»Ζσ¥ϋΓ±÷–Κ§”–Χζ–ΦΓΔΧΩΖέΓΔΡΨ–ΦΚΆ…ΌΝΩ¬»Μ·ΡΤΓΔΥ°Β»Θ§»»Ζσ¥ϋΤτ”Ο«ΑΘ§”ΟΥήΝœ¥ϋΚΆΩ’ΤχΗτΨχΘ§Ττ”Ο ±¥ρΩΣΥήΝœ¥ϋΘ§«α«α»ύ¥ξΨΆΜαΖ≈≥ω»»ΝΩΓΘ ‘Άξ≥…œ¬Ν–Έ ΧβΘΚ
(1)»»Ζσ¥ϋ≤ζ…ζ»»ΝΩΒΡά¥‘¥ «_____________________________________________________ΓΘ
(2)ΧΩΖέΒΡ÷ς“ΣΉς”Ο «___________________________________________________________ΓΘ
(3)Φ”»κNaClΒΡΉς”Ο «__________________________________________________________ΓΘ
(4)ΡΨ–ΦΒΡΉς”Ο «_______________________________________________________________ΓΘ
ΫβΈωΘΚ±ΨΧβ÷ς“ΣΩΦ≤ι―ß…ζΕ‘‘≠Βγ≥Ί‘≠άμΒΡ’ΤΈ’ΚΆ”Π”ΟΒΡΧβΡΩΘ§ «“ΜΒάάμ¬έΝΣœΒ ΒΦ ΒΡΚΟΧβΓΘ
¥πΑΗΘΚ(1)Χζ±Μ―θΜ·Ζ≈≥ωΒΡ»»ΝΩ
(2)”κΧζ–ΦΓΔNaCl»ή“ΚΙΙ≥…‘≠Βγ≥ΊΘ§Φ”ΥΌΧζ–ΦΒΡ―θΜ·
(3)NaCl»ή”ΎΥ°Θ§–Έ≥…ΒγΫβ÷ »ή“Κ
(4) Ι”ΟΓΑ»»Ζσ¥ϋΓ± ± ή»»Ψυ‘»
2.XΓΔYΓΔZΕΦ «Ϋπ τΘ§Α―XΆΕ»κZΒΡœθΥα―Έ»ή“Κ÷–,XΒΡ±μΟφ”–ZΈω≥ωΘ§X ”κYΉι≥…‘≠Βγ≥Ί ±Θ§YΈΣΒγ≥ΊΒΡΗΚΦΪΘ§XΓΔYΓΔZ»ΐ÷÷Ϋπ τΒΡΜνΤΟ–‘Υ≥–ρΈΣ(ΓΓΓΓ )
A.X>Y>ZΓΓΓΓΓΓΓΓΓΓΓΓΓΓ B.X>Z>YΓΓΓΓΓΓΓΓΓΓΓΓΓΓ C.Y>X>ZΓΓΓΓΓΓΓΓΓΓΓΓ D.Y>Z>X
ΫβΈωΘΚXΡήΑ―Z¥”ΤδœθΥα―Έ»ή“Κ÷–÷ΟΜΜ≥ωά¥Θ§ΥΒΟςXΒΡΜνΤΟ–‘«Ω”ΎZΘΜX ”κYΉι≥…‘≠Βγ≥Ί ±Θ§YΈΣΒγ≥ΊΒΡΗΚΦΪΘ§ΥΒΟςYΒΡΜνΤΟ–‘«Ω”ΎXΘ§Ι ’ΐ»Ζ¥πΑΗΈΣCΓΘ
¥πΑΗΘΚC
1.ΗυΨίZn+Cu2+====Zn2++CuΒΡΖ¥”Π‘≠άμ…ηΦΤ“ΜΗω‘≠Βγ≥ΊΘ§Β±ZnΈΣΗΚΦΪ ±Θ§’ΐΦΪΩ…“‘―Γ”ΟΒΡΫπ τ≤ΡΝœ «(ΓΓΓΓ )
A.ΟΨΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ B. ·ΡΪΓΓΓΓΓΓΓΓΓΓΓΓΓΓ C.¬ΝΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ D.«Π
ΗυΨί‘≠Βγ≥Ί–Έ≥…ΧθΦΰΘ§“Σ ΙZnΉςΗΚΦΪΘ§”κΥϋœύΝ§ΒΡΫπ τ±Ί–κ“Σ±»ZnΒΡΜνΤΟ–‘≤νΘ§ ·ΡΪΈΣΖ«Ϋπ τΘ§Ι ¥πΑΗΈΣDΓΘ
¥πΑΗΘΚD
15.AΓΔBΓΔCΓΔDΓΔEΈε÷÷‘ΣΥΊΘ§CΚΆD‘≠Ή”–ρ ΐΖ÷±π±»EΚΆAΒΡ‘≠Ή”–ρ ΐ¥σ1Θ§BΚΆDΒΡάκΉ”ΨΏ”–œύΆ§ΒΡΒγΉ”≤ψΫαΙΙΘ§B «Ά§÷ήΤΎ÷–‘≠Ή”ΑκΨΕΉν¥σΒΡ‘ΣΥΊ(≥ΐœΓ”–ΤχΧε‘ΣΥΊΆβ)ΓΘA‘ΣΥΊ‘ΎΤδΉνΗΏΦέ―θΜ·Έο÷–Κ§ΝΩ «40%Θ§‘ΎΤδ«βΜ·Έο÷–ΒΡΚ§ΝΩ «94.1%Θ§A‘ΣΥΊ‘≠Ή”÷–÷ Ή”ΓΔ÷–Ή”ΓΔΒγΉ” ΐœύΒ»ΓΘ18 g CΒΡΒΞ÷ ”κΉψΝΩΒΡœΓΝρΥαΖ¥”ΠΘ§‘Ύ±ξΉΦΉ¥Ωωœ¬Θ§…ζ≥…22.4 L«βΤχΓΘC‘ΣΥΊ‘≠Ή”÷–”–14Ηω÷–Ή”ΓΘ‘ρΘΚ
(1)AΓΔBΓΔCΓΔDΓΔEΗς «(Χν–¥‘ΣΥΊΖϊΚ≈) _________________________________________ΓΘ
(2)AΓΔBΓΔCΓΔDΓΔE‘Ύ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο“ά¥Έ «____________________________________ΓΘ
(3)AΓΔBΓΔCΓΔDΓΔE÷–ΒΟΒγΉ”ΡήΝΠΉν«ΩΒΡ‘ΣΥΊ «_________________Θ§ ßΒγΉ”ΡήΝΠΉν«ΩΒΡ‘ΣΥΊ «____________ΓΘ
(4)œ÷––‘ΣΥΊ÷ήΤΎ±μ÷–ΒΟΒγΉ”ΡήΝΠΉν«ΩΒΡ‘ΣΥΊ «_________________Θ§ ßΒγΉ”ΡήΝΠΉν«ΩΒΡ‘ΣΥΊ «______________ΓΘ
(5)ΥφΉ≈÷ήΤΎ±μΒΡ÷π≤ΫΆξ…ΤΘ§”ΟΖΔ’ΙΒΡΙέΒψΖ÷ΈωΘ§‘ΣΥΊ÷ήΤΎ±μ÷–ΒΟ ßΒγΉ”ΡήΝΠΉν«ΩΒΡ‘ΣΥΊ «ΖώΜαΖΔ…ζ±δΜ·?
ΫβΈωΘΚ±ΨΧβ «ΫΪΈο÷ ΫαΙΙΓΔ‘ΣΥΊΦΑΤδΜ·ΚœΈο÷Σ Ε“‘ΦΑ‘ΣΥΊΒΡΫαΙΙΓΔΈΜ÷ΟΚΆ–‘÷ Β»÷Σ ΕΫαΚœΤπά¥Ε‘‘ΣΥΊ÷÷άύΫχ––ΆΤΕœΓΘΧβΡΩ÷–“Σ«σΆΤΕœΒΡΈε÷÷‘ΣΥΊ÷–Θ§Ε‘A‘ΣΥΊΧαΙ©ΒΡΧθΦΰΚή≥δΖ÷Θ§Ε‘AΫχ––”–ΙΊΜ·―ß ΫΦΤΥψ «Ϋβ¥π±ΨΧβΒΡ“ΜΗωΆΜΤΤΩΎΓΘΝμΆβΘ§C‘ΣΥΊ“≤Ω…Ά®ΙΐΜ·―ßΖΫ≥Χ ΫΦΤΥψ«σΒΟΤδœύΕ‘‘≠Ή”÷ ΝΩΘ§ΫχΕχ»ΖΕ®C‘ΣΥΊ÷÷άύΓΘ
¥πΑΗΘΚ(1)SΓΔKΓΔAlΓΔClΓΔMg
(2)ΒΎ»ΐ÷ήΤΎΔωAΉεΓΔΒΎΥΡ÷ήΤΎI AΉεΓΔΒΎ»ΐ÷ήΤΎΔσAΉεΓΔΒΎ»ΐ÷ήΤΎΔςAΉεΓΔΒΎ»ΐ÷ήΤΎΔρAΉε
(3)ClΓΓ KΓΓ (4)FΓΓ Fr
(5)ΥφΉ≈÷ήΤΎ±μΒΡ÷π≤ΫΆξ…ΤΘ§ΫΪά¥≥ωœ÷–¬ΒΡ÷ήΤΎ÷°ΚσΘ§ΉνΉσœ¬ΖΫΒΡ‘ΣΥΊΜαΖΔ…ζ±δΜ·ΕχΉν”“…œΖΫΒΡ‘ΣΥΊ «≤ΜΜαΖΔ…ζ±δΜ·ΒΡΘ§Φ¥ΒΟΒγΉ”ΡήΝΠΉν«ΩΒΡ‘ΣΥΊ≤ΜΜα±δΘ§Εχ ßΒγΉ”ΡήΝΠ«ΩΒΡ‘ΣΥΊΜαΖΔ…ζ±δΜ·ΓΘ
14.ΒΣΜ·ΡΤ(Na3N) «ΩΤ―ßΦ“÷Τ±ΗΒΡ“Μ÷÷÷Ί“ΣΜ·ΚœΈοΘ§Υϋ”κΥ°Ής”Ο…ζ≥…NH3ΚΆ«β―θΜ·ΡΤΓΘ«κΆξ≥…œ¬Ν–Έ ΧβΘΚ
(1)Na3NΒΡΒγΉ” Ϋ «____________Θ§ΗΟΜ·ΚœΈο”…____________Φϋ–Έ≥…ΓΘ
(2)Na3N”κ―ΈΥαΖ¥”Π…ζ≥…____________÷÷―ΈΓΘ
(3)Na3N”κΥ°Ζ¥”Π τ”Ύ____________Ζ¥”Π(ΧνΜυ±ΨΖ¥”Πάύ–Ά)ΓΘ
(4)±»ΫœNa3N÷–ΝΫ÷÷ΝΘΉ”ΒΡΑκΨΕΘΚNa+____________N3-(ΧνΓΑΘΨΓ±ΓΑΘΫΓ±ΜρΓΑΘΦΓ±)
ΫβΈωΘΚΡΤ «ΜνΤΟΫπ τΘ§ΒΣ «ΫœΜνΤΟΖ«Ϋπ τΘ§Na3N τ”ΎάκΉ”Μ·ΚœΈοΓΘNa3N”κΥ°Ζ¥”ΠΘ§ΡΤάκΉ”ΫαΚœ«β―θΗυάκΉ”Θ§ΒΣάκΉ”ΫαΚœ«βάκΉ”–Έ≥…Α±Θ§NH3”κHClΖ¥”Π…ζ≥…οß―ΈΓΘ
¥πΑΗΘΚ(1)Na+Θέ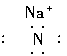 Θί3-Na+ΓΓ άκΉ”
Θί3-Na+ΓΓ άκΉ”
(2)2ΓΓ (3)Η¥Ζ÷ΫβΓΓ (4)ΘΦ
13.Ρ≥Ά§―ß‘ΎΜ≠Ρ≥÷÷‘ΣΥΊΒΡ“Μ÷÷ΒΞΚΥΝΘΉ”ΒΡ‘≠Ή”ΫαΙΙ Ψ“βΆΦ ±Θ§ΆϋΦ«‘Ύ‘≤»ΠΡΎ±ξΤδ÷ Ή” ΐ.«κΡψΗυΨίœ¬ΟφΒΡΧα ΨΉς≥ωΉ‘ΦΚΒΡ≈–ΕœΓΘ
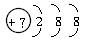
(1)ΗΟΝΘΉ” «÷––‘ΝΘΉ”Θ§’β÷÷ΝΘΉ”ΒΡΖϊΚ≈ «__________________ΓΘ
(2)ΗΟΝΘΉ”ΒΡ―Έ»ή“ΚΡή ΙδεΥ°Ά …ΪΘ§≤Δ≥ωœ÷ΜκΉ«Θ§’β÷÷ΝΘΉ”ΒΡΖϊΚ≈ «________________ΓΘ
(3)ΗΟΝΘΉ”ΒΡ―θΜ·–‘Κή»θΘ§ΒΟΒΫ1ΗωΒγΉ”Κσ±δΈΣ‘≠Ή”Θ§‘≠Ή”ΒΡΜΙ‘≠–‘Κή«ΩΘ§’β÷÷ΝΘΉ”ΒΡΖϊΚ≈ «
________________ΓΘ
(4)ΗΟΝΘΉ”ΒΡΜΙ‘≠–‘Κή»θΘ§ ß»Ξ1ΗωΒγΉ”Κσ±δΈΣ‘≠Ή”Θ§‘≠Ή”ΒΡ―θΜ·–‘Κή«ΩΘ§’β÷÷ΝΘΉ”ΒΡΖϊΚ≈ «
________________ΓΘ
ΫβΈωΘΚΧβ…η÷–ΓΑΝΘΉ”Γ±ΒΡΚΥΆβΒγΉ”≈≈≤ΦΈΣ2ΓΔ8ΓΔ8Θ§ «“Μ÷÷Έ»Ε®ΫαΙΙΘ§ΗΟΝΘΉ”Ω…“‘ «‘≠Ή”Θ§“≤Ω…“‘ «“θΓΔ―τάκΉ”ΓΘ»γΙϊ «÷––‘ΝΘΉ”Φ¥‘≠Ή”Θ§ΚΥΡΎΒΡ÷ Ή” ΐ”ΠΗΟΒ»”ΎΚΥΆβΒΡΒγΉ” ΐΘ§Φ¥2+8+8=18Θ§÷ Ή” ΐΈΣ18ΒΡ‘ΣΥΊ «ArΘΜ‘Ύ»ή“Κ÷–Ρή ΙδεΥ°Ά …Ϊ≤Δ≥ωœ÷ΜκΉ«ΒΡΈο÷ ”ΠΗΟ «ΝρΜ·ΈοΘ§ΗΟΝΘΉ””ΠΗΟ «S2-ΘΜΝΘΉ”ΒΟΒΫ1ΗωΒγΉ”Κσ±δΈΣ‘≠Ή”Θ§‘ρΤδ‘≠Ή”ΒΡΒγΉ” ΐ”ΠΗΟΈΣ18+1=19Θ§÷ Ή” ΐ”ΠΗΟ «19Θ§Φ¥ΦΊ‘≠Ή”Θ§‘ρ’β÷÷ΝΘΉ” «K+Θ§K+ΒΡ―θΜ·–‘Κή»θΕχΦΊΒΡΜΙ‘≠–‘Κή«ΩΘ§ΖϊΚœΧβΡΩ“Σ«σΘΜΝΘΉ” ß»Ξ1ΗωΒγΉ”Κσ±δΈΣ‘≠Ή”Θ§‘ρΤδ‘≠Ή”ΒΡΒγΉ” ΐ”ΠΗΟΈΣ18-1=17Θ§÷ Ή” ΐ”ΠΗΟ «17Θ§Φ¥¬»‘≠Ή”Θ§‘ρ’β÷÷ΝΘΉ” «Cl-Θ§Cl-ΒΡΜΙ‘≠–‘Κή»θΕχ¬»‘≠Ή”ΒΡ―θΜ·–‘Κή«ΩΘ§ΖϊΚœΧβΡΩ“Σ«σΓΘ
¥πΑΗΘΚ(1)ArΓΓ (2)S2-ΓΓ (3)K+ΓΓ (4)Cl-
12.œ¬ΆΦ «Ρ≥Ά§―ßΜ≠ΒΡΝυ÷÷ΝΘΉ”ΒΡ‘≠Ή”ΫαΙΙ Ψ“βΆΦΘ§«κΡψΗχΥϊ»œ’φ≈ζΗΡΘ§÷Η≥ωΤδ÷–ΒΡ¥μΈσΓΘ
a.LiΓΓ 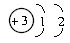 ΓΓb.KΓΓ
ΓΓb.KΓΓ 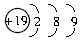 ΓΓc.ClΓΓ
ΓΓc.ClΓΓ 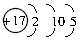 ΓΓd.KrΓΓ
ΓΓd.KrΓΓ 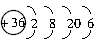 ΓΓe.S2-ΓΓ
ΓΓe.S2-ΓΓ 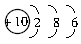 ΓΓf.Mg2+ΓΓ
ΓΓf.Mg2+ΓΓ 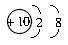
ΫβΈωΘΚ±ΨΧβ ΒΦ …œΩ…Φ”…νΈ“Ο«Ε‘ΚΥΆβΒγΉ”Ζ÷≤ψ≈≈≤ΦΥΡΧθΙφ¬…ΒΡάμΫβΓΘ‘ΎΖ÷ΈωΝΘΉ”ΒΡ‘≠Ή”ΫαΙΙ Ψ“βΆΦ’ΐΈσ ±Θ§’βΥΡΧθΙφ¬…±Ί–κΆ§ ±¬ζΉψΓΘ‘≠Ή”ΫαΙΙ Ψ“βΆΦ≥ΐΩ…“‘±μ Ψ‘≠Ή”ΒΡΫαΙΙΆβΘ§ΜΙΩ…“‘±μ Ψ“θΓΔ―τάκΉ”ΒΡΫαΙΙΓΘ–η“ΣΉΔ“βΒΡ «Θ§±μ Ψ“θΓΔ―τάκΉ”ΒΡΫαΙΙ ±Θ§ΚΥΡΎΒΡ÷ Ή” ΐ”κΚΥΆβΒγΉ” ΐ «¥φ‘Ύ≤ν±πΒΡΓΘ
¥πΑΗΘΚ(1)ΗυΨίΒγΉ”Ήή «ΨΓΝΩœ»≈≈≤Φ‘ΎΡήΝΩΫœΒΆΒΡΒγΉ”≤ψΘ§”ΠΗΟœ»≈≈¬ζΒΎ“Μ≤ψ‘Ό≈≈ΒΎΕΰ≤ψΘ§ΒΎ“Μ≤ψΉνΕύΩ…“‘»ίΡ…2ΗωΒγΉ”Θ§ Θœ¬1Ηω≈≈‘ΎΒΎΕΰ≤ψΘ§Υυ“‘a «¥μΈσΒΡΓΘ
(2)ΒΎ»ΐ≤ψΉνΕύΩ…“‘»ίΡ…18ΗωΒγΉ”Θ§ΒΪ «‘Ύ¥ΥΫαΙΙ÷–Θ§ΒΎ»ΐ≤ψΆ§ ± «ΉνΆβ≤ψΘ§ΉνΆβ≤ψ»ίΡ…ΒΡΒγΉ” ΐ≤ΜΡή≥§Ιΐ8ΗωΘ§Υυ“‘K‘≠Ή”ΒΡΚΥΆβΒγΉ”≈≈≤ΦΥφΒγΉ”≤ψ ΐΒΡΒί‘ω“ά¥ΈΈΣ2ΓΔ8ΓΔ8ΓΔ1Θ§b“≤ «¥μΈσΒΡΓΘ
(3)ΒΎΕΰ≤ψΉνΕύ»ίΡ…8ΗωΒγΉ”Θ§Υυ“‘c¥μΓΘ
(4)ΒΎ»ΐ≤ψΉνΕύ»ίΡ…18ΗωΒγΉ”Θ§Υυ“‘d¥μΓΘ(5)S2-ΒΡΚΥΆβΒγΉ” ΐΈΣ18Θ§Υυ“‘S2-ΒΡΚΥΆβΒγΉ”≈≈≤Φ”ΠΗΟΈΣ2ΓΔ8ΓΔ8Θ§Υυ“‘e¥μΓΘ
(6)Mg2+ΒΡΚΥΆβΒγΉ” ΐΈΣ10Θ§ΒΪΚΥΡΎΒΡ÷ Ή” ΐ»‘»ΜΈΣ12Εχ≤Μ «10Θ§Υυ“‘f¥μΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com