
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
2ЁЂЯТСааджЪЕФБШНЯжаЃЌДэЮѓЕФЪЧ(ЁЁЁЁЁЁ )
AЁЂШлЁЂЗаЕуЃКK>Na>LiЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁBЁЂдзгАыОЖЃКCa>Mg>Al
CЁЂЛюЖЏадЃКK>Ca>NaЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁDЁЂбѕЛЏадЃКAg+>Cu2>Mg2+
1ЁЂЯТСаЫЕЗЈжаЃЌе§ШЗЕФЪЧ(ЁЁЁЁЁЁ )
AЁЂЗВФмЕМЕчЕФЮяжЪвЛЖЈЪЧЕЅжЪЁЁЁЁЁЁЁЁЁЁ
BЁЂ Н№ЪєЕЅжЪЖМФмгыЯЁСђЫсЗЂЩњжУЛЛЗДгІ
CЁЂЛюЦУН№ЪєЖМФмДгбЮШмвКжажУЛЛГіНЯВЛЛюЦУЕФН№Ъє
DЁЂдкЛЏбЇЗДгІжаЃЌН№ЪєЪЇЕчзгЃЌГЃзїЛЙдМС
33ЃЎ31.9ПЫгЩAlЁЂBaCl2ЁЂNa2CO3ЗлФЉзщГЩЕФЛьКЯЮяЃЌЗХШы200 mlNaOHШмвКжаНјааЗДгІЃЌЪеМЏЕНБъПіЯТЦјЬх13.4Щ§ЁЃЙ§ТЫКѓЃЌдкВПЗжТЫвКжаМгШыТСЦЌЮоЦјЬхВњЩњЃЌдкСэвЛВПЗжТЫвКжаМгШызуСПЕФH2SO4(ЯЁ)ЃЌМШЮоЦјЬхЃЌгжЮоГСЕэЩњГЩЁЃНЋТЫдќШмНтдкбЮЫсжаЃЌПЩЪеМЏЕНБъПіЯТЦјЬхG 7.84Щ§ЁЃЧѓЃК
ЁЁЁЁ (1)NaOHШмвКЕФЮяжЪЕФСПЕФХЈЖШЁЃ
ЁЁЁЁ (2)ЦјЬхGЕФзщГЩКЭУмЖШЁЃ
(3)ЛьКЯЮяжаТСЕФжЪСПЗжЪ§ЁЃ
32ЃЎгЩЭЦЌЁЂаПЦЌКЭ200mLЯЁH2SO4зщГЩЕФдЕчГижаЃЌШєаПЦЌжЛЗЂЩњЕчЛЏбЇИЏЪДЃЌдђЕБдкЭЦЌЩЯЙВЗХГі3.36L(БъзМзДПі)ЦјЬхЪБЃЌH2SO4ЧЁКУШЋВПгУЭъЃЌВњЩњетаЉЦјЬхЯћКФаПЖрЩйПЫЃПгаЖрЩйИіЕчзгЭЈЙ§СЫЕМЯпЃПдЯЁH2SO4ЕФЮяжЪЕФСПХЈЖШЪЧЖрЩйЃП
31ЃЎКкЩЋЙЬЬхЮяжЪAгаЯТЭМЫљЪОЕФзЊЛЏЙиЯЕЃЌУПИіЗНПђБэЪОгавЛжжЗДгІЮяЛђЩњГЩЮя(ЗДгІЬѕМўМАЩњГЩЕФЫЎвбТдШЅ)ЃЌЦфжаCЁЂFГЃЮТЮЊЮоЩЋЦјЬхЃЌЦфжаCгаГєМІЕАЦјЮЖЃЛDЁЂEгаЙВЭЌЕФбєРызгЃЌDжаМгШыKSCNШмвКЯдКьЩЋЁЃ
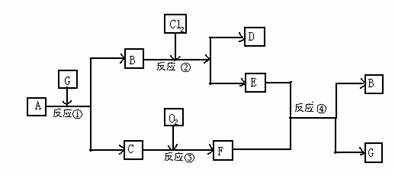
ЁЁЁЁЁЁ (1)аДГіBКЭCЕФЛЏбЇЪНЃКBЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЂCЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁЁЁЁЁ (2)аДГіЗДгІЂмЕФРызгЗНГЬЪНЃКЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
30ЃЎГЦЕШжЪСПЕФШ§ЗнаПЗлЃЌЗжБ№ЪЂгкМзЁЂввЁЂБћШ§жЇЪдЙмжаЃЌАДЯТСавЊЧѓСэМгЮяжЪКѓЃЌШћЩЯДјЕМЙмЕФШћзгЃЌвЛЖЈЪБМфКѓВтЖЈЩњГЩЧтЦјЕФЬхЛ§ЁЃМзМгШы50mL PH=3ЕФбЮЫсЃЛввМгШы50mL PH=3ЕФДзЫсЃЛБћМгШы50mL PH=3ЕФДзЫсМАЩйСПЕЈЗЏЗлФЉЁЃШєЗДгІжеСЫЃЌЩњГЩЧтЦјЕФЬхЛ§вЛбљЖрЁЃНЋМзЁЂввЁЂБћгУЗћКХЁА>ЁБЁЂЁА=ЁБЁЂЁА<ЁББэЪОЫќУЧжЎМфЕФЙиЯЕЃК
ЁЁЁЁЁЁ (1)ПЊЪМЪБЗДгІЫйТЪЕФДѓаЁЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁЁЁЁЁ (2)Ш§ЪдЙмжаВЮМгЗДгІЕФаПжЪСПЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁЁЁЁЁ (3)ЗДгІжеСЫЃЌЫљашЪБМфЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁЁЁЁЁ (4)дкЗДгІЙ§ГЬжаЃЌввЁЂБћЫйТЪВЛЭЌЕФРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
29ЃЎ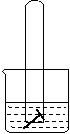 ШчЭМЃКЫЎВлжаЪдЙмФкгавЛУЖЬњЖЄЃЌЗХжУЪ§ЬьЙлВьЃК
ШчЭМЃКЫЎВлжаЪдЙмФкгавЛУЖЬњЖЄЃЌЗХжУЪ§ЬьЙлВьЃК
ЁЁЁЁЁЁ (1)ШєвКУцЩЯЩ§ЃЌдђШмвКГЪЯжЁЁЁЁЁЁ адЃЌ
ЗЂЩњЁЁЁЁЁЁ ИЏЪДЃЌЕчМЋЗДгІЪНЃК
ИКМЋЁЁЁЁЁЁЁЁЁЁ ЁЁЃЌе§МЋЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁЁЁЁЁ (2)ШєвКУцЯТНЕЃЌдђШмвКГЪЁЁЁЁЁЁЁЁЁЁЁЁ адЃЌ
ЗЂЩњЁЁЁЁЁЁ ЁЁИЏЪДЃЌЕчМЋЗДгІЪНЃК
ИКМЋЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЃЌе§МЋЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
28ЃЎгУЯТУцСНжжЗНЗЈПЩвджЦЕУАзЩЋЕФFe(OH)2ГСЕэЁЃ
ЗНЗЈвЛЃКгУВЛКЌFe3+ЕФFeSO4ШмвКгыгУВЛКЌO2ЕФеєСѓЫЎХфжЦЕФNaOHШмвКЗДгІжЦБИЁЃ
(1)гУСђЫсбЧЬњОЇЬхХфжЦЩЯЪіFeSO4ШмвКЪБЛЙашМгШыЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)Г§ШЅеєСѓЫЎжаШмНтЕФO2ГЃВЩгУЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЕФЗНЗЈЁЃ
(3)ЩњГЩАзЩЋFe(OH)2 ГСЕэЕФВйзїЪЧгУГЄЕЮЙмЮќШЁВЛКЌO2ЕФNaOHШмвКЃЌ
ВхШыFeSO4ШмвКвКУцЯТЃЌдйМЗГіNaOHШмвКЁЃетбљВйзїЕФРэгЩЪЧЁЁЁЁЁЁЁЁ ЁЃ
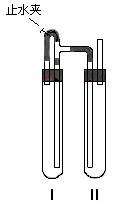 ЗНЗЈЖўЃКдкШчЭМзАжУжаЃЌгУNaOHШмвКЁЂЬњаМЁЂ
ЗНЗЈЖўЃКдкШчЭМзАжУжаЃЌгУNaOHШмвКЁЂЬњаМЁЂ
ЯЁH2SO4ЕШЪдМСжЦБИЁЃ
(1)дкЪдЙмIРяМгШыЕФЪдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)дкЪдЙмIIРяМгШыЕФЪдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ЮЊСЫжЦЕУАзЩЋFe(OH)2ГСЕэЃЌдкЪдЙмIКЭIIжаМгШыЪдМСЃЌ
ДђПЊжЙЫЎМаЃЌШћзгКѓЕФЪЕбщВНжшЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)етбљЩњГЩЕФFe(OH)2ГСЕэФмНЯГЄЪБМфБЃГжАзЩЋЃЌ
ЦфРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
27ЃЎТЬЗЏОЇЬхгЩгкБЃДцВЛЭзЛђГЄОУЗХжУЃЌШнвзВПЗжЛђШЋВПБЛбѕЛЏЁЃЯжгавЛЦПТЬЗЏбљЦЗЃЌЯыСЫНтЦфЪЧЗёБЛбѕЛЏКЭБЛбѕЛЏЕФГЬЖШЃЌЪдбЁдёКЯЪЪЕФЪдМСКЭВйзїЃЌИљОнЯрЙиЕФЪЕбщЯжЯѓНјааЭЦВтЁЃ
ЁЁЁЁЁЁ (1)жЄУїЦфЭъШЋУЛгаБЛбѕЛЏЕФЪдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЃЌЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁЁЁЁЁ (2)жЄУїЦфвбЭъШЋБЛбѕЛЏЕФЪдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЃЌЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁЁЁЁЁ (3)ЭЈЙ§дѕбљЕФЪЕбщКЭЯжЯѓПЩЫЕУїЦфжЛЪЧВПЗжБЛбѕЛЏЃПЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЩцМАЕФРызгЗНГЬЪНЮЊЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
26ЃЎ ГЃЮТЯТЃЌНЋ100gЬњЭЖШывЛЖЈСПЕФЯѕЫсжаЃЌВЛдйЗДгІКѓЃЌШЁГіЯДОЛЃЌжЪСПЮЊ94.4gЃЌШєЯѕЫсЕФЛЙдВњЮяЪЧЕЊЕФбѕЛЏЮяЃЌдђЗДгІжаЮДБЛЛЙдЕФЯѕЫсЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁЁЁ )
ЁЁ AЃЎ0.1molЁЁЁЁЁЁ BЃЎ0.2 molЁЁЁЁ CЃЎ0.3 molЁЁЁЁЁЁ DЃЎ0.4 mol
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com