
题目列表(包括答案和解析)
16、汽车的启动电源常用铅蓄电池,电池反应如下:
 PbO2 + Pb + 2H2SO4 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的 是( )
PbO2 + Pb + 2H2SO4 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的 是( )
A.PbO2放电时是电池的负极,充电时是电池的阳极。
B.负极的电极反应式为:Pb + SO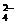 – 2e – = PbSO4
– 2e – = PbSO4
C.放电时,PbO2得电子,被氧化
D.电池放电时,溶液酸性增强
15.常温时,将足量的AgCl分别加入同体积的下列各溶液中,AgCl溶解最少的是 ( )
A.1mol/L的MgCl2溶液 B.2mol/L的NaCl溶液
C.1.4mol/L的BaCl2溶液 D.1mol/L的AlCl3溶液
14.下列实验方案合理的是 ( )
A.用湿润的pH试纸测定某盐溶液的pH
B.制备FeCl3溶液时,先将固体溶于较浓盐酸,再加水稀释
C.用甲基橙检验溶液的酸碱性m
D.为了加更快得到氢气,可以用纯锌代替粗锌
13、将相同物质的量浓度的某弱酸HX溶液与NaX溶液等体积混合,测得混合后溶液中c(Na+) > c (X- ),则下列关系正确的是:( )
A.c (OH- ) > c (H+ )
B.c (HX ) < c (X- )
C.c (X- ) + c(HX )= c (Na+)
D.c (Na+ ) + c (OH- )== c( H+ ) > c (HX )
12、反应4A(g) + 5B(g) 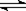 4C(g)
+ 6D(g) △H =-Q kJ/mol,在一定温度下达到化学平衡状态时,下列说法正确的是:( )
4C(g)
+ 6D(g) △H =-Q kJ/mol,在一定温度下达到化学平衡状态时,下列说法正确的是:( )
A. 若增大压强,A和B的转化率都增大
B. 若升高温度最终能生成更多的C和D
C. 单位时间里有4n mol A消耗,同时有5n mol B生成
D. 容器里A、B、C、D的浓度比是4:5:4:6
11、pH相同的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌粒全部溶解且放出气体一样多,为此下列说法正确的是( )
A.反应开始时的速率:甲>乙
B.反应开始时,酸的物质的量浓度:甲<乙
C.反应所需时间:甲<乙 D.反应后溶液的pH:甲<乙
10、反应:L(s)+a
G(g) 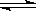 b R(g) 达到平衡时,
b R(g) 达到平衡时,
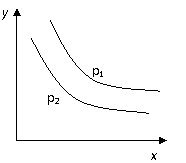 温度和压强对该反应的影响如图所示:图中压强p1>p2,
温度和压强对该反应的影响如图所示:图中压强p1>p2,
x轴表示温度,y轴表示平衡混合气中G的体积分数。
据此可判断( )
A.上述反应是放热反应 C.a>b
B.上述反应是吸热反应 D.a=b
9、已知反应A2(g)+2B2(g) 2AB2(g) △H <0,下列说法正确的( )
2AB2(g) △H <0,下列说法正确的( )
A.升高温度有利于反应速率增加,从而缩短达到平衡的时间
B.升高温度,正向反应速率增加,逆向反应速率减小
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
8、体积相同、pH相同的HCl溶液和CH3COOH溶液,与NaOH溶液中和时两者消耗NaOH的物质的量:( )
A.相等 B.中和HCl的量 C.中和CH3COOH的量多 D.无法比较
7、常温下,下列物质的水溶液,其pH小于7的是( )
A.Na2CO3 B.NH4NO3 C.Na2SO4 D.Fe(OH)3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com