
题目列表(包括答案和解析)
7.将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合后,溶液pH>7,以下关系式错误的是 ( )
A.质子守恒:c(HA)+c(H+)= c(A-)+c(OH-)
B.物料守恒:c(HA)+c(A-)=0.1mol/L
C.电荷守恒:c(Na+)+c(H+)= c(A-)+c(Cl-)+c(OH-)
D.物料守恒:c(Na+)= c(A-)+ c(HA)
6.下列有关pH变化的判断中,正确的是 ( )
A. 随着温度的升高,Na2CO3溶液的pH减小。
B. 随着温度的升高,纯水的pH增大。
C. 新制氯水经光照一段时间后,pH减小。
D. 氢氧化钠久置于空气中,pH增大。
5.常温下,下列离子能使纯水中的H+离子数目增加的是 ( )
A.S2- B.CO32- C.NH4+ D.Br-
4. 25℃时,PH和体积均相等的氨水和烧碱溶液中c(NH4+)与c(Na+)关系正确的是( )
A.c(NH4+)>c(Na+) B.c(NH4+)=c(Na+)
C.c(NH4+)<c(Na+) D.无法判断
3.中和滴定是利用已知物质的量浓度的酸(或碱)来测定未知物质的量浓度的碱(或酸),若用A代表酸,用B代表碱,可以利用下式来计算未知碱的物质的量浓度的是
(ν为化学计量数) ( )
A.cB =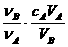 B.cB =
B.cB =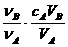 C.cB =
C.cB =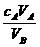 D.cB =
D.cB =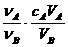
2.下列变化不属于盐类水解反应的是 ( )
①NH3+H2O NH4++OH-
②HCO3-+H2O
NH4++OH-
②HCO3-+H2O H2CO3+OH-
H2CO3+OH-
③HCO3-+H2O H3O++CO32-
④Al3++3HCO3-=Al(OH)3↓+3CO2↑
H3O++CO32-
④Al3++3HCO3-=Al(OH)3↓+3CO2↑
⑤AlO2+HCO3-+H2O=Al(OH)3↓+CO32- ⑥NH4++2H2O NH3·H2O+H3O+
NH3·H2O+H3O+
A.①③⑤ B.②③⑤ C.①④⑤ D.①③
1.用pH试纸测定溶液pH的正确操作是: ( )
A.将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照
B.将一小块试纸用蒸馏水润湿后放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照
C.将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照
D.将一小条试纸先用蒸馏水润湿后,在待测液中蘸一下,取出后与标准比色卡对照
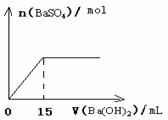
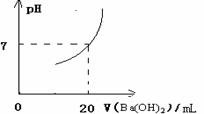
25、在20mL由HNO3和H2SO4组成的混合溶液中,逐滴加入4mol/L Ba(OH)2溶液,结果如下图所示,求原溶液中HNO3和H2SO4的物质的量浓度分别是多少?
24、 某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 。直到因加入一滴盐酸后,溶液由 色变
 为 色,并且
为止。
为 色,并且
为止。
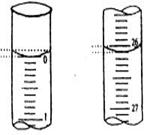
(2)若滴定开始和结束时,酸式滴定管中的液
面如图所示:则起始读数为 mL,终点读数 mL;
(3)某学生根据三次实验分别记录有关数据如下:
|
滴定次数 |
待测氢氧化钠溶液的体积/mL |
0.1000mol/L盐酸的体积(mL) |
||
|
滴定前刻度 |
滴定后刻度 |
溶液体/mL |
||
|
第一次 |
25.00 |
0.00 |
26.11 |
26.11 |
|
第二次 |
25.00 |
1.56 |
30.30 |
28.74 |
|
第三次 |
25.00 |
0.22 |
26.31 |
26.09 |
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:
c(NaOH)=
(4)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是( )
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B. 滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C. 酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定结束时俯视读数
23、(每空2分,共14分)
为了证明醋酸是弱电解质,几位同学分别选用下列试剂进行实验:0.01mol/L醋酸溶液、0.1mol/LCH3COONa溶液、pH=3的盐酸、pH=3的醋酸、CH3COONa晶体、NaCl晶体、甲基橙、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.10mol/L的醋酸溶液pH=4,则认定醋酸是弱电解质,你认为这一方法正确吗?(填“正确”或“不正确”) .
(2)乙取出10ml0.10mol/L的醋酸溶液,用pH试纸测出其pH=a,然后用蒸馏稀释到1000mL,在用pH试纸测定其pH=b,要确定醋酸是弱电解质,则a、b应该满足的关系是 (用“等式”或“不等式”表示)
(3)丙取出10ml0.10mol/L醋酸溶液,滴入甲基橙试液,显红色,再加入醋酸钠晶体,颜色变橙色,你认为这一方法能否证明醋酸是弱电解质?(填“能”或“不能”) 。
(4)丁用pH试纸来测定0.1mol/LCH3COONa溶液的pH值,发现0.1mol/LCH3COONa溶液的PH 7,则可以认定醋酸是弱电解质。
(5)戊将pH=3醋酸和盐酸,各取10ml,用蒸馏水稀释到原来的100倍,然后用pH试纸测定该溶液的pH, 的变化小,则认定醋酸是弱电解质。
(6)己将pH=3醋酸和盐酸,分别加入相应的钠盐固体,醋酸的PH变化大,则认定醋酸是弱电解质,你认为这一方法正确吗?(填“正确”或“不正确”) 。
(7)庚取pH=3的盐酸和醋酸,分别稀释到原来的100倍,然后加入完全一样的锌粒, 放出H2的速率快,就可以认定醋酸是弱电解质。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com