
题目列表(包括答案和解析)
29.下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
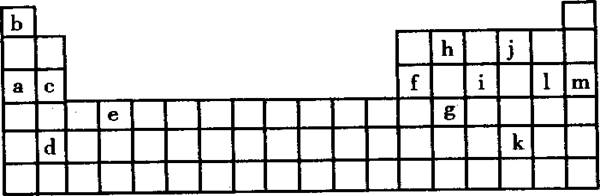
(1)下列 (填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
a.原子核对核外电子的吸引力
b.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1)。
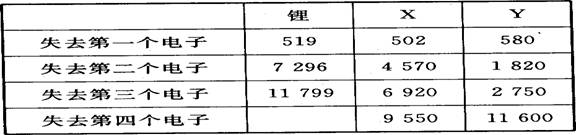
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量。
②表中x可能为以上13种元素中的 (填写字母)元素。用元素符号表示x和j形成化合物的化学式 。
③Y是周期表中 族元素。
④以上13种元素中 (填写字母)元素原子失去核外第一个电子需要的能量最多。
28.下表为元素周期表前三周期的一部分:
(1)X的氢化物的沸点与w的氢化物的沸点比较: > (填化学式),原因是
(2) X的基态原子的电子排布图为 ,另一电
子排布图不能作为基态原子的电子排布图是因为它不符合 (填序号)。
A.能量最低原 B.泡利原理 C.洪特规则
(3)以上五种元素中, (填元素符号)元素第一电离能最大。
(4)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线形分子G反应,生成两种盲线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图所示,则下列判断错误的是 。
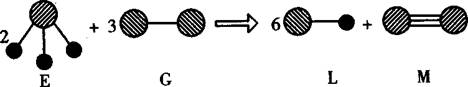
A.G是最活泼的非金属单质
B.L是极性分子
C.M的化学性质比同主族相邻元素单质的化学性质活泼
27.如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞溶液,在F极附近显红色。试完成以下问题:
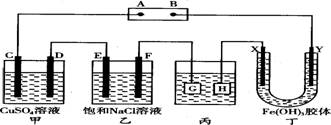
(1)电源A极的名称是 。
(2)甲装置中电解反应的总化学方程式是 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是 。
(4)欲用丙装置给铜镀银,G应该是 (填“铜”或“银”),电镀液的主要成分是 (填化学式)。
(5)装置丁中的现象是 .
说明 。
26.航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H3OH等可燃物质与02一起构成的电池装置,它可直接将化学能转化为电能。我国发射的“神舟”五号载人飞船是采用先进的甲烷电池为电能的,该电池以KOH溶液为电解质,其总反应的化学方程式为:
CH4+202+20H-==CO32-+3H20。
(1)负极上的电极反应为 。
(2)消耗标准状况下的5.6 L 02时,有 mol电子发生转移。
(3)开始放电时,正极附近溶液的pH (填“增大”、“减小”或“不变”)。
25.向明矾溶液中逐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH 7(填>、<、=),离子反应总方程式为 。
向明矾溶液中逐漓加入Ba(OH)2溶液至铝离子刚好沉淀完全时,溶液的pH 7
(填>、<、==),离子反应总方程式为 。
24.基态原子的4s能级中只有1个电子的元素共有 ( )
A.1种 B.2种 C.3种 D.8种
23.鲍林的电负性是以最活泼的非金属元素作为标度计算出来的,该元素是 ( )
A.氧 B.氯 C.氟 D.硫
22.下列说法中正确的组合是:①元素电负性越大,表示该元素的金属性越强;②元素电负性越大,表示该元素的非金属性越强;③元素电负性很小表示该元素的单质不发生化学反应;④元素电负性很大,表示该元素的单质在发生化学反应时一般得到电子 ( )
A.①③ B.①④ C.②③ D.②④
21.元素的电负性随着原子序数的递增而递增的是 ( )
A.Na K Rb B.N P As C.0 S Se D.Na P C1
20.根据下列五种元素的电离能数据(单位;kJ/mol), 回答下列问题: ,
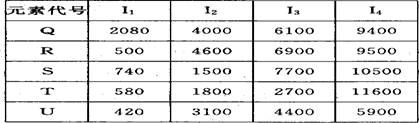
s元素最可能是 ( )
A.s 区元素 B.稀有气体元素 C.p 区元素 D.准金属
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com