
题目列表(包括答案和解析)
7.某一元弱酸HA的相对分子质量为M。在t℃时,将a gHA完全溶解于水,得VmL饱和溶液,测得该溶液的密度为ρg·cm-3,其中n(A-)为bmol。下列叙述,错误的是
A.溶液中c(H+) =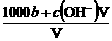 B.物质的量浓度c(HA) =
B.物质的量浓度c(HA) =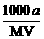 mol·L-1
mol·L-1
C.t℃时,HA的溶解度S =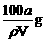 D.HA的质量分数w(HA) =
D.HA的质量分数w(HA) =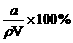
6.下列有关说法正确的是
A.H2SO4的酸性比HClO的酸性强,所以S的非金属性比Cl强
B.Mg(OH)2是中强碱,Al(OH)3是两性氢氧化物,所以Al的金属性比Mg强
C.H2S加热到300℃时开始分解,H2O加热到1000℃开始分解,说明O的非金属性比S强
D.Na和Mg与酸都能激烈反应放出氢气,因此无法比较它们的金属性强弱
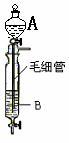
5. Inorganic Syntheses一 书中,有一如右图所示的装置,用以制备某种干燥的纯净气体。该特制的装置中所装的药品正确的是
A. A中装浓盐酸,B中装浓硫酸
B. A中装浓硫酸,B中装浓盐酸
C.A中装氢氧化钠浓溶液,B中装浓氨水
D.A中装浓氨水,B中装氢氧化钠浓溶液
4.已知在某温度下,将1 mol SO3(g)充入一定容积的密闭容器中,反应:
2SO 3 2SO2(g)+O2(g)达到平衡时,混合气体的压强比起始时增大了20%。若起始充入1 mol SO2和1 mol O2,在相同条件下建立平衡,则该情况下SO2转化率为:
A.20% B.20%--60% C.60% D.大于60%
3. t℃时,将一定量A(不含结晶水)的不饱和溶液均分为三份,分别加热蒸发,然后冷却至t ℃,已知三份溶液分别蒸发水的质量为10g、20g、30g,析出A晶体(不含结晶水)的质量依次为ag、bg、cg,则a、b、c三者的关系为
A.c = a + b B.c = 2b-a C.c = a + 2b D.c = 2a-b
2.已知
(l)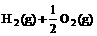 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·
(2)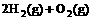 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·
(3)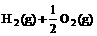 =H2O(l) △H3=c kJ·
=H2O(l) △H3=c kJ·
(4)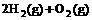 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·
下列关系式中正确的是
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
1. 10月13日有关媒体报道天津巨能化学有限公司生产的巨能钙含有双氧水,经农业部产品质量监督检验测试中心检测,部分送检品种不同程度地含双氧水。双氧水属于危险化学品及有毒有害物质,以前也曾作为漂白剂、杀菌剂、防腐剂广泛用于食品中。下列有关H2O2的叙述中正确的是
A.H2O2是二元弱酸,将H2O2溶液滴入含有酚酞的NaOH溶液中,红色消失,一定是因为发生了酸碱中和反应
B.H2O2分子中含有非极性键,因此H2O2是非极性分子
C.H2O2的自然分解过程非常缓慢,一般不易察觉,但正因为如此,一般药用的双氧水在贮存期间也会逐渐失效
D.人体中含有过氧化氢酶,过氧化氢酶可以使H2O2分解,因此人体即使吸收多量的H2O2也没有关系,可以被过氧化氢酶分解为无毒物质
32、在50 mL 0.018mol/L的硝酸银溶液中加入50mL 0.02mol/L的盐酸,生成沉淀。若在溶液中[Ag+]和[Cl-]的乘积是一个常数,即[Ag+]·[Cl-]=1.0×10-10(mol/L) 2,求:
(1)沉淀完全后溶液的pH值;
(2)沉淀完全后,[Ag+]是多少?(体积变化忽略不计)
31、已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度……。今有HA、H2B、H3C三种弱酸,根据“较强酸+较弱酸盐=较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:
(1)HA+HC2-(少量)==A-+H2C-
(2)H2B(少量)+2A-==2B2-+2HA
(3)H2B(少量)+H2C-==HB-+H3C
回答下列问题:
(1)相同条件下HA、H2B、H3C三种酸中,酸性最强的是_________。
(2)A-、B2-、C3-、HB-、H2C-、HC2-六种离子,最易结合质子(H+)的是___________,最难结合质子的是___________。
(3)判断下列离子方程式正确的是___________(填序号)。
A、H3C+3A-==3HA+C3-
B、HB-+A-==HA+B2-
(4)完成下列反应的离子方程式
A、H3C+__OH-(过量)=__________________。
B、HA(过量)+C3-=______________________。
30、 近年来,某些自来水厂在用液氯进行消毒处理时还加入少量的液氨,其反应的化学方程式为:NH3+HClO H2O+NH2Cl(一氨胺),NH2Cl较HClO稳定,试分析加液氨能延长液氯杀菌消毒时间的原因:_______________________________________________。
近年来,某些自来水厂在用液氯进行消毒处理时还加入少量的液氨,其反应的化学方程式为:NH3+HClO H2O+NH2Cl(一氨胺),NH2Cl较HClO稳定,试分析加液氨能延长液氯杀菌消毒时间的原因:_______________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com