
题目列表(包括答案和解析)
11.阿伏加德罗常数约为6.02×1023mol-1。,下列叙述中正确的是 ( )
A.在含1 mol C02的干冰晶体中含有C=O键的数目为2×6.02×1023
B.工业生产硫酸生成1 mol H2S04时实际投入的S02分子数为6.02×1023
C.78 g Na202与足量水充分反应,转移的电子数为2×6.02×1023
D.以铝、稀H2S04、NaOH溶液制备Al(OH)3,若消耗nmol H+,则消耗OH一的数目为n×6.0×1023
10.用含有少量银和锌的粗铜做阳极,纯铜片做阴极,CuS04溶液做电解液电解精炼铜,当电
路中有2 mol e一通过时,下列结论中正确的是 ( )
A,阴极质量增加65 g B.阳极质量减少216 g
C.阳极质量减少大于64 g D.电解质溶液的质量增加64 g
9.下列离子方程式正确的是 r 、
A.碘化亚铁溶液中通人少量氯气C12+2Fe2+=2C1一 + 2Fe3+
B.硫酸氢钠溶液与少量氢氧化钡溶液反应
2H+ + SO42- + Ba2+ + 20H一 =BaS04 ↓ + 2H2O
C.将等物质的量的C12和SO2同时通入水中
C12+SO2+2H20=S042-十 2Cl一 + 4H+
D.金属铝溶于氢氧化钠溶液Al +2OH一 =A!O2- + H2O
8.测试空气中污染物H2S气体含量的吸收剂,既可选用CuS04溶液,也可选用浓溴水。有关化学反应的原理为:
①Cu2+ + H2S= CuS↓ + 2H+; ②Br2+H2S=S↓ +2H+ + 2Br一。
下列说法中,正确的是 ( )
A.反应①②中,-2S 都被氧化,转化进入沉淀
B.反应①②都使反应物的某些离子浓度减小
C.以CuS04溶液为吸收剂,吸收前后溶液的导电性变化明显
D.吸收很高浓度H2S,宜选用浓溴水作吸收剂
7.中学化学教材中提供了不少数据(图表)。下列为某同学利用相关数据作出推理和判断的依据,其中不正确的是 ( )
A.依据中和热的数据,推算一定量的H2S04和NaOH的稀溶液反应的反应热
B.依据沸点的数据判断将两种互溶的液态混合物用蒸馏的方法分离开来的可能性
C.依据相对分子质量的大小,判断组成和结构相似的物质的熔、沸点的高低
D.用键能大小的数据,判断分子的稳定性
6.下列各组物质的分离、提纯或除杂,可采用相同的原理和操作方法的是 ( 1
A.除去苏打中混有的少量小苏打杂质;分离氯化钠溶液中混有的碘单质
B.除去粗食盐中的泥沙;除去氯化钾中的二氧化锰
. c.分离氯化钾与氯化钠;除去氢氧化铁胶体中混有的氯化钠
D.除去二氧化碳中混有的少量二氧化硫;除去二氧化碳中混有的少量一氧化碳
符合题意。)
1·2005年10月12日上午9:00CZ-2F火箭将“神舟六号”载人航天飞船送人太空,谱写了中国航天航空事业的新篇章。下列叙述中正确的是 ( )
A.火箭所用的燃料是气体燃料
B.宇航员呼吸所备的气体是液态氧
c.在太空失重的条件下,过滤实验较地面更易进行
D.飞船返回仓的绝热层所使用的是耐高温、抗氧化的新型无机非金属材料
2·旨在限制全球温室气体排放量的《京都都议定书》于2005年2月16日正式生效。为降低
我国二氧化碳气体排放量(居世界第二)的下列措施中,你认为不切合实际的是 ( )
A.停止使用产生二氧化碳气体的化学能
B.充分利用太阳能
C:合理、安全开发利用氢能、核能
D.因此制宜开发利用风能、水能、地热能、潮汐能
3·下列说法中,正确的是 ( )
A.离子晶体的组成中一定有金属元素
B.晶体中有阳离子就一定有阴离子 。
C.由原子组成的晶体可以是原子晶体,也可以是分子晶体
D.离子晶体不可能存在非极性共价键
4·纳米材料是纳米粒子(直径lnm--lOOnm)所组成的材料。它具有奇特的光、热、声、电、磁、力学等性质和较高的化学活性。下列分散系中不含纳米粒子的是 ( )
A.血液 B.生理盐水
C.有色玻璃 D.将FeCl3溶液滴人沸水所得的红褐色液体
5.下列说法或表示方法中,正确的是 ( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(石墨)→ C(金刚石):△H=+119 kJ/mol可知,金刚石较石墨稳定
C.在稀溶液中,H+(ag) + OH一(ag) = H20(1);△H=一57.3KJ/mol。若将含0.5mol
H2S04的浓硫酸与含1molNaOH的稀溶液混合,放出的热量大于57.3 kJ
D.在101kPa 25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,则氢气燃烧的热化学方程式表示为:2H2(g)+02(g)==2H2O(1);△H = 一285.8 kJ/mol
27.(12分)将40g铁粉放入600g稀硝酸中,若两者恰好完全反应,且稀硝酸被还原成NO,请计算:(1)稀硝酸的质量分数;(2)被还原的硝酸的物质的量。
2004-2005学年广州市高三化学调研测试(二)
26.(8分)为测定人呼出的气体中的二氧化碳的含量,将1000 mL(已按标准状况折算)呼出的气体通入50.0 mL氢氧化钡溶液中,使其完全吸收,过滤后取20.0 mL澄清溶液,用0.100 mol·L-1盐酸滴定,当消耗20.4 mL盐酸时恰好完全反应。另取20.0 mL原氢氧化钡溶液,用同种盐酸滴定,耗去36.4 mL盐酸时,恰好反应完全。试求人呼出气体中CO2的体积分数。
25.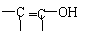 (10分)含有C、H、O三种元素的芳香族化合物A,其苯环上有两个取代基,且位置相邻。A的相对分子质量不超过200,分子中氧的质量分数为19.75%,该物质可使溴的CCl4溶液褪色,可发生银镜反应,能与钠反应产生氢气,但不能与NaOH溶液反应。已知具有烯醇式(
)结构的物质不稳定。
(10分)含有C、H、O三种元素的芳香族化合物A,其苯环上有两个取代基,且位置相邻。A的相对分子质量不超过200,分子中氧的质量分数为19.75%,该物质可使溴的CCl4溶液褪色,可发生银镜反应,能与钠反应产生氢气,但不能与NaOH溶液反应。已知具有烯醇式(
)结构的物质不稳定。
请用中学化学知识回答:
(1)A的相对分子质量为______________,A的分子式为________________________。
(2)写出符合题意的A的结构简式(任写三种)
_________________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com