
题目列表(包括答案和解析)
2.食品保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等种类。PVC被广泛地用于食品、蔬菜外包装,它对人体有潜在危害。下列有关叙述不正确的是
A.PVC保鲜膜属于链状聚合物,在高温时易熔化,能溶于酒精
B.PVC单体可由PE的单体与氯化氢加成制得
C.鉴别PE和PVC,可把其放入试管中加热,在试管口放置一湿润的蓝色石蕊试纸,如果试纸变红,则是PVC;不变红,则为PE。
D.等质量的聚乙烯和乙烯燃烧消耗的氧气相等
1.一种新型材料B4C,它可用于制作切削工具和高温热交换器。关于B4C的推断正确的是
A.B4C是一种分子晶体 B.B4C是一种离子晶体
C.B4C是一种原子晶体 D.该分子是有4个硼原子和1个碳原子构成
24. (11分)
氯酸钾 与50
mL浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2,反应的化学方程式为(未配平):KClO3+HCl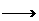 KCl+Cl2↑+ClO2↑+H2O
KCl+Cl2↑+ClO2↑+H2O
(1)配平上述反应的化学方程式:____________。
(2)浓盐酸在反应中显示出来的性质是_________(填写编号,多选倒扣分)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)若产生0.1 mol Cl2,则转移电子的物质的量为_________ mol。
(4)若反应中HCl的利用率只有50%,当产生黄绿色的气体4.2升(标况)时,求浓盐酸的物质的量浓度?
 祁阳二中2006年下期高三第一次月考
祁阳二中2006年下期高三第一次月考
23.(10分)已知在pH为4-5的环境中,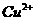 几乎不水解,而
几乎不水解,而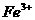 已完全水解,转化为
已完全水解,转化为 。某同学欲提纯含有少量
。某同学欲提纯含有少量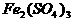 和稀
和稀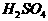 的
的 溶液,并利用电解纯净的
溶液,并利用电解纯净的 溶液得到的数据,计算Cu的相对原子质量。
溶液得到的数据,计算Cu的相对原子质量。
(1)向含有少量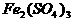 和稀
和稀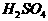 的
的 溶液中,加入稍过量的黑色粉末A搅拌、过滤,得到较纯净的
溶液中,加入稍过量的黑色粉末A搅拌、过滤,得到较纯净的 溶液。A的化学式为___________,加入A的作用是_________________________________________________________________;
溶液。A的化学式为___________,加入A的作用是_________________________________________________________________;
(2)将较纯净的 溶液放入下图所示的装置中进行电解,
溶液放入下图所示的装置中进行电解,
石墨电极上的电极反应式为_______________________________________________,
电解反应的离子方程式为_________________________________________________;
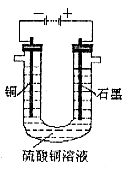
(3)实验完成后,石墨电极产生标准状况下的气体V mL,铜电极增重a g,则Cu的相对原子质量(用带有a、V的计算式表示)为________________________________。
22.(8分)通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
Si-O |
Si-Cl |
H-H |
H-Cl |
Si-Si |
Si-C |
|
键能/ KJ·mol-1 |
460 |
360 |
436 |
431 |
176 |
347 |
请回答下列问题:
 ⑴ 比较下列两组物质的熔点高低
(填>或<)
⑴ 比较下列两组物质的熔点高低
(填>或<)
SiC______ Si; SiCl4 ______ SiO2
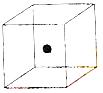
⑵ 右图立方体中心的“●”表示硅晶体中的一个原子,
请在立方体的顶点用“●”表示出与之紧邻的硅原子。
⑶ 工业上高纯硅可通过下列反应制取:
SiCl4 (g) + 2H2(g)  Si(s) + 4HCl(g)
Si(s) + 4HCl(g)
该反应的反应热△H = ___________ KJ/mol
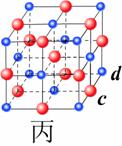
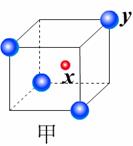
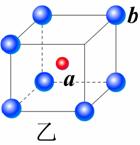
21.(6分)现有甲、乙、丙(如下图)三种晶体,可推知甲晶体的化学式为
乙晶体的化学式为 丙晶体中c与d的个数比为
20.(7分)某溶液中含有X-、Y2-、Z2-三种常见的无机离子。如下面框图所示,发生了一系列化学反应。
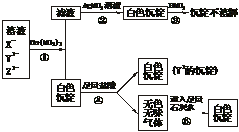
(1)判断X-、Y2-、Z2-分别为_________、_________、_________。(写离子符号)
(2)写出①②④⑤步反应的离子方程式。
①________________________________________________;
②________________________________________________;
④________________________________________________;
⑤________________________________________________。
19.用上图装置进行实验,回答有关问题:
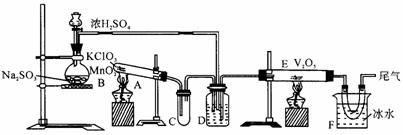
(1)玻璃管E内发生反应的化学方程式______________________________.
(2)小试管C的作用______________________________________________.
(3)广口瓶D内盛的试剂是________.
(4)从管E中导出的气体成分是________.
(5)装置F中U型管所收集的物质颜色、状态是________.
(6)若U型管内收集到的物质很少,分析其原因,不可能的是(填标号)________.a.装置气密性不好;b.制得的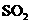 中混有少量
中混有少量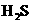 杂质使催化剂中毒;c.气流速度过快.
杂质使催化剂中毒;c.气流速度过快.
(7)从U型管导出的尾气的处理方法是________________.
17.G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的分子式或化学式,但知道它们在一定条件下具有如下的转换关系(未配平):
(1)G→Q十NaCl
(2)Y十NaOH→G十Q十H2O
(3)
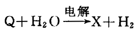 (4)Z十NaOH→Q十X十H2O
这五种化合物中氯的化合价由低到高的顺序为
A.QGZYX B.GYQZX C.GYZQX D.ZXGYQ
18.N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是
(4)Z十NaOH→Q十X十H2O
这五种化合物中氯的化合价由低到高的顺序为
A.QGZYX B.GYQZX C.GYZQX D.ZXGYQ
18.N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是
A.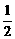 N2H4(g)+
N2H4(g)+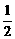 O2(g)====
O2(g)====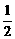 N2(g)+H2O(g);ΔH=+267 kJ·mol-1
N2(g)+H2O(g);ΔH=+267 kJ·mol-1
B.N2H4(g)+O2(g)====N2(g)+2H2O(l);ΔH=-133.5 kJ·mol-1
C.N2H4(g)+O2(g)====N2(g)+2H2O(g);ΔH=+534 kJ·mol-1
D.N2H4(g)+O2(g)====N2(g)+2H2O(g);ΔH=-534 kJ·mol-1
第II卷(选择题 共56分)
16.在25℃时,将两根铂电极插入一定量的硫酸钠饱和溶液中进行电解,当电路中有amol电子转移时,溶液中析出m g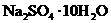 晶体.若温度不变,在剩余溶液中溶质的质量分数为
晶体.若温度不变,在剩余溶液中溶质的质量分数为
A.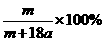 B.
B.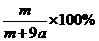
C.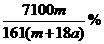 D.
D.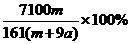
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com