
题目列表(包括答案和解析)
22.(10分)已知:
①卤代烃(或 -Br)可以和金属反应生成烃基金属有机化合物。后者又能与含羰基化合物反应生成醇:
-Br)可以和金属反应生成烃基金属有机化合物。后者又能与含羰基化合物反应生成醇:
RBr+Mg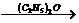 RMgBr
RMgBr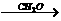 RCH2OMgBr
RCH2OMgBr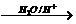 RCH2OH
RCH2OH
②有机酸和PCl3反应可以得到羧酸的衍生物酰卤:
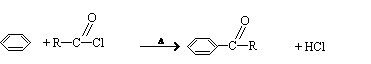
③苯在AlCl3催化下能与酰卤作用:
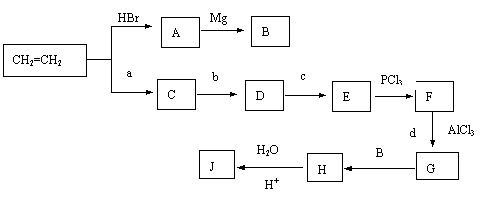 请以最基础的石油产品(乙烯、丙烯、丙烷、苯等)并任选无机试剂为原料依下列路线合成J,已知J分子式为C10H14O,
请以最基础的石油产品(乙烯、丙烯、丙烷、苯等)并任选无机试剂为原料依下列路线合成J,已知J分子式为C10H14O,
(1)写出下列反应的反应类型:C→D: F→G:
(2)写出E和J的物质的结构简式:E: J:
(2)写出下列反应方程式:
D→E:
G→H:
21.(8分)A为某芳香烃的衍生物,只含C、H、O三种元素,环上有两个取代基。又已知A的相对分子质量为150,A不能使FeCl3溶液显色,但可被新制Cu(OH)2氧化为B,B能浓硫酸存在和加热时,发生分子内的酯化反应生成C,C分子中有一个含氧的六元环。
(1)写出符合上述条件的B的可能的结构式:
(2)写出任意一种B生成的C的结构简式:
(3)含有苯环的属于酸的A的同分异构体的有 种
20.(12分)已知A是常见气体,K是石油化学工业的重要的基础原料,是一种植物生长调节剂,G是一无色液体,D、E、I、J四种物质中含同一种元素。图中一些反应条件和产物已省去。
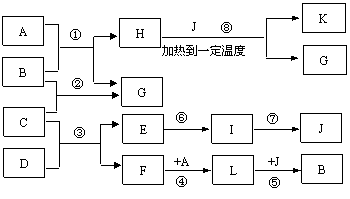
(1)工业上反应③在 _______________中进行,反应⑦在_______________(均填工业设备名称)中进行。反应⑥的条件是________ _______。
(2)除反应③、⑦外,还有 反应是工业反应。(填数字序号)
(3)反应①的化学方程式是______________________________________________。
反应③的化学方程式是______________________________________________。
反应⑧的化学方程式是______________________________________________。
19.(14分)硼酸晶体呈片状,有滑腻感,可作润滑剂,硼酸对人体的受伤组织有缓和和防腐作用,故可以用于医药和食品防腐等方面。试回答下列问题:
(1)从题目信息可知硼酸应属于 酸(弱、强、中强)
(2)硼酸的分子式为H3BO3,已知H与O成键,则其分子结构式为: 。
(3)研究表明:在大多数情况下,元素的原子在形成分子或离子时,其最外层具有达到8电子稳定结构的趋向。已知0.01mol硼酸可以被20mL 0.5mol·L -1NaOH溶液恰好完全中和,据此推测硼酸在水溶液中酸性的原因是(用离子方程式表示)
写出硼酸与NaOH溶液反应的化学方程式:
(4)硼酸和甲醇在浓硫酸存在的条件下,可生成挥发性硼酸酯,试写出硼酸完全酯化的方程式:
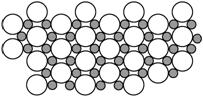 (5)科学家发现硼化镁在39 K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列,右图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据右图确定硼化镁的化学式为
(5)科学家发现硼化镁在39 K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列,右图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据右图确定硼化镁的化学式为
(6)核磁共振氢谱(PMR)是研究有机物结构的有力手段之一。在所研究的化合物分子中,每一结构中的等性氢原子在PMR谱中都给出了相应的峰(信号)。谱中峰的强度与结构中的H原子数成正比。例如:乙醛的PMR谱中有2个信号峰,其强度之比为3:1。某硼烷的核磁共振氢谱有两个峰且强度比为1:2,
已知其相对分子质量为28,试写硼烷可能的结构式
该硼烷气体在空气中能剧烈燃烧,生成1mol液态水可放出722kJ的热量,请写热化学方程式:
18.(8分)某同学查资料得知α-AgI是一种固体导体,导电率很高。他为了研究α-AgI究竟是Ag+离子导电还是I-离子导电,设计一个如下图所示(用铅蓄电池做电源)的电化学实验。
已知铅蓄电池总反应: 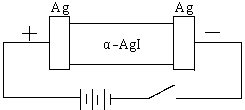 Pb+PbO2+2H2SO4
Pb+PbO2+2H2SO4  2PbSO4+2H2O
2PbSO4+2H2O
(1)该电解池的阳极电极方程式:
铅蓄电池的正极电极方程式:
(2)若Ag+导电,α-AgI本身质量将 。(填不变、变大、或变小)
若I-导电,阳极附近的α-AgI晶体密度将会 。(填不变、变大、或变小)
(3)若通电一段时间后铅蓄电池中消耗了1molH2SO4,则电解池的阴极增重 g。
17.(15分) 为清楚地看到无色NO遇空气变为红棕色(或浅棕色)的过程。某化学兴趣小组的甲、乙两位同学分别设计如下两个实验:
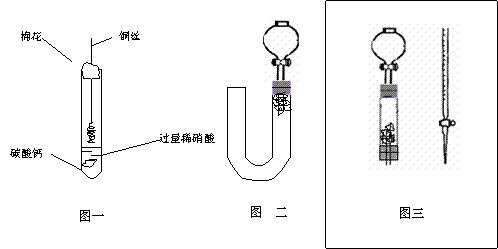
(1)甲同学实验如图一,步骤如下:①取大试管,放入适量大理石,加入过量稀硝酸 ②如图塞好疏松的棉花和铜丝 ③一段时间后,使铜丝浸入过量的硝酸反应 ④慢慢向试管底部推入棉花,可见明显现象。 第①步放入大理石的作用是:
(2)乙同学则用图二装置,他的设想是这样:从分液漏斗注入稀硝酸,直到浸没铜丝,然后,关闭分液漏斗活塞, NO产生的压强将排开稀硝酸,达一定体积后,打开分液漏斗活塞,硝酸液体将NO气体压入空分液漏斗,在分液漏斗球部空间因接触空气而变色。但按他的方法实际操作的丙同学发现此法至少存在两个问题:
①当酸液加到浸没分液漏斗下端管口以后,会 而使后面的实验无法观察到预期现象。
②反应开始后,因为随着NO的体积增加, 影响铜丝与硝酸的继续反应。
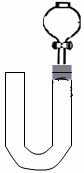 (3)丙同学将分液漏斗下端管口上提至与塞子下端齐平,解决了第①个问题,再用一个与U形管配套的单孔塞和另一个分液漏斗,仍用前述乙的仪器和思路,从左边顺利地将硝酸加到分液漏斗活塞处,请在答题卷相应图上(如左)补齐装置并特别画出铜丝的适当位置:
(3)丙同学将分液漏斗下端管口上提至与塞子下端齐平,解决了第①个问题,再用一个与U形管配套的单孔塞和另一个分液漏斗,仍用前述乙的仪器和思路,从左边顺利地将硝酸加到分液漏斗活塞处,请在答题卷相应图上(如左)补齐装置并特别画出铜丝的适当位置:
(4)丁同学根据丙的思路,认为可以测定一下NO的体积并计算其产率(不考虑有其它气体),如果给你图三所示的仪器及一个酸式滴定管,用一根橡胶皮管将它们连接起来。为成功量取产生NO的体积,此实验中注入的硝酸在滴定管中至少应到达 ,设定有条件精确称量,还
需要的数据是
(5)计算知:将等体积NO和O2通入倒置于水槽中的盛满水的试管中,充分反应后剩余气体的体积为原气体总体积的1/8,但准确的实验表明:余气体积比计算结果要大,实事求是的科学精神,要求我们应认真思考。已知氢氧化钠溶液可以吸收NO2,方程式为2NaOH+2NO2=NaNO2+NaNO3+H2O,氢氧化钠溶液可以吸收NO、NO2的混合气体,方程式为2NaOH+NO2+NO=2NaNO2+H2O,能否受此启发,写出可能发生的反应方程式,并对上述情况作一合理的解释:
16.(7分)(1)下面所列的是中学化学实验室中几种常见的仪器:
容量瓶 、酸式滴定管、碱式滴定管、温度计、量筒 、托盘天平、 普通漏斗 、烧杯
①若要进行中和滴定实验,还缺少的玻璃仪器是 ;
②若要用碳酸钠固体配制一定物质的量浓度的碳酸钠溶液,还缺少的玻璃仪器是 ;
③使用酸式滴定管的第一步操作是 ;
④中和热测定时,一次完整实验,温度计应使用 次。
(2)下列实验最后结果与理论值相比,偏小的是
A.配制一定物质的量浓度溶液时,药品与砝码放反了,游码读数为0.3g,所得溶液的浓度
B.酸碱中和滴定时,滴定终点仰视标准液滴定管读数,所得待测液的浓度
C.中和热测定实验时,用铜质搅拌棒代替环形玻璃搅拌棒,所得的中和热的数值
D.测定硫酸铜晶体结晶水含量时,坩埚内有高温不分解的固体物质,所得到的结晶水的含量
15. 某结晶水合物的化学式为A·nH2O,其相对分子质量为M,在25℃时,ag晶体溶于bg水中即达饱和,形成密度为ρg/mL的溶液,下列表达式正确的是
A.饱和溶液的物质的量浓度为:1000a(M-18n)/M(a+b)mol/L
B.饱和溶液中溶质的质量分数为:100a(M-18n)/M(a+b)%
C.饱和溶液的体积为:(a+b)/ρL
D.25℃时,A的溶解度为:a(M-18n)/(bM+18an)g
第II卷 (非选择题 共90分)
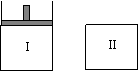
14.如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,在Ⅰ、Ⅱ中分别加入3mol Z,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):aX(?)+2Y(?) 3Z(g)。此时Ⅱ中X、Y、Z的物质的量之比为3:2:2,则下列说法一定正确的是
3Z(g)。此时Ⅱ中X、Y、Z的物质的量之比为3:2:2,则下列说法一定正确的是
A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
B.若X、Y不均为气态,则平衡时X的产率:Ⅰ>Ⅱ
C.若X、Y均为气态,则从起始到平衡所需时间:Ⅰ>Ⅱ
D.若X为固态,Y为气态,到达平衡后若在Ⅱ中再加入1molZ,则新平衡时Z的体积分数变小
13.某学生设计了如图的方法对A盐进行鉴定:
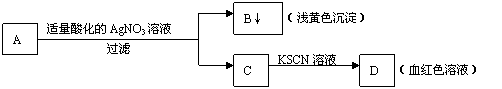
由此分析,下列结论中,正确的是
A.A中一定有Fe3+ B.C中一定有Fe3+
C.B为AgI沉淀 D.A一定为FeBr2溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com