
题目列表(包括答案和解析)
22.(12分)有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。已知:A和C、B和D分别位于同主族,且B、D质子数之和是A、C质子数之和的2倍;E在同周期元素中原子半径最小。
(1)A2B和A2D的沸点较高者是 ____________(填化学式),其原因是____
_____________;
(2)由A、B、C、D四种元素形成的两种化合物相互间反应的离子方程式为_______________。
(3)A、B、C三种元素所形成的化合物的电子式为____________。
(4)用多孔的石墨电极电解滴有酚酞的C和E形成的化合物的饱和溶液。接通电源一段时间后,_________极(填电极名称)附近出现红色;另一极的电极反应式为____________,可用________________检验该极所得产物。
21.(8分)将1 mol I2(g)和2mol H2(g)置于某2L密闭容器中,在一定温度下发生反应:
I2(g)
+ H2(g)  2HI(g);△H < 0,并达到平衡。HI的体积分数Φ(HI)随时间变化如图中曲线(Ⅱ)所示:
2HI(g);△H < 0,并达到平衡。HI的体积分数Φ(HI)随时间变化如图中曲线(Ⅱ)所示:
(1)达平衡时,I2(g)的物质的量浓度为______mol · L – 1。
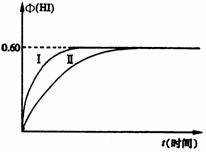 (2)若改变反应条件,在某条件下Φ(HI)的变化如曲线(I)所示,则该条件可能是________(填入下列条件的序号)。
(2)若改变反应条件,在某条件下Φ(HI)的变化如曲线(I)所示,则该条件可能是________(填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温、恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c应满足的关系为_________________(用一个含a、b、c的代数式表示)。
20.有一瓶无色溶液,可能含有K+、Al3+、Mg2+、NH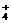 、Cl –、SO
、Cl –、SO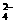 、HCO
、HCO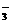 、MnO
、MnO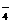 离子中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的
( )
离子中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的
( )
A.肯定有Al3+、Mg2+、NH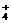 、Cl – B.肯定有Al3+、Mg2+、HCO
、Cl – B.肯定有Al3+、Mg2+、HCO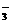
C.肯定有K+、HCO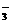 、MnO
、MnO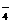 D.肯定有Al3+、Mg2+、SO
D.肯定有Al3+、Mg2+、SO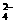
第Ⅱ卷(非选择题,共80分)
19.用溶质的物质的量浓度均为0.1 mol · L – 1的氨水和氢氧化钠溶液,分别和等体积pH = 2的盐酸反应,当盐酸恰好被完全中和时,消耗氨水和氢氧化钠溶液的体积分别是V1和V2,则V1和V2的关系正确的是 ( )
A.V1 < V2 B.V1 = V2 C.V1 > V2 D.V1≤V2
18.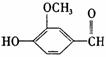 香兰素的结构简式如下图所示,它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料。下列关于香兰素的判断不正确的是
( )
香兰素的结构简式如下图所示,它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料。下列关于香兰素的判断不正确的是
( )
A.可与银氨溶液反应
B.可与氢氧化钠溶液反应
C.分子中所有原子都在同一平面上
D.可与浓溴水发生取代反应
17.将一定量Fe和Fe2O3的混合物放入2 mol · L – 1的HNO3溶液25 mL中,反应完全后,无固体剩余,生成224mL NO气体(标准状况),再向反应后的溶液中加入1 mol · L – 1的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是 ( )
A.45mL B.50mL C.40mL D.无法确定
16.下列离子方程式中书写正确的是 ( )
A.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2+ + 2H+ + H2O2 = Fe3+
+ 2H2O
B.铁与稀硫酸反应:2Fe + 6H+ = 2Fe3+ + 3H2↑
C.向氯化铝溶液中加入过量的氨水:Al3+ +
3NH3 · H2O = Al(OH)3↓+ 3NH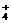
D.碳酸氢铵溶液中加入过量的氢氧化钠溶液:HCO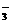 + OH – = CO
+ OH – = CO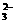 + H2O
+ H2O
15.根据等电子原理,由短周期元素组成的粒子,只要其原子数相同,各原子的最外层电子数之和也相同,可互称为等电子体。等电子体之间结构相似、物理性质相近。以下各组粒子不能互称为等电子体的是 ( )
A.CO和N2 B.O3和SO2 C.CO2和N2O D.N2H4和C2H4
14.如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是 ( )
①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐
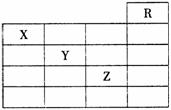 ②Y、Z的气态氢化物水溶液的酸性Y
< Z
②Y、Z的气态氢化物水溶液的酸性Y
< Z
③Z的单质在常温下是液体,可与铁粉反应
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素
A.①②③④ B.①②③④⑤
C.只有③ D.只有①④
13.将0.2 mol · L – 1的一元弱酸HA溶液和0.1 mol · L – 1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是( )
A.c (HA) < c (A – ) B.c (Na+) > c (A – )
C.c (Na+) = c (A – ) + c (OH – ) D.c (HA) + c (A – ) = 0.2 mol · L – 1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com