
题目列表(包括答案和解析)
23. (10分)水是极弱的电解质其可以发生微弱的电离, 纯水
(10分)水是极弱的电解质其可以发生微弱的电离, 纯水
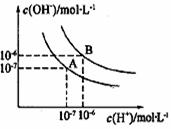
的电离平衡曲线如图所示:
⑴曲线A和B对应的温度不同,其中温度高的为 ,
在B点的纯水的PH= 呈 性
⑵曲线A对应温度下, 1 mol/L NaB溶液的pH = 9,则该溶液中各离子的物质的量浓度由大到小的顺序为 。
⑶曲线B对应温度下,pH = 2的某HA溶液和pH = 10的NaOH溶液等体积混合后,混合溶液的pH =5,结合必要的化学用语解释pH = 5的原因:
。
⑷曲线B对应温度下,若1体积的某强酸和10体积的某强碱混合后溶液显中性,则混合前强酸的pH(pH酸)和强碱的pH(pH碱)的关系为 。
22.(8分)已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复: Ba2+、H+、Na+、NH4+、CO32-、NO3-、OH-、SO42-将这4种溶液分别标记为A、B、C、D进行如下实验:
①在A或D中滴入C,均有沉淀生成
②A和B反应生成的气体能被D吸收
③A和D反应生成的气体能被B吸收
试回答下列问题:
(1)A的化学式是 ,判断的理由是
(2)写出其余几种物质的化学式:B C D
(3)写出实验②中有关反应的离子方程式 。
21.(10分)我们知道自然界中的蜘蛛丝和细菌纤维素纤维是典型的纳米纤维。较细的蜘蛛丝直径还不足100纳米,是真正的天然纳米纤维。美国与加拿大的科学家合作,采用蜘蛛基因,利用仿生结构,成功地纺制出人造蜘蛛丝,其强韧性能优于钢材。
(1)纳米纺织材料凭借其内部所特有的小尺寸效应、表面效应等日益受到广大消费者的
喜爱。许多纳米材料的粒子直径都在1-100nm之间,从分散系的角度看应该属于
(2) 纳米是长度单位,物质的颗粒达到纳米级时,具有不同的性质,如果单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,下列对“纳米铜”的说法正确的是: (填序号)
A.“纳米铜”与铜片还原性相同 B.“纳米铜”比铜片更易失电子
C.“纳米铜”比铜片的氧化性强
(3)钢铁在人们生活中应用非常广泛,但是钢铁因腐蚀造成的损失全球每年高达7000亿美元,目前钢铁被腐蚀的主要形式是吸氧腐蚀,其正极发生 反应,负极发生的电极反应式为 。为了减少这种腐蚀生产生活中常见的有哪些防腐措施: 。(至少填两种措施)
20.(10分)已知A为常见金属,在空气中燃烧发出耀眼的白光,X、Y为常见非金属,X、E、F、G常温常压下为气体,C为液体,B是一种盐,受热易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现在A与石墨作电极,B的浓溶液作电解质溶液,构成原电池。
请填写下列空白:
(1) 反应④为在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为
(2) 反应②的化学方程式为
(3) 从D溶液制备D的无水晶体的“操作a”为
(4) 工业上常利用电解熔融D的无水晶体来制取A,而不用电解熔融A的氧化物来制取A,简述理由
(5) 为了较准确测定G气体的相对分子质量,对测定条件有何要求
19.(9分)已知A、B、C、D均为短周期元素,它们的原子序数依次递增。 A单质是自然界中密度最小的气体,C 原子的最外层电子数是次外层的3倍; C和D可形成两种固态化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物。A、B、C三种元素可以形成离子晶体,该晶体可以和氢氧化钠反应放出无色刺激性气味气体E。请回答下列问题:
(1) 写出B单质的电子式 ;C和D形成淡黄色固体化合物电子式 。
(2)元素原子的物质的量之比为A:B:C=4:2:3 的晶体名称为 其水溶液
显 性,用离子方程式说明 。
(3) E分子的空间构型是 ,属于 分子(填极性或非极性)
(4) A、B、C三种元素还可以形成另一种化合物,其热的浓溶液可以溶解铝和铁,但常
情况下它的浓溶液又可盛放在铝或铁制的容器中,原因是
。
18.(14分)钠和氯气反应可以在下面的试验装置中完成,将新切取并用滤纸吸去煤油的一小块钠,放入具支试管中,然后按照图组装好,
加热金属钠,到钠熔化成光亮的球状时,立即
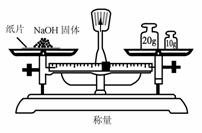 通入氯气,并停止加热,此时可看到钠剧烈燃
通入氯气,并停止加热,此时可看到钠剧烈燃
烧并生成大量白烟,片刻,试管内壁各处都附
着一层白色固体。请完成下面问题:
⑴停止加热,反应仍能继续进行,说明该反应是 反应。(填放热或吸热)
⑵有时熔融的钠跟氯气接触时会产生黑烟,这是因为 。
⑶具支试管的支管应通到10%的NaOH溶液中,防止 。
⑷钠刚熔化时就要通入氯气,如果熔化前通氯气或熔化后还不通氯气都会影响实验效果,为什么 。
⑸通入氯气的量不要太多以免 但也不能太少,以免 。
(6)有同学想证明白色固体就是NaCl,应补充什么实验来说明
。
17.(6分)下列操作或说法合理的是
A.用10毫升的量筒量取4.80毫升的浓硫酸
B.金属钠着火,用泡沫灭火器扑灭
C.用胶头滴管向试管滴液体时,滴管尖端与试管内壁一般不应接触
D.用盐酸可以清洗长期存放过石灰水的试剂瓶
E. 配制FeCl3溶液时,向溶液中加入少量Fe和稀硫酸
F.用已知浓度的酸滴定未知浓度的碱时,碱式滴定管用蒸馏水洗后,未用待测液润洗会导致测量的浓度偏低
16. 时钟反应或振荡反应提供了迷人课堂演示实验,也是一个活跃的研究领域。测定含I-浓度很小的碘化物溶液时,利用振荡反应进行化学放大,以求出原溶液中碘离子的浓度。主要步骤如下:
①在中性溶液中,用溴将试样中I-氧化成IO3-,将过量的溴除去。
②再加入过量的KI,在酸性条件下,使IO3-完全转化成I2。
③将②中生成的碘完全萃取后,用肼将其还原成I-,方程式为:N2H4+2I2==4I-+N2+4H+
④将生成的I-萃取到水层后用①法处理。
⑤将④得到的溶液加入适量的KI溶液,并用硫酸酸化。
⑥将⑤反应后的溶液以淀粉作指示剂,用Na2S2O3标准液滴定,方程式为:2Na2S2O3+I2==Na2S4O6+2NaI
经过上述放大后,则溶液中I-浓度放大为原溶液中I-浓度的(设放大前后溶液体积
相等): ( )
A.2倍 B.4倍 C.6倍 D.36倍
15. 合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g
)+3H2(g) 2NH3(g),△H ﹤0。673K、30Mpa下n(NH3)和n(H2)随时间变化的
2NH3(g),△H ﹤0。673K、30Mpa下n(NH3)和n(H2)随时间变化的
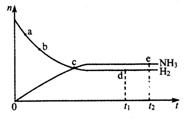 关系如图所示。下列叙述正确的是:( )
关系如图所示。下列叙述正确的是:( )
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,
n(H2)比图中d点的值小
14.  随着石油资源不断减少,石油价格不断上扬,相对环保型的电瓶车愈来愈受到人们的喜爱。电瓶车所用电池一般为铅蓄电池,这是一种可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42-
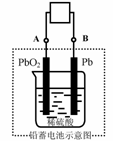
随着石油资源不断减少,石油价格不断上扬,相对环保型的电瓶车愈来愈受到人们的喜爱。电瓶车所用电池一般为铅蓄电池,这是一种可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O 则下列说法正确的是
2PbSO4+2H2O 则下列说法正确的是
A.放电时:电子流动方向由A到B
B.放电时:正极反应是Pb-2e-+SO42-=PbSO4
C.放电时:B极为负极,A极为正极
D.充电时:阳极反应是PbSO4-2e-+2H2O=PbO2+SO42-+4H+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com